
Retour au sommaire des cours |

Une version pdf est à votre disposition ici. |
� Je le
r�p�te chaque ann�e et je ne le vois pas dans la moiti� des copies.
Alors,
je ne cesserai pas de vous le r�p�ter tout le long de ce cours et �a ne sera
pas de trop� �
Les lymphocytes B et T sont les 2 types de cellules importantes dans
la r�ponse immune car ils poss�dent des r�cepteurs sp�cifiques aux antig�nes.
Il
existe dans l�environnement de nombreux micro�organismes qui attaquent notre
organisme. Il doit donc avoir une d�fense : le syst�me immunitaire qui
permet de d�velopper des r�ponses immunes.
Immunit� :� R�sistance des individus vis���vis d�agents
infectieux.
Immunologie :� Etude de l�immunit� vis���vis d�agents
infectieux.

Anticorps
:� Mol�cule de nature prot�ique produite par la
ligne B (chez les vert�br�s) en r�ponse � un antig�ne en se liant � celui�ci de
mani�re sp�cifique.
Antig�ne :� Mol�cule qui induit sp�cifiquement la
production d�anticorps.
v Les cellules impliqu�es
dans la r�ponse immune :
Toutes
les r�ponses immunitaires ont la m�me origine : une origine
h�matopo��tique.
Il
y a aussi d�autres cellules avec une autre
origine comme les cellules �pith�liales
De cette origine, 2 lign�es se
distinguent :
-
La
lign�e lympho�de : Lymphocytes T et B (en priorit�),
-
La
lign�e my�lo�de avec :
-
Les
polynucl�aires et les macrophages,
-
Les
m�gacaryocytes et les plaquettes,
-
Ainsi
que les globules rouges.
Immunit�
sp�cifique :
Elle
est appel�e aussi immunit� humorale. Elle est due � la lign�e lympho�de.

 ������������������������������ BCR (B_Cell receptor)�������������������� TCR (T_Cell receptor)
������������������������������ BCR (B_Cell receptor)�������������������� TCR (T_Cell receptor)
������������������������������ (=
Immunoglobuline
������������������������������ ���� de membrane)
Les
lymphocytes T s�cr�tent des cytokines (CK, anciennement lymphokines)
On parle
d�immunit� � m�diation cellulaire.
On
observe un ph�nom�ne m�moire :
la r�ponse immunitaire augmente en rapidit� (et donc en efficacit�) lors d�une
r�infection.
On parle
d�immunit� acquise ou immunit� adaptative.
Immunit� non
sp�cifique :
Elle est appel�e aussi immunit� inn�e ou naturelle.
Elle est due � la lign�e my�lo�de, notamment les polynucl�aires et les
macrophages (fonction de phagocytose)
La r�ponse immunitaire est basique : il n�y a
pas de ph�nom�ne m�moire. Elle consiste en l�action :
-
Du
lysosyme (au niveau des muqueuses) = substance prot�ique qui d�truit l�antig�ne
infectieux,
-
Du
compl�ment qui augmente le processus inflammatoire en stoppant la
progression de l�antig�ne et en favorisant l�opsonisation (phase de
phagocytose),
-
Les
interf�rons a,
b
et g
(mais surtout a et b) qui ont une
action antivirale.
 Antig�ne
Antig�ne
Lymphocyte
Cellule
phagocytaire
Destruction
de l�antig�ne pi�g� dans la cellule phagocytaire
������
Anticorps
Cytokines
D� Notion de clonalit� pour les lymphocytes B et
T.
Phagocytes
![]()

La lign�e
lympho�de :

����������������������������������������������������������������� Cytokine
������� ����������� �����Cytokine
Anticorps
����������������������������������������������������������������������������� Macrophages,
polynucl�aires (lign�e my�lo�de)
Lymphocyte B
Lymphocyte T

La
phagocytose :
-
Adh�sion (ou
opsonisation) :
Il
y a des facteurs cellulaires et extracellulaires : pH, temp�rature,
pr�sence d�ions (notamment le Ca2+ et Mg2+) et la pr�sence
opsines (mol�cules s�riques interm�diaires entre les cellules et les antig�nes)
qui se fixent sur des r�cepteurs aux opsines, dont les RFC.
-
Ingestion :
Elle
consiste en la formation d�un phagosome. On observe un changement de pH
(acidification)
-
Digestion :
Elle
consiste en une d�gradation enzymatique (lyse) et une exocytose des d�bris. La
lyse se fait par 2 m�canismes : un d�pendant de la consommation d�O2 et un
ind�pendant.
L�augmentation
de la consommation d�O2 entra�ne une
augmentation du catabolisme du glucose et donc une augmentation des radicaux
libres, ensuite oxyd�s en H2O2.
La
phagocytose est �tudi�e dans l��ventualit� de traitement des tumeurs et des
inflammations. Comme tout m�canisme, il peut pr�senter des pathologies
(attaques de cellules normales)
Les polynucl�aires
neutrophiles :
Ils sont caract�ris�s par la pr�sence de granules
colorables (colorant basique comme le bleu de m�thyl�ne ou colorant acide
comme l��osine) Il existe :
-
Des
granules IAIRES : les
lysosomes,
-
Des
granules IIAIRES : les plus
dense et un peu plus petites,
-
Des
peroxysomes qui contiennent des peroxydases.
Les
polynucl�aires neutrophiles pr�sentent une chimiotactie : ils peuvent se
d�placer sur le site de l�agression.
Ils phagocytent
surtout des bact�ries et des levures.
Les
polynucl�aires eusitophiles :
Ils
ont des granules (colorables) sous forme de cristaux (structure cristallo�de)
qui contiennent des enzymes (en majorit� des lysophospholipases)
Leur nombre
augmente avec l�infection par des helminthes (vers plats) Ils sont stimul�s par
certaines immunoglobulines.
Les
polynucl�aires basophiles :
Ils
sont rares. Ils poss�dent des granules particuli�res que l�on met en �vidence
par des colorations basiques. Ces granules contiennent des enzymes dont
l�histamine et l�h�parine (m�diateurs pr�form�s)
"� Ils interviennent dans les r�actions
allergiques.
L�allergie est
une pathologie du syst�me immunitaire. Il s�agit d�une hypersensibilit� de type
I.
IgE

Normalement, les
IgE (produites par les lymphocytes B sp�cifiquement en r�ponse � l�allerg�ne)
disparaissent en quelques jours. Mais elles peuvent se fixer sur un
polynucl�aire basophile. Ce dernier effectue un � comptage � et, si
les IgE sont en trop forte quantit�, il lib�re de l�histamine.
Les monocytes
(circulants) et macrophages (fix�s dans un tissu) :
Ils
pr�sentent un noyau en forme de fer � cheval et un cytoplasme granuleux
(lysosymes, peroxydases, etc.)
La
transformation des monocytes en macrophages est stimul�e par des cytokines.
Ils
causent la destruction des cellules cibles par cytotoxicit� et d�gradation
enzymatique. Ils constituent le syst�me r�ticulo�histiocytaire.
Les macrophages :
Ils
sont pr�sents un peu partout dans l�organisme (poumons, foie, os, tissus
lympho�des, etc.)
-
Ils
ont la capacit� de s�infiltrer dans les tissus et fixer les particules
�trang�res (r�ponse immunitaire non sp�cifique)
-
Ils
informent aussi le syst�me immunitaire de la pr�sence d�antig�nes : les macrophages sont des CPA (cellules
pr�sentatrices d�antig�nes)
Les
m�gacaryocytes :
Ce
sont des cellules g�antes avec beaucoup de cytoplasme. Ce dernier se fragmente
pour former les plaquettes (absence de noyau)
Les
plaquettes ont un r�le dans le m�canisme de l�hom�ostasie, mais elles n�ont
qu�un faible r�le dans la r�ponse immune : activation des lymphocytes et
des polynucl�aires neutrophiles.
Les
�rythrocytes :
Ce
sont les globules rouges. Leur r�le majeur est le transport de l�O2, mais ils
participent aussi � la r�ponse immune en �liminant le complexe immun.
Les cellules NK
(natural killer) :
Elles
permettent l��limination des cellules tumorales. Elles pr�sentent des �l�ments
membranaires communs aux lymphocytes T.
v Les organes
lympho�des :
Tous les organes lympho�des comportent un syst�me
sanguin et un syst�me lymphatique. Il existe 2 types d�organe lympho�de :
-
Les
organes lympho�des IAIRES (ou
centraux) : la moelle osseuse et le thymus,
-
Les
organes lympho�des IIAIRES (ou
p�riph�riques) :
-
Les
organes lympho�des encapsul�s : la rate, les ganglions lymphatiques, etc.
-
Les
organes lympho�des non encapsul�s (ou diffus) : tissus associ�s � des
muqueuses. Exemples :
-
GALT :
tissu associ� � l�intestin (= gult en
anglais),
-
MALT :
tissu associ� aux muqueuses.
Le
passage d�un organe lympho�de IAIRE � un organe
lympho�de IIAIRES se fait par le
syst�me sanguin.
� Le
thymus :
Il
se situe dans le thorax. C�est un organe lympho�de encapsul� par une enveloppe
de tissu conjonctif. Le thymus involue en �lots thymiques � la pubert�.
Chez les
mammif�res et les oiseaux, il appara�t lors de la 7�me semaine de
d�veloppement.
Pathologie :
Le
syndrome de Di�George est une maladie cong�nitale qui consiste en l�absence de
thymus durant le d�veloppement. Cette absence est souvent que partielle. Elle
cause l�absence de lymphocytes T et une diminution des B (absence de r�ponse
immune sp�cifique)
Des cellules d�origine �pith�liale (cellules
� nurse �) servent de support des lymphocytes T et aide � leur
diff�renciation par la s�cr�tion d�hormones.
Lors de la
diff�renciation, il y a beaucoup de perte (apoptose fr�quente) ; c�est
pourquoi il y a une forte pr�sence de macrophages.
 Cortex (zone
corticale) :��� ����������� LT immatures : CD� et CD����������� ������� Cellules peu d�velopp�es
Cortex (zone
corticale) :��� ����������� LT immatures : CD� et CD����������� ������� Cellules peu d�velopp�es
������������������ Superficiel
����������������������������������������������������� LT
immatures : CD1 et CD2
������������������ Profond
Zone
cortico�m�dulaire
����������������������������������������������������� LT
immatures : TCR, CD3 et CD2 ( ?)
����������������������������������������������������� LT
matures : TCR, CD� et CD4 ou CD8
M�dula (zone
m�dullaire) ���������� ���������������������������������������������������������� ���Cellules tr�s d�velopp�es
� La
moelle osseuse :
Elle
est mise en place vers les 9�10�mes semaines.

���������������������������������������������������������������������������������������������������������������� Sang
����������������������������������������� Pr� B�� "������� "������� "������� "� LB mature &
� La
rate :
Elle est situ�e dans la partie gauche de l�abdomen,
derri�re l�estomac. Elle est tr�s �tudi�e dans les rejets de greffe. Elle joue
le r�le de filtre.
On observe 2
r�gions : la pulpe blanche et la pulpe rouge (�limination des h�maties)
 �����������������������
����������������������� 

� Les
ganglions lymphatiques :
Ils constituent la cha�ne ganglionnaire. Ils ont
aussi un r�le de filtre (pr�sence de macrophages)
La
formation lympho�de se fait autour des vaisseaux lymphatiques.
On y observe
aussi des lymphocytes T et B en fin de diff�renciation.
Cortex :
follicules lymphoides :
Paracortex :
zone thymo-d�pendante :
R�gion m�dullaire :
zone mixte :
Cellules B et plasmocytes, cellules T, macrophages
Lymphocytes T et macrophages
Cellules B, quelques T, cellules dendritiques
Capillaires lymphatiques aff�rents

![]() ��
Aorte���������� ��
Veine���������������������� Hile
��
Aorte���������� ��
Veine���������������������� Hile
����������������������������������������������������� Capillaire
lymphatique eff�rent
v M�canisme du Homing et
circulation lymphocytaire :
La
population des lymphocytes B et T est tr�s diverse et doit reconna�tre le
� non�soi � uniquement. Il faut donc lui apprendre � aller vers
celui�ci. Ceci n�cessit� une coop�ration entre les lymphocytes B et T, ainsi
qu�une r�ponse fonctionnelle.
L�environnement du lymphocyte est
capable de jouer un r�le sur l�hom�ostasie du syst�me immun. Pour pr�server
cette hom�ostasie, il faut 2 m�canismes :
-
La
circulation des lymphocytes,
-
Le
homing (= reconnaissance)
Les
cellules endoth�liales et des mol�cules d�adh�sion sont impliqu�es dans cette
hom�ostasie en permettant la fixation lympho�endoth�lium (liaison
ligand�r�cepteur)
Conclusion :
Les lymphocytes sont programm�s :
-
Au
d�part, ils sont � na�fs � (cad : sans avoir rencontr�
d�antig�ne)
-
Ils
font 2 ou 3 fois le tour de la circulation avant de rencontrer un antig�ne
(probabilit� de rencontre)
-
Une
fois l�antig�ne rencontrer, il termine sa diff�renciation et d�veloppe soit un
m�canisme effecteur, soit un m�canisme m�moire.
Il
faut comprendre les interactions cellule � cellule :
-
Ligand� +�
R�cepteur
-
Antig�ne� +�
Anticorps
-
Cytokine� +�
R�cepteur
-
Substrat� +�
Enzyme� �� Complexe
Enzyme�Substrat
-
Liaison
forte :������ Liaison covalente
" N�cessit�
d�enzymes, d�hydrolyse, d��nergie pour les casser
(Exemple :
pont disulfure)
-
Liaison
faible :����� Liaison hydrog�ne
(entre H et un atome plus �lectopositif comme O),
Liaison
�lectrostastique (entre des particules charg�es : force de Van der Waals),
Liaison hydrophobe (quand des mol�cules d�eau
entourent des groupements non polaires)

En
immunologie, on caract�rise la liaison antig�ne�anticorps comme �tant une
liaison exothermique (2 � 40 Cal) Il s�agit d�une liaison sp�cifique
r�versible.
"� Antig�ne�
+� Anticorps� �� Antig�ne�Anticorps
La
dissociation est possible par la chaleur, le pH ou avec un apport de cations.
L�affinit� est
l�intensit� des forces qui vont participer � la liaison antig�ne�anticorps.
La
pente k correspond au facteur d�association ou de dissociation.

����������������������������������������������������������������� Pente
k forte : grande
affinit�
104�
<� k� <� 1012
����������������������������������������������������������������� Pente
k faible : peu d�affinit�
En
immunologie, la constante k varie entre :������ 107 � 1010 � "� Faible affinit�
����������������������������������������������������������������������������� 1010 � 1013 � "� Forte affinit�
L�avidit� d�un anticorps
pour un antig�ne sp�cifique est caract�ris�e par la rapidit� de la r�ponse
immune. Elle d�pend :
-
De
la constante d�association,
-
De
la balance de l�anticorps,
-
Du
nombre d��pitopes.
v Structure des
immunoglobulines :
Le
plus souvent, on �tudie l�immunoglobuline de classe G (IgG)
Mais il existe 5 classes : A, D, E,
G et H. Ces diff�rentes classes pr�sentent des points communs :
-
Mol�cule
sym�trique,
-
Constitu�e
de cha�nes polypeptidiques de 2 cat�gories :
-
Des
cha�nes lourdes ou cha�nes H (heavy),
-
Des
cha�nes l�g�res ou cha�nes L (light)
-
Stabilit�
par des ponts disulfure.

Sp�cificit� :
Le nom de la cha�ne lourde d�termine le nom de
l�immunoglobuline :
-
a, d, e, g ou m " cha�nes
lourdes,
-
k ou l " cha�nes
l�g�res.
Exemple :� (H2 k2) ou (H2 l2) qui peut �tre
r�p�t� n fois :
-
n
=1 :� Ig monom�rique qui existe dans
toutes les classes,
-
n
=2 :� pour les IgA et certaines IgM,
-
n
=5 :� pour les IgM (= IgM
pentam�riques)
Il
existe des sous�classes, essentiellement pour les IgG qui pr�sentent 4
sous�classes dues � des variantes de la cha�ne lourde (g1, g2, g3 et g4), mais aussi
pour les IgA (a1 et a2)
Rappels sur la
nomenclature :
Elle
a �t� �tablie � l�aide de 2 enzymes couramment utilis�es : la papa�ne et
la pepsine.
Disparition de la r�gion
C_terminale par r�duction

Fab = Fragment � antigen
binding �
Fc = Fragment cristallisable
(C�est le site
de fixation du compl�ment)
Remarque :
Les
anticorps peuvent se fixer sur les antig�nes (au niveau du Fab) mais peuvent
aussi se fixer sur des cellules de l�organisme (au niveau du Fc) ce qui peut
entra�ner des faux positifs dans les exp�riences. C�est pourquoi les
laboratoires utilisent des fragments F(ab�)2.
-
Il
existe des ponts disulfures entre 2 cha�nes diff�rentes (ponts disulfures
intercha�nes) et des ponts disulfures � l�int�rieur de la cha�ne (ponts
disulfures intracha�nes)
-
Les
extr�mit�s NH2 sont le site de liaison �
l�antig�ne.
-
Il
existe 2 r�gions principales (ou domaines) :
-
R�gions
variables :� VL et VH,
-
R�gions
constantes :� CL, CH1, CH2, CH3 et CH4 (plusieurs
cat�gories de r�gion constante et parfois plus comme chez les IgM et IgE)
-
La
r�gion de reconnaissance de l�antig�ne est une r�gion hypervariable pour
s�adapter � la diversit� antig�nique.

� Les
IgA :
Elles
pr�sentent 2 cha�nes lymphocyte (l ou k) et 2 cha�nes H de sous�classes a1 et a2.
Il existe des
IgA :
-
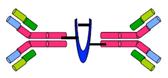 Monom�riques (⅔ des IgA du
sang)
Monom�riques (⅔ des IgA du
sang)
-
 Dim�riques, qui
sont reli�es d�une pi�ce de jonction (= cha�ne J) par des liaisons covalentes
avec les avant�derni�res cyst�ines de la partie C�terminale de chacune IgA.
Dim�riques, qui
sont reli�es d�une pi�ce de jonction (= cha�ne J) par des liaisons covalentes
avec les avant�derni�res cyst�ines de la partie C�terminale de chacune IgA.
-
S�cr�trices,
qui sont retrouv�es dans les s�cr�tions (en particulier dans les s�cr�tions
intestinales, mais aussi dans la salive, les bronches, etc.) Elles pr�sentent
une pi�ce s�cr�trice (ou s�cr�toire) synth�tis�e au niveau des cellules
�pith�liales.
Exemple :� L�intestin :
La
pi�ce s�cr�trice a pour fonction de prot�ger l�IgA dim�rique de la d�gradation
enzymatique.

Il existe surtout des IgA2 : les IgA1 sont plus
fragiles aux prot�ases.
 Les
IgM :
Les
IgM :
Elles pr�sentent 4 cha�nes H de classe m.
Elles existent sous forme soluble ou
membranaire. Sous forme soluble, il y a la formation d�IgM pentam�rique (n = 5)
li�e par une pi�ce de jonction.
Chez
l�homme, la forme principale est la forme pentam�rique. Chez la souris, il
existe parfois des hexam�res. Les monom�res constituent la plupart de nos BCR.
� Les
IgD :
Elles
sont monom�riques. Comme les IgM, elles sont peu nombreuses dans le sang (inf.
� 1%) Ceci est d� � leur tendance � la prot�olyse et au fait qu�elles sont la
plupart du temps fix�es � la membrane pour la reconnaissance de l�antig�ne.
Il
est donc difficile de les �tudier en dehors d�une situation pathologique
(my�lome d�IgD)
� Les
IgE :
Elles sont monom�riques et poss�dent 4
cha�nes constantes. Elles sont pr�sentes en faible concentration dans le sang.
Elles sont responsables du d�veloppement d�une
hypersensibilit� de type I (allergie)
En effet, elles
sont capables de se fixer par leur Fc sur les polynucl�aires basophiles et les
mastocytes, entra�nant la lib�ration d�histamines.
|
|
IgG |
IgD |
IgA |
IgD |
IgE |
|
Proportion dans le sang |
Dont |
|
|
Traces |
Traces |
|
Poids mol�culaire |
155 000
Da |
950 000
Da |
170 000
Da Pour
le pentam�re |
180 000
Da |
190 000
Da |
|
Formes |
(g2
l2) (g2
k2) |
(m2
l2) x5 + J (m2
k2) x5 + J |
(a2
l2) (a2
k2) (a2
l2) x2 + J (a2
k2) x2 + J (a2
l2) x2 + J + CS (a2
k2) x2 + J + CS CS =
composante s�cr�trice |
(d2
l2) (d2
k2) |
(e2
l2) (e2
k2) |
v R�arrangement des
immunoglobulines :
Comment dans une
m�me prot�ine
peut�il y avoir
des s�quences variables et constantes ?
Le
nombre d�antig�nes s��l�ve � 109 � 1010. Notre syst�me
immun doit pouvoir faire des r�cepteurs pour reconna�tre les antig�nes et
fabriquer des anticorps pour y r�pondre.
Au
d�but, on partait sur l�hypoth�se de base qu�un g�ne codait pour une prot�ine.
Mais il aurait alors fallu 109 � 1010 g�nes codant
uniquement pour les diff�rentes immunoglobulines. Cette hypoth�se a donc �t�
revue : un g�ne pour plusieurs produits prot�iques.

������ Duplications g�niques
= Super�famille
des immunoglobulines
Il existe un m�canisme responsable de
cette synth�se : c�est le r�arrangement des immunoglobulines. Il est
d�crit dans le syst�me lympho�de uniquement.
Pour
qu�une immunoglobuline soit fonctionnelle, il faut un r�arrangement des g�nes
fonctionnel.
� M�canisme
de recombinaison (ou r�arrangement) g�nique :
� Les cha�nes k :
Les
g�nes se situent sur le chromosome 2.
Une
cha�ne k est constitu�e
d�une r�gion V et une autre C. Il y a la n�cessit� de 3 cat�gories de
g�nes : C, V et J.
Description
avant et apr�s r�arrangement :
-
Sur
l�ADN, il y a plusieurs g�nes impliqu�s (V, J et C)
-
Les
g�nes V : 150 � 300 g�nes diff�rents (dans la r�gion
-
Les
g�nes J : un peu plus de 5 g�nes diff�rents,
-
Un
seul g�ne C.
-
Les
g�nes V et J sont s�par�s par plusieurs centaines de kb.
-
Il
y a la pr�sence d�une s�quence leader (L) devant chaque g�ne V qui dispara�t
sur la derni�re �tape de maturation de la prot�ine (protection)
-
La
cha�ne C est cod�e par le g�ne C ; la cha�ne V est cod�e par un
r�arrangement de V et J.
-
Il
y a syst�me de � couper�coller � pour donner une nouvelle structure
V�J :
-
Coupure
en
-
Elimination
de la partie entre�deux,
-
Association
des brins.
D Le terme de
� couper�coller � n�est pas � r�utiliser (dans une copie par exemple)
C�est juste pour faire comprendre le
m�canisme.
Ce
m�canisme de r�arrangement est al�atoire, mais il est sous le contr�le de
m�canismes mol�culaires.
![]()

El�ments de
contr�le :
-
Pr�sence
de s�quences hepta�nonam�res (= RRS
= Recombinaison Signal Sequence)
-
Heptam�re :
-
 Nonam�re :
Nonam�re :
-
Elles
sont s�par�es par 23 pb du cot� du g�ne V et de 12 pb du cot� du g�ne J.
-
Elles
suivent la loi des 12�23 qui consiste en la compl�mentarit� des bases
entra�nant un rapprochement des g�nes V et J.
-
Pr�sence
de la recombinase. Il s�agit d�une
enzyme sp�cifique de la lign�e lympho�de qui emp�che les recombinaisons
ill�gitimes. Pour cela, elle poss�de 2 activit�s : endonucl�ase et ligase.
-
Les
g�nes RAG1
et RAG2 (= Recombinaison ou Recombinase Activating Gene)

����������������������������������������������������������������������������� Coding
ends�����
![]()
![]() Signal ends�
Signal ends�
Prot�ines synth�tis�es par RAG1 et RAG 2
Ce
sont des �l�ments sp�cifiques de la lign�e lympho�de et du r�arrangement.
-
-
L�ac�tylation des histones peut modifier
la structure de la chromatine. Sans l�ac�tylation, la recombinase et les
prot�ines de RAG1 et RAG2 ne pourraient
pas reconna�tre les s�quences hepta�nonam�res.
� Les cha�nes l :
Les
g�nes se situent sur le chromosome 22.
-
Sur
l�ADN, il y a plusieurs g�nes impliqu�s (V, J et C)
-
Il
y a autant de g�nes J que de g�nes C.
![]()
Leader
Elimination
Dans les r�gions variables, il existe
des r�gions hypervariables. Elles sont sous le contr�le de mutations somatiques (hypersomatiques) Elles sont plus tardives que
les autres m�canismes.
C�est
une sp�cificit� de la lign�e des lymphocytes B (environ 1000 mutations par
division cellulaire)
On
pense qu�elles ont lieu surtout dans les organes lympho�des IIAIRES.
� Les cha�nes lourdes :
Les
g�nes se situent sur le chromosome 14.
-
Sur
l�ADN, il y a plusieurs g�nes impliqu�s (V, D, J et C)
![]()
-
1�re
recombinaison :� D " J
-
2�me
recombinaison :� V " D

Bloc de g�nes de
C :
![]()
l :
S�quence Switch.
Elle est pr�sente devant chaque g�ne C (sauf pour le g�ne Cm)
La
1�re cha�ne lourde synth�tis�e est une cha�ne lourde m : IgM (= immunoglobuline
membranaire) Parfois, cela peut aussi �tre une IgD.
Immunoglobuline
membranaire :
Les IgM et les IgD sont, pour la plupart du temps,
fix�s. Dans le cas o� les IgM sont s�cr�t�es, elles forment des pentam�res.
Les transcrits
sont faits avec Cm et Cd ou avec Cm seulement. La
s�lection se fait ensuite avec un �pissage alternatif.
Cm et Cd sont sous le
contr�le de la m�me s�quence S. Le fait que Cm et Cd soient les 1ers
� �tre synth�tis�s s�explique par le fait qu�ils soient les plus proches.
Immunoglobulines s�cr�t�es :
La s�quence synth�se est responsable de
la commutation des cha�nes lourdes des immunoglobulines. La commutation est la
recombinaison entre 2 s�quences synth�se et l��limination de ce qu�il y a
entre�deux.
Cette
recombinaison est irr�versible et conduit � l��volution clonale.
|
|
V |
D |
J |
C |
|
|
Cha�ne L |
k |
Inf. � 300 |
� |
5 |
1 |
|
l |
Inf. � 300 |
� |
6 |
6 |
|
|
Cha�ne H |
Inf. � 300 |
~ 30 |
6 |
9 |
|
Cha�ne l�g�re :
( 300 x 5 ) (recombinaison V�J)� x� 4 (TdT :
incertitude de jonction) =�
6 000
Cha�ne l�g�re :
( 300 x 30 ) (recombinaison V�D)� x� 4 (TdT)� x� (4 x
4) (recombinaison
D�J) =� 576 000
�� 6 000�
x� 576 000 = 3 456 . 106��� x 103 (mutation
somatique pour les r�gions hypervariables)� =� 3
456 . 109
-
ADN avant le r�arrangement (cellule non
lymphocytaire) :

Promoteur
fort�������������������������������������������������������������������������������������������� S�quence Enhancer
���������������������������������������������������������������������������������������� ������ (trop lointaine du promoteur)
-
ADN apr�s le r�arrangement g�nique (lymphocyte
B) :

���������������������������������������������������������������������� S�quence Enhancer
����������������������������������������� ������ (suffisamment proche du promoteur pour
l�activer)
Exclusion
all�lique (ou haplo�die fonctionnelle) :
Pour
devenir fonctionnels, les g�nes des immunoglobulines ne vont pas r�arranger
syst�matiquement les 2 all�les.
Cha�ne lourde :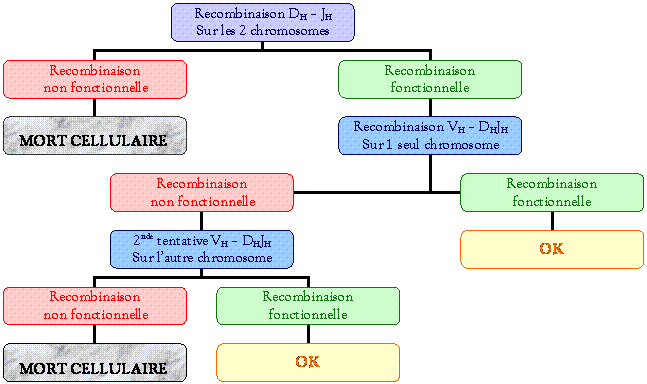

Cha�ne l�g�re :
�����������������������������������������������������������
����������������������������������������������������������
�����������������������������������������������������������������������������������������������������������������������������
Les
immunoglobulines de membrane :
La
cha�ne lourde (6000 Da) pr�sente une extr�mit� hydrophobe qui permet la
fixation � la membrane. Elle est facilit�e par la pr�sence de cyst�ines.
� "� M�canisme
de capping avec les mol�cules du cytosquelette (d�pendant de la
temp�rature)
������ = Endocytose
Toutes
les r�gions d�une immunoglobuline peuvent se comporter comme un antig�ne.
-
Isotypie :
On va retrouver des �pitotes (=
d�terminant antig�nique) de type isotypique au niveau des domaines C
(constants) et pr�sents chez tous les individus � une m�me esp�ce. Les
anticorps de type isotypique vont �tre reconnus chez tous les anticorps des
individus d�une m�me esp�ce.
-
Allotypie :
Les anticorps qui appartiennent �
cette famille correspondent � des anticorps qui ont des variations all�liques
au niveau des domaines C.
Le 1er exemple a �t�
d�crit par Oudin : � L�allotypie est la propri�t� observ�e sur
certaines prot�ines animales de poss�der, chez certains groupes d�individus
d�une m�me esp�ce, des sp�cificit�s antig�niques transmises de fa�on
h�r�ditaire.
-
Idiotypie :
Elle est port�e par la r�gion
variable de l�anticorps. Chaque anticorps va pouvoir se comporter de fa�on
diff�rente. Il n�y a pas de r�gle.

�������������������������������������������������������
Le
r�arrangement des immunoglobulines est un processus ordonn� et r�gul�.
� Ca passe
ou �a casse �
Il
y a peu d��lues, d�o� la pr�sence de monocytes et macrophages pour �liminer la
casse.
NB :
Il existe une sous�population de lymphocytes B qui
pr�sente de marqueur de surface CD5. Les cellules CD5+ ne sont pas
capables de synth�tiser beaucoup d�immunoglobulines. Celles synth�tis�es sont
de faible affinit�, mais elles reconnaissent des antig�nes un peu
particulier : autog�nes (origine de pathologies auto�immunes) et les
antig�nes de nature polysaccharidique.
Ces cellules CD5+ sont aussi
appel�es cellules T�ind�pendantes, c�est���dire ind�pendantes des cytokines
s�cr�t�es par les lymphocytes T.
Leur
r�le est un peu flou (� cause des difficult�s d��tude) Elles sont associ�es �
des tumeurs : LLC (= leuc�mie lymphocytaire chronique)
Dans l��volution, il n�y a pas de changement des
structures, mais plut�t l�ajout de nouvelles structures venant compl�ter les
structures d�j� existantes :
-
Le
malt (en premier),
-
Le
thymus,
-
La
moelle osseuse,
-
Les
organes lympho�des IIAIRES.
+��� Le
r�arrangement d�un g�ne ancestral
Le g�ne V peut �tre rendu diverse par la pr�sence de
pseudog�ne. Le pseudog�ne a la structure d�un g�ne mais pas la fonction :
il n�est pas exprim�.
Il permet une
modification de la structure, de s�quence, donc une possible modification de la
r�gion V et augmenter sa diversit�.
-
Chez
la souris, les antig�nes peuvent �tre polysaccharidiques.
-
Chez
les poissons, la cellule doit s�adapter � des temp�ratures basses (par
exemple : la pr�sence d�acides gras dans la membrane des lymphocytes B)
-
Chez
le x�nope, la diff�renciation des lymphocytes B s�arr�te pendant la
m�tamorphose puis reprend apr�s.
La lign�e T poss�de un r�cepteur
sp�cifique � un antig�ne, mais � besoin d�une cellule pr�sentatrice d�antig�ne
(CPA)
Le syst�me immun
d�veloppe un r�pertoire de lymphocytes T (grande diversit�)
Le TCR est un r�cepteur de nature prot�ique
(peptidique) compos� de 2 cha�nes : une cha�ne a et une cha�ne b.
Une autre forme
existe avec une cha�ne g et une cha�ne d (plus chez le mouton ou le
poulet)
L�utilisation de d�tergents montre
l�existence des cha�nes a et b, mais aussi de
5 autres cha�nes polypeptidiques invariantes qui forment un complexe autour du
TCR proprement dit.
Il
s�agit des 5 cha�nes du CD3 (g, d, e, z et h) Les cha�nes g, d
et e proviennent de 3 g�nes
diff�rents mais pr�sentent une forte homologie de s�quence : la r�p�tition
du motif ARAM (ou ITAM)
Le motif ITAM est la s�quence intra�cytoplasmique
Y�X�X�L (= Tyrosine�quelconque�quelconque�Leucine) La s�quence consensus est
Y�L�Y�L.
Il permet
l�activation du lymphocyte T quand ce dernier reconna�t un antig�ne en
d�clenchant la synth�se de cytokines.
Le CD4 :
-
C�est
une glycoprot�ine avec 4 domaines cytoplasmiques pr�sente chez les LT immatures
et les ’ des LT circulants (= matures)
-
Elle
est tr�s sp�cifique des LT.
-
Son
domaine N�terminal contient des r�gions qui reconnaissent les mol�cules du CMH
de classe II.
-
C�est
aussi le site de fixation de
Le CD8 :
-
C�est
une glycoprot�ine compos�e de 2 cha�nes a et b (diff�rentes des cha�nes a et b cit�es
ci�dessus) organis�es soit en a�a, soit en
a�b, soit enb�b.
-
Elle
est pr�sente sur € des LT.
-
Elle
a besoin du CMH de classe I.
-
Sa
r�gion intra�cytoplasmique est riche en tyrosine, permettant la fixation de
kinase.
Les g�nes codant
pour les cha�nes a, b, g et d :
-
La
cha�ne a :�� Sur le chr 14 q11
"� Combinaison des g�nes V, J et C
-
Va � 40
-
Ja � 50
-
Ca = 1
-
La
cha�ne d :�� Sur le chr 14 q11
"� Combinaison des g�nes V, D, J et C
-
Vd = 8
-
Dd = 3
-
Jd = 4
-
Cd = 1
-
La
cha�ne g :�� Sur le chr 7 q15
"� Combinaison des g�nes V, J et C
-
Vg = 8
-
Jg = 5
-
Cg = 1 (voire
2, maintenant)
-
La
cha�ne b :�� Sur le chr 7 q35
"� Combinaison des g�nes V, D, J et C
-
Vb � 50
-
Db = 2
-
Jb = 14
-
Cb = 2
�� 1015
TCR diff�rents dans le r�pertoire th�orique.
La
pr�sence de 3 g�nes permet une seule recombinaison, alors que la pr�sente de 4
g�nes permet 2 recombinaisons.
![]()
Les recombinaisons sont sous le contr�le :
-
Des
s�quences hepta�nonam�res (= SSR),
-
De
la recombinase,
-
Des
prot�ines RAG1 et RAG2,
-
De
+��� La d�l�tion ou l�inversion � la place de la
mutation somatique pour les LB.
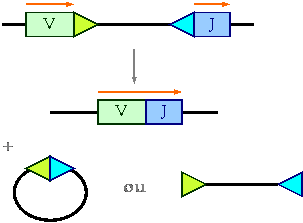 D�l�tion :
D�l�tion :
G�nes :
m�me orientation
������ Signaux de recombinaison :
orientation invers�e
 Inversion :
Inversion :
G�nes :
orientation invers�e
������ Signaux de recombinaison : m�me
orientation
Les lymphocytes ont des propri�t�s plut�t
h�t�rog�nes :
-
Fonction
r�gulatrice :
Lymphocyte
T appel� TH (helper = auxiliaire)� "�� CD4+
Lymphocyte
T appel� TS (suppresseur)� "�� CD8+
-
Fonction �
m�diation cellulaire :
Lymphocyte
T s�cr�teur de cytokines� "�� CD4+
Lymphocyte T appel� TC
(cytotoxique)� "�� CD8+
Mais
on parle surtout des lymphocytes TH et des
lymphocytes TC (en terme d�utilit�)
La
coop�ration entre les lymphocytes T et B se fait avec les lymphocytes TCD4.
La
proportion en lymphocytes T est de 60% TCD4 et 40% TCD8.
v Fonction des lymphocytes
CD4+ :
Les lymphocytes TH constituent la
population majeure des TCD4 et sont
subdivis�s en 2 sous�populations TH1 et TH2.
En
g�n�ral, les travaux sur les clones TH posent plus de
probl�mes chez l�homme que chez la souris.
-
Les
TH1 sont sensibles aux antig�nes de
grande taille et une forte irradiation des CPA.
-
Les
TH2 sont sensibles aux antig�nes de
petite taille et une faible irradiation des CPA.
L�interleukine
3 (IL�3) intervient dans l�endog�nie des lymphocytes B.
-
Hypersensibilit�
de type I�� "� Allergie (avec les IgE)
-
Hypersensibilit�
de type II
-
Hypersensibilit�
de type III
-
Hypersensibilit�
de type IV�� "� Hypersensibilit� retard�e (avec les LTH1)
Les
LTH2 ont un effet sur la lign�e des
LB.
Les
LTHP = pr�curseurs ; l�INFg = interf�ron g
-
Le
macrophage s�cr�te de l�interleukine 12 pour activer le LTH1.
-
Le
macrophage s�cr�te de l�interleukine 10 pour inhiber le LTH1.
A
conna�tre sur le bout des doigts�
Mise en �vidence
du r�le des LTH1 :
-
Injection
de toxoplasme (= parasite) dans l�organisme :
"� R�ponse non
sp�cifique

Le
parasite n�est pas d�truit, mais stabilis� dans le macrophage (absence de
r�plication)
Si
on �limine l�interf�ron g, la r�plication
reprend.
Mise en �vidence
du r�le des LTH2 :
-
Injection
d�helminthe (Nippostrongylus brasiliensis) :
"� Cytotoxicit�
cellulaire d�pendante de l�anticorps
������ ���
= Cyotoxicit� � m�diation cellulaire

La
pr�sence de LTH2 aide les
lymphocytes B � synth�tiser des anticorps.
v Les cytokines (LTCD4) :
La
r�ponse immune n�cessite des interactions cellule�cellule, soit en direct, soit
par un message d�livr� par des m�diateurs solubles (hormones et/ou
cytokines)
Les
cytokines (ou IL) sont s�cr�t�es de fa�on transitoire (uniquement par des
cellules pr�alablement activ�es)
Les
hormones sont s�cr�t�es de mani�re continue (influence uniquement par la
concentration)
Il
existe d�autres cellules (ext�rieures au syst�me h�matopo��tique) qui
synth�tisent des cytokines : les cellules de l�endoth�lium vasculaire, les
fibroblastes, les ent�rocytes�
Les cytokines n�ont qu�un seul moyen
d�agir : par le biais d�un r�cepteur. Il existe donc une r�gulation
subtile par une �quation ligand�r�cepteur.
Elles peuvent
intervenir en cascade : induction des unes par les autres.
Elles peuvent �tre class�es en 3 grands
groupes :
-
Les
cytokines impliqu�es dans l�h�matopo��se : IL�5, 7 et 3,
-
Les
cytokines impliqu�es dans l�immunit� sp�cifique :
-
Synth�se
de TH1 (immunit� � m�diation) : IL�2
et INFg,
-
Synth�se
de TH2 (coop�ration avec les LB) :
IL�4, 5, 6 et 10,
-
Les
cytokines impliqu�es dans la r�action anti�inflammatoire : INFg, IL�1 et toute la famille de TNF
(surtout les TNF a et b)
� M�canisme
d�amplification de la r�ponse immune :
Les
cytokines sont des mol�cules m�diateurs peptidiques (~ 15000 Da) qui
peuvent �tre glycosyl�es ou non. Mais cette glycosylation ne semble pas
n�cessaire, notamment avec les cytokines recombinantes (= fabriqu�es dans des
bact�ries) qui ne sont donc pas glycosyl�es et qui restent fonctionnelles.
Les cytokines peuvent aussi �tre
class�es en :
-
Cytokines
� faible rayon d�action,
-
Cytokines
� action � distance.
Les cytokines �
faible rayon d�action :
-
Elles
sont capables d��tre synth�tis�es par un type de cellules voisines
=� Situation
� paracrine �
-
Elles
sont capables d��tre synth�tis�es par le m�me type de cellules
=� Situation
� autocrine �
-
Elles
sont capables d��tre synth�tis�es � longue distance
=� Situation � exocrine �
j Activit�s pl�iotropes :
Selon
le tissu cible, l�effet est diff�rent. Il n�y a pas que le tissu
h�matopoi�tique, mais aussi le syst�me nerveux, les cellules r�nales, etc.)
Exemple :
TNF� "� Synth�se d�IL�1� "� IL�6 dans les fibrocytes� "� IL�8� "� Action sur les leucocytes
k Activit�s physiologiques :
Les
cytokines agissent � des concentrations faibles, m�me tr�s faibles (de l�ordre
de la picomole, voire la nanomole)
On
peut augmenter la concentration en cytokines d�un facteur de 1, 2, voire 3.log,
mais cela provoque une action diff�rente. Les cytokines n�ont plus les m�mes
fonctions (peut �tre utilis� comme traitement)
Exemple :
L�augmentation
de l�IL�12 entra�ne un trouble des fibres musculaires dans les muscles lisses,
notamment un probl�me cardiaque.
l Activit�s redondantes :
Les
cytokines ont une activit� pouvant se compenser les unes aux autres.
Exemple :
Un
animal d�ficient en IL�2 (qui permet la mise en place des LT et LB) ne meurt
pas et vit m�me normalement.
On observe la
pr�sence de r�cepteurs � IL�6 permettant de palier le manque en IL�2.
� Nomenclature :
Les
cytokines sont aussi appel�es interleukine (IL) mais leur nom ne permet pas de
pr�dire l�activit� de telle ou telle cytokine.
L�interf�ron
g est une cytokine. Les
interf�rons a
et
b sont des antiviraux.
Il
y a souvent des cellules pr�curseurs (exemple : IL�12) L�IL�12 est un
peptide h�t�rodim�re. La cha�ne de l�interleukine pr�curseur est plus longue
que la forme mature.
On conna�t les
g�nes et leurs effets.
Les
cytokines ne fonctionnent que par l�interm�diaire de leur r�cepteur. Ceux�ci
sont tr�s variables. Ils sont plut�t des dim�res et il y a l�absence de
sp�cificit� compl�te. Il existe plusieurs cat�gories de r�cepteurs selon le
type cellulaire.
Exemple : Le r�cepteur �
IL�2 = CD25

���������������������������������������������������������
Il
y a un effet�dose des cytokines :

����������������������������������������� Cytokine
(en fonction de la quantit�)
����������������������������������������������������� Apoptose
(mort cellulaire)
Diff�renciation,
Prolif�ration��������������������� Anergie
(Evolution
clonale)
v Cytotoxicit� des LTCD8 :
Exemples :
-
Le
rejet de greffe ou une pathologie consiste en la destruction des cellules du
m�me organisme.
-
La
destruction d�agents infectieux, virus, bact�ries.
La
cytotoxicit� est r�duite � un type de cellules qui proviennent du HLA de classe
I. Elle s�effectue en 3 phases : la reconnaissance, l�action puis la
d�sint�gration des cellules cibles.
-
La
reconnaissance a besoin de cations (Mg2+) et elle est
plut�t courte. Elle est aussi appel�e le baiser
de la mort.
-
L�action
est sensible au Ca2+ et elle est
tr�s rapide. On parle aussi de coup
mortel.
-
La
d�sint�gration n�a besoin de rien, mais sa dur�e est variable.
Les
LT cytotoxiques peuvent tuer plusieurs cellules les unes apr�s les autes.
La cytotoxicit�
indirecte (ou lyse indirecte) :
C�est
la mise en place du programme de mort cellulaire (apoptose)
Elle
est qualifi�e d�indirecte car elle a besoin d�une interaction
ligand�r�cepteur :
 TNF�TNFr� =� FAS�FASl� =�
CD95�CD95l
TNF�TNFr� =� FAS�FASl� =�
CD95�CD95l
����������������������������������������������������� Activation de prot�ines adaptrices
����������������������������������������������������� IL�b�Converting�Enzyme
(= ICE)
������������������������������ �� Apoptose
La cytotoxicit�
directe (ou lyse directe) :
Il s�agit plut�t d�un ph�nom�ne de
n�crose. Il y a l�exocytose de granules contenant des enzymes de diff�rentes
cat�gories :
-
Des
s�rine�est�rases : granzine A et granzine B.
Les g�nes codant pour les
s�rines�est�rases sont sur le chr 14,
proches
des g�nes codant pour le TCR et des autres Ig.
-
Des
perforines qui ont une forte homologie avec le compl�ment (surtout la prot�ine
C9 du compl�ment)

Quelques
exemples de cytotoxicit� :
Cytotoxicit�
d�pendante � l�anticorps (ADCC) :

Cela
marche aussi avec des lectines � la place des anticorps.

Lymphotoxicit�
:
Rejet
de greffe dit aigu :
La
cellule cible est le greffon. Les cellules impliqu�es dans la destruction sont
les cellules NK. Elles ressemblent aux TL par la pr�sence du CD�34 et par leur
sensibilit� � l�IL�15, mais en sont diff�rentes par l�absence de TCR (=
r�cepteur sp�cifique � l�antig�ne)
Les
cellules NK sont impliqu�es dans la r�ponse immune exog�ne (contre les virus),
dans la r�ponse immune endog�ne (lyse directe des cellules tumorales) ou encore
dans la synth�se de certaines cytokines et la stimulation des LTH.
Elles
pr�sentent d�autres cat�gories de r�cepteurs que les r�cepteurs sp�cifiques �
l�antig�ne. Certaines sont sensibles aux HLA de classe I, d�autres non.
Les cellules NKT :
Elles
ont des propri�t�s communes entre les LTCD8 et les cellules
NK. Elles participent au rejet des cellules tumorales et sont associ�es aux
pathologies comme les maladies autoimmunes.
Ind�pendante du thymus Ind�pendance
au CMH Cytotoxicit�* NK NKT Sous le contr�le (restriction) du CD�1 + Sensibilit� au IL�4 Restriction par rapport aux HLA de classe I. LTCD8 * : responsable de la s�cr�tion d�au moins un type de
cytokine : l�INFg

Les
plus connus : HLA, H2
Il
se caract�rise par des prot�ines de surfaces tr�s diff�rentes. Ce sont ces
mol�cules qui sont impliqu�es dans le rejet de greffe. Il a pour fonction
essentielle la pr�sentation de l�antig�ne aux lymphocytes T.
Le
CMH est pr�sent chez tous les animaux. Il a �t� mis en �vidence chez l�homme en
1958 par l�utilisation d�anticorps. Le HLA (human
leucocytes antigens = CMH) sont pr�sents sur tous les leucocytes.
Ce syst�me
pr�sente une grande diversit� par polymorphisme.
D Polymorphisme � R�arrangements
L�ADN est polymorphe, c�est���dire qu�un
g�ne s�exprime sous diff�rentes formes all�liques.
Ce
syst�me HLA est dit multig�nique, multi�all�lique et co�dominant. Il existe 200
g�nes qui peuvent appartenir au HLA (dont 49 avec une sp�cificit� de
pr�sentation de l�antig�ne)

Un haplotype est un ensemble d�all�les
transmis d�un individu � un autre enfant. Cela peut �tre a�c, a�d, b�c et b�d.
"� Cela permet une �norme diversit�.
On
a constitu� un patrimoine g�n�tique pour le HLA et on peut coder 1013 prot�ines
diff�rentes pour le HLA.
v Description
des g�nes :
Ils occupent une vaste r�gion de notre
g�nome : 2000 � 4000 kb (soit 1/1000 du g�nome total) Les g�nes sont
situ�s dur le chromosome 6p (bras court)
Il existe 3
cat�gories de g�nes :

Classe I :���� une cinquantaine de g�nes
Classe II :�� une quinzaine de g�nes
� Classe
I :
Les g�nes se situent plut�t dans la r�gion t�lom�rique.
Ils sont divis�s en plusieurs sous�classes : A, B, C, etc.
De nombreux
g�nes sont des pseudog�nes. Ces g�nes vont coder pour des prot�ines exprim�es �
la surface de toutes les cellules nucl��es. Ils vont coder pour une prot�ine
HLA classe I.
Cette prot�ine est compos�e de 2
cha�nes :
-
Une
cha�ne lourde polymorphe (a1, a2, a3) synth�tis�e
par un g�ne HLA classe I.
Elle
pr�sente un domaine avec une forte homologie de s�quences.
PM = 43 kDa.
-
Une
cha�ne l�g�re (b2_microglobuline)
synth�tis�e par un g�ne qui se situe sur le chromosome 15 (il n�appartient aux
g�nes du HLA)
Il
peut �tre reli� ou non � la prot�ine de classe I.
Sa
structure est bien connue.
Il
y a la pr�sence de 8 exons :

La
r�gion transmembranaire est riche en acides amin�s hydrophobes. Elle pr�sente
des sites de fixation pour la tyrosine, permettant ainsi des interactions avec
des kinases et des mol�cules du cytosquelette.
Les s�quences a1 et a2 sont les
r�gions les plus externes : elles pr�sentent les plus forts taux de
polymorphisme pour pr�senter le peptide antig�nique. Elles vont former une
cavit� vide o� le peptide peut venir se nicher (place maxi de 9 acides amin�s)
C�est
une r�gion de +/� forte affinit� pour le peptide antig�nique.
� Classe
II :
Il existe 2 types de g�nes regroup�s
sous une organisation particuli�re. Il y a une association des g�nes de type D
(DP, DN, DM, DO, DQ, DR)
Ces
g�nes vont coder pour une prot�ine HLA classe II qui est compos�e de 2 types de
cha�nes :
-
Une
cha�ne a
(33 kDa) compos�e de 2 sous�unit�s a1 et d�une
sous�unit� a2,
-
Une
cha�ne b
(29 kDa) compos�e de 2 sous�unit�s b1 et d�une
sous�unit� b2.
 Les sous�unit�s a1 et b1 sont souvent
les plus externes : elles fabriquent sp�cialement la cavit� o� le peptide
pourra se nicher pour �tre pr�sent� aux LT4.
Les sous�unit�s a1 et b1 sont souvent
les plus externes : elles fabriquent sp�cialement la cavit� o� le peptide
pourra se nicher pour �tre pr�sent� aux LT4.
" Types
s�rologiques
![]()
![]()
Les g�nes de
type DR de classe II :
Il
existe plusieurs cat�gories de g�nes qui codent la cha�ne a. La cha�ne b est toujours
cod�e par le m�me type de g�nes.

Les
g�nes TAP vont coder pour les prot�ines de transports (� fonction enzymatique)
� Classe
III :
Ce
sont des g�nes situ�s dans la r�gion HLA mais on ne sait pas � quoi ils
correspondent. Ils vont coder pour des prot�ines de compl�ments pour les TNF a et b, et pour l�Hsp
70.
v Distribution
des mol�cules HLA de classe I et de classe II :
Les HLA de
classe I :
Elles
sont situ�es � la surface de toutes les cellules nucl��es de l�organisme. Elles
sont exprim�es par les lymphocytes, les macrophage, h�patocytes, �rythrocytes, SNC,
pancr�as, glande salivaire, endoth�lium de la corn�e, etc.
Les HLA de
classe II :
Leur distribution est plus
restreinte : elles sont pr�sentes que sur certaines cellules qui ont pour
fonction de pr�senter l�antig�ne (CPA)
Les CPA les plus
connues sont les cellules dendritiques, les macrophages, les lymphocytes B
activ�s, les ent�rocytes, les cellules �pith�liales des voies respiratoires.
Les cellules dendritiques sont des cellules cutan�es
pr�sentant de longs prolongements. Ce sont des cellules qui ont un pr�curseur
m�dullaire qui pr�sente le marqueur CD43.
Elles
appartiennent � un groupe h�t�rog�ne de cellules tissulaires qui participent �
la circulation lymphocytaire. Elles sont diff�renci�es selon la zone o� elles
se situent :
-
Les
cellules de Langerhans,
-
Les
cellules dendritiques du derme.
Les cellules de Langerhans sont d�crites
en 1968. Elles sont plus faciles d�acc�s : elles se trouvent au niveau des
cellules basales de l��piderme.
Elles pr�sentent
un noyau polylob� et des granules (= granules de Birbeck) Elles expriment des
prot�ines HLA de classe II, des mol�cules d�adh�rence (int�grines), des
r�cepteurs aux cytokines et d�autres marqueurs (CD1A)
Les cellules dendritiques expriment
aussi le marqueur CD1A. Elles se diff�rencient par l�absence de granules de
Birbeck.
Elles quittent
la peau pour migrer vers les organes lymphocytaires et stimuler les cellules T
na�ves. Elles expriment � la surface des mol�cules d�adh�rence et sont des
pr�curseurs CD34.
Les
monocytes et macrophages peuvent apparemment �voluer en cellules dendritiques
v Pr�sentation
de l�antig�ne par les prot�ines HLA de classe I :

j Pr�sentation du
peptide antig�nique par des enzymes prot�olytiques (= prot�osome) qui le
transforme en petits fragments
k Franchissement
de la membrane plasmique par un transport actif (hydrolyse d�ATP) Le peptide
est transport� par TAP1 et TAP2.
l Le peptide
antig�nique va se nicher dans une petite activit� cr��e par a1 et a2 (dans le RE)
m Entr�e dans une
v�sicule de golgi de la prot�ine HLA de classe I accompagn�e du peptide
antig�nique et de calnexine.
n Exocytose. Le
peptide est pr�t � �tre reconnu par un lymphocyte TCD8+.
v Pr�sentation
de l�antig�ne par les prot�ines HLA de classe I :
j Endocytose et
formation d�un endosome, permettant la coupure en petits fragments par les
prot�ases.
k Dans le RE,
mise en place d�une cha�ne invariante qui prot�ge l�ensemble prot�ique.
l Dans l�appareil
de Golgi, terminaison de la maturation.
m Fusion des
membranes qui permet la rencontre de la prot�ine HLA de classe II et du peptide
antig�nique. La cha�ne invariante est cliv�e et, en g�n�ral, elle est ensuite
d�grad�e ou recycl�e.
n Pr�sentation au
lymphocyte TCD4+.
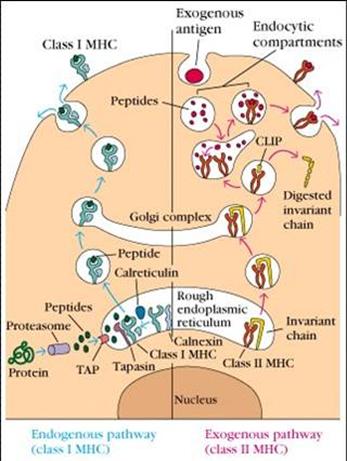
Le
syst�me CD1 permet la pr�sentation pour les mol�cules lipidiques aux
lymphocytes T. Il existe un locus CD1 o� il y a 5 g�nes (CD1�A, CD1�B, CD1�C,
CD1�D, CD1�E)
C�est un syst�me
multig�nique, mais il n�est pas polymorphe.
Le syst�me est +/� bien d�finit chez
toutes les esp�ces de mammif�res.
La
prot�ine CD1 (45 kDa) est compos�e d�une cha�ne lourde glycosyl�e, elle�m�me
compos�e de 3 sous�unit�s (a1, a2, a3) Elle ressemble
aux HLA de classe I avec une mol�cule de b_2M qui peut
�tre associ�e de fa�on non covalente.
Il devrait y
avoir un g�ne ancestral qui s�est adapt� et a �volu� en HLA de classe I et HLA
de classe II.

2 grands
groupes :
-
Groupe 1 : Les prot�ines
sont cod�es par les g�nes CD1�A, CD1�B, CD1�C. Elles sont localis�es sur les
thymocytes immature. On les retrouve sur les cellules de Langerhans, les
monocytes et les lymphocytes activ�s.
-
Groupe 2 : Les prot�ines
sont cod�es par le g�ne CD1�D. On les retrouve sur les lymphocytes T, les
cellules dendritiques mais surtout sur les h�patocytes et l��pith�lium
intestin.
La
cavit� form�e par les sous�unit�s a1 et a2 est hydrophobe
et permet donc la fixation des mol�cules lipidiques.
Une sous�unit� population de LT va �tre
sensible par la pr�sentation d�antig�ne par les CD1. Il y a la formation
d�auto�antig�ne.
Le
CD1 peut avoir un r�le � jouer dans le m�canisme anti�infectieux et la fonction
anti�tumorale. Il a aussi un r�le dans des pathologies. Il permet de contr�ler
un environnement tissulaire correct (hom�ostasie)
" Immunit� classique et inn�e.
� Identification
des diff�rents types s�rologiques de HLA :
j Diff�renciation � de s�rologie :
Le
HLA se comporte comme une prot�ine de surface entra�nant une r�action de
lymphotoxicit� car le compl�ment peut venir se fixer sur le Fc, l�Ig et
provoquer la lyse de la cellule cible.
k M�thode biochimique
l M�thodes de biologie cellulaire :
Culture mixte lymphocytaire (CML) : 2
populations en culture pour d�finir :
-
Une
population stimulante " irradiation
pour les supprimer,
-
Une
population reperdant (cytokines, cytotoxicit�)
" Compatibilit�
m M�thodes de biologie mol�culaire :
Utilisation de sondes de g�nes HLA.
Technique : RFLPs, microsatellites.
" On trouve
diff�rents types HLA (par exemple : lors d�un rejet de greffe)
Les
HLA sont souvent associ�s � de nombreuses pathologies.
Exemple :
-
Le
HLA B27 est fortement associ� � l�inflammation chronique des microsquelettes
(arthrite) Il existe une distribution de cette population qui augmente des
exemples qui pr�sentent de l�arthrite.
-
Les
HLA de classe II sont associ�s � des pathologies auto�immunes comme la
myasth�nie ou le diab�te (plurifactoriel dont l�environnement) de type I
insulinod�pendant :
L�HLA
de classe II : le g�ne DQ donne la s�quence prot�ique, l�aspartate en
position 57 permet la r�sistance au diab�te. Si c�est un autre acide amin�, le
risque de d�velopper le diab�te de type I est plus important.
Le
destin d�une greffe va d�pendre des diff�rentes de compatibilit� entre donneur
et receveur.
v Greffes :
� Quelques
d�finitions :
-
Autogreffe : Le donneur est
le receveur.
-
Isogreffe : C�est une
greffe synergique. Le donneur et le receveur sont g�n�tiquement identiques (=
vrais jumeaux)
-
Allogreffe : Le donneur et
le receveur sont diff�rents mais appartiennent � la m�me esp�ce.
-
X�nogreffe : Le donneur et
le receveur appartiennent � 2 esp�ces diff�rentes.
-
Greffe : Il s�agit de
toute transportation de cellules ou tissus. Il n�y a pas d�anastomose
vasculaire. C�est diff�rent de la transplantation.
Le
m�canisme de rejet de greffe est une r�ponse immunitaire des lymphocytes du
receveur contre les antig�nes du donneur.
� 3
cat�gories :
-
Rejet aigu� : Il est caract�ris�
par le moment de l�apparition du rejet (8 � 15 jours)
-
Rejet suraigu� : Il s�agit de
rejets plus rapides (quelques heures � quelques minutes)
-
Rejet chronique
-
GVH (Graft Vernes Host) : Il s�agit de la
r�action du greffon contre l�autre. Le r�cepteur ne peut pas rejeter le
greffon.
S�il y a des
lymphocytes T dans le greffon, ceux�ci peuvent r�agir contre le receveur en
cr�ant une r�ponse immune pathologique du greffon contre l�autre.
-
Autogreffe : Il n�y a pas de
rejet (exemple de la moelle osseuse)
-
Isogreffe : Il n�y a pas de
rejet.
-
Allogreffe : Il peut y avoir
des rejets aigus. Les lymphocytes du receveur (surtout CD8+) sont
responsables de la r�ponse immune cytotoxique. Les cellules tueuses sont donc
activ�es.
Quand il y a un
nombre suffisant de LTCD8+, il faut
plusieurs jours pour la destruction du greffon.
-
X�nogreffe : Il peut y avoir
des rejets suraigus. Les anticorps pr�form�s du receveur vont se fixer sur
l�antig�ne du greffon. Une fixation compl�te entra�ne la lyse du greffon.
� Les
lymphocytes :
Les
lymphocytes TCD4+ :
Ils
peuvent �tre �ventuellement impliqu�s dans le rejet. Ils sont allor�actifs. Ils
s�cr�tent aussi du TNF, l�interf�ron g et l�IL�6
entra�nant un processus de destruction.
Les
lymphocytes TCD8+ :
Ils
entra�nent la cytotoxicit� directe ou indirecte, causant la lyse cellulaire du
greffon.
Les
lymphocytes B :
Des allo�anticorps pr�existants chez le
receveur entra�nent l��limination directe par la fixation du compl�ment sur les
cellules du greffon. Cela cause les rejets chroniques.
Il y a
l�alt�ration au niveau des vaisseaux.
Le rejet se fait en 2 phases :
-
La
sensibilisation,
-
La
migration des lymphocytes sensibilis�s.
La
sensibilit� consiste en la d�fense des cellules dendritiques qui pr�sentent les
antig�nes. La migration se fait du donneur vers le receveur.
Il
existe diff�rents traitements utilis�s en cas de rejet ou d�exp�rimentation.
Pour pr�venir un rejet de greffe, on effectue une immunosuppression soit
sp�cifique, soit non sp�cifique.
Immunosuppression
sp�cifique :
On utilise des agents alkylants,
inhibiteurs du m�tabolisme des purines et pyrimidines (azathioprine et
m�thotrexate) Ces m�dicaments sont associ�s � des cortico�des.
-
L�azathioprine
limite le d�veloppement des LT et la prolif�ration des cellules tueuses de type
NK.
-
La
m�thotrexate bloque la division cellulaire. Elle pr�sente des effets
secondaires.
La
famille des cyclosporines (d�origine fongique) va agir exclusivement des
lymphocytes activ�s et surtout les LTCD4+. Il n�y a pas
d�effet toxique sur l�h�matopo��se. Il y a moins d�effets secondaires mais il y
a une toxicit� au niveau des reins.
On
peut effectuer une irradiation (= immunosuppression) par l�application de
rayons UV (sur les cellules de la peau, les cellules dendritiques et les
cellules de Langerhans), ou de rayons X et g (entra�nant une
irradiation totale)
L�immunosuppression
est utilis�e avant la greffe (de moelle osseuse, par exemple)
Immunosuppression
non sp�cifique :
Les cellules de Langerhans ont un r�le
important � jouer dans la pr�sentation des antig�nes du greffon. Les cellules
dendritiques sont trait�es avec des anticorps anti�cellule dendritique, puis on
r�injecte ces cellules dendritiques.
Cela permet une
diminution de la probabilit� de rejet de greffe.
Il
faut augmenter de tol�rance des populations lymphocytaires par rapport aux
antig�nes du greffon.
Le thymus a un r�le important dans ce
d�veloppement. Il peut �tre � l�origine de plusieurs pathologies comme le
syndrome de Di George.
Pendant la 1�re
ann�e de la vie, le thymus involue mais reste fonctionnel. Il s�agit d�une
r�duction quantitative mais pas qualitative.
Il
pr�sent un r�le important dans la mise en place du TCR et des marqueurs CD.

Mais c�est plus
compliqu� L
Les
cellules pr�curseurs arrivent par la m�dulla et migrent dans le cortex. C�est
une cellule dite � double n�gative �, c�est���dire CD4� et CD8� (DN)
Maintenant, on
peut parler de cellules triples n�gatives (TN) : CD4�, CD8� et CD3�.
Au niveau du cortex, la cellule DN
devient DP (CD4+ et CD8+) et doit
maintenant faire son choix entre le CD4� et le CD8�. Il est rare
qu�un lymphocyte T mature reste DP.
Il
y a alors une s�lection : seuls 5% des cellules arrivent � terme (soit 95%
de perte cellulaire)
Il y a l�existence
de cellules stromales qui synth�tisent des facteurs de croissance.
Les cellules souches pr�sentent initialement des
marqueurs (CD44, CMH de classe 1)
-
Le
passage du stade pr�curseur au stade mature n�cessite l�intervention de l�IL�2.
Il y a donc un pic d�expression du CD25 (= r�cepteur � IL�2)
-
Le
CD44 dispara�t un peu plus t�t.
-
Le
HLA de classe I, en stade cellule souche, dispara�t au stade immature et
r�appara�t au stade mature.
-
Le
CD5 appara�t un peu apr�s le CD3.
|
Thymus cortex |
Cortex |
M�dulla |
P�riph�rique |
||
|
LT
pr�coce |
Pr�T (pr�coce) |
Pr�T (tardif) |
TCR Double positif |
TCRab Simple positif Immature |
TCRab SP
mature |
|
CD44+ CD117+ (C�Kit) IL�7R CD44+ |
( CD44+ ( CD44+ CD2+ |
Pr�TCR (=
b + d�but de mise
en place de a) |
CD44� CD25� CD8+ CD4+ |
CD8+/CD4� CD4+/CD8� |
|
|
|
VDJ�b =
1er arrangement (cha�ne b
du TCR) |
Cha�ne b Pr� Ja� (pTa) =
cha�ne a en cours de mise
en place (il manque notamment la r�gion
variable) =
glycoport�ine invariable |
VJ�a (intervention
des g�nes RAG) |
|
|
IL�7 D�pendance CD3 S�lection
n�gative S�lection
n�gative
![]()
![]()
![]()
|
|
|
Stade
important dans le contr�le du passage au stade suivant = S�lection positive avec association de b�pTa
qui permet ce passage |
Phases d�pendante du CMH |
-
La
pTa
a un r�le anti�apoptotique. Si elle s�exprime, elle va contr�ler l�exclusion
all�lique des cha�nes b.
-
CD3
� un r�le dans la survie cellulaire.
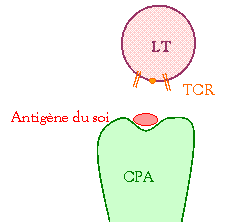 R�le du CMH :
R�le du CMH :
3
cas de figures :
�
Pas
d�affinit�
" Mort par
apoptose
‚
Faible
affinit�
" S�lection
positive (survie et diff�renciation)
ƒ
Forte
affinit� (pathologie auto�immune)
" S�lection
n�gative (mort cellulaire)
La
diversit� des peptides du soi exerce une influence sur la s�lection et la
diff�renciation des lymphocytes T.
Interaction TCR
� peptide HLA�complexe :
La r�gion hypervariable du TCR (CDR1, CDR2 et CDR3) pr�sente une
orientation transversale pour mieux reconna�tre l�antig�ne. CDR1 et CDR2 fonctionnent
ensemble.
Dans
les cellules pr�curseur, il existe un facteur notch, appartenant � une famille
de g�nes, qui va coder pour un r�cepteur membranaire (Notch 1)
Cela entra�ne la
r�gulation du choix des diff�rentes cellules :
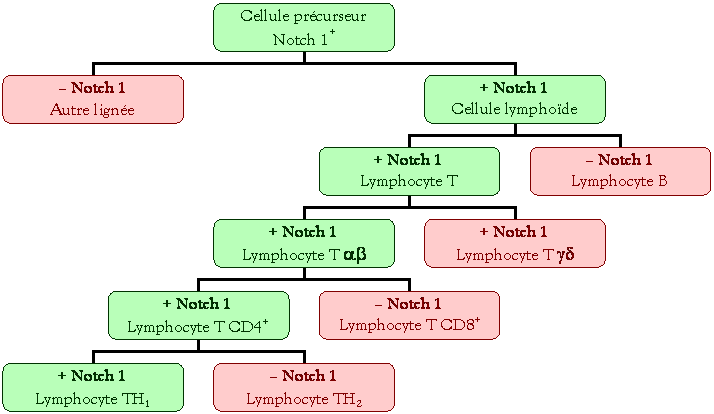
D�autres
g�nes interviennent aussi dans la s�lection (GATA, runX), ainsi que la
structure de la chromatine.
Il y a 2 concepts :
-
Il
y a la mise en place de r�cepteurs avec la constitution d�un r�pertoire,
-
L�activation
des lymphocytes n�est pas directe apr�s la rencontre entre un antig�ne et le
r�cepteur.
v M�canismes effecteurs de la
r�ponse immune :
3
cas de figures :
-
La rencontre
entre un antig�ne et les lymphocytes B et T entra�ne une r�ponse :
" Il y a survie
du lymphocyte qui permet l��volution clonale (= s�lection clonale) qui entra�ne
la prolif�ration et la diff�renciation cellulaire (2 ou 3 cycles de divisions
cellulaires)
-
La rencontre
entre un antig�ne et les lymphocytes B et T entra�ne une anergie :
" Il y n�a pas de
r�ponse, mais il n�y a pas de mort cellulaire.
-
La rencontre
entre un antig�ne et les lymphocytes B et T entra�ne la mort par apoptose.
Les
2 derniers cas sont des s�lections n�gatives permettant une tol�rance
immunitaire (en particulier contre les �l�ments du soi)
� R�pertoires :
-
Le
r�pertoire des lymphocytes B est vari� car il doit reconna�tre l�antig�ne directement.
-
Le
r�pertoire des lymphocytes Tab est plus limit�
que celui des lymphocytes B car il est aid� par le HLA.
-
Les
lymphocytes Tgd ont une
position interm�diaire entre les lymphocytes Tab.
Les
lymphocytes B ont des �tapes de prolif�ration limit�es ; les lymphocytes T
ont une prolif�ration plus forte (gr�ce � la synth�se de cytokines pouvant
activer les cycles cellulaires)
L��tape
de reconnaissance est sensible � la concentration en antig�ne.
Il
y des interactions sp�cifiques entres les cellules de la r�ponse immune. Cette
sp�cificit� est expliqu�e sur le plan g�n�tique par le m�tamorphisme et le
r�arrangement all�lique avant et apr�s la fixation de l�antig�ne.
� 3
cat�gories de r�ponse immunes :
Elles
sont d�finies selon l��tape terminale de diff�renciation et de prolif�ration
clonale : soit la r�ponse est positive, soit elle est n�gative (apoptose
ou anergie)
v Activation lymphocytaire :
Elle
passe par la caract�risation des r�cepteurs et la transduction du signal. Ce
signal peut �tre traduit sous diff�rentes modalit�s dont l�action de la
r�action enzymatique (prot�inases K) responsable d��tapes de phosphorylation
sp�cifiques.
� R�cepteurs :
Il existe diff�rents types de r�cepteurs :
-
Le
r�cepteur de type I = r�cepteur kinase,
-
Le
r�cepteur de type II = r�cepteur catalytique (coupl� � une prot�ine G),
-
Le
r�cepteur de type III = r�cepteur coupl� � une enzyme
(par
exemple la phospholipase C)
-
Le
r�cepteur de type IV = r�cepteur coupl� � un canal
(pas en immonuologie)
La
phospholipase C catalyse la d�gradation du PIP2 en IP3 et DAG. Le DAB
reste sur la membrane et stimule une prot�ine kinase (PK) L�IP3 est impliqu�
dans la stimulation de la modification de la concentration en Ca2+ intracellulaire
qui active des facteurs de transcription.
v Transduction du signal :
Le complexe TCR�CD3 reconna�t l�antig�ne (fixation
du TCR) Le CD3 pr�sente un motif consensus : YXXL. La tyrosine (Y) est le
substrat d�une prot�ine kinase.
La
fixation de l�antig�ne a pour cons�quence :
-
Une cascade
d�action qui est une cascade de kinase (autophosphorylation)
La derni�re
passe la membrane nucl�aire et active des facteurs trans (d�j� dans le noyau)
-
Une cascade des
MAP�Kinases :
La
phospholipase C fournit du DAG (= substrats de la prot�ine kinase C) et de l�IP3 entra�ne une
augmentation de la concentration interne en Ca2+ qui stimule la
calcineurine (stimulatrice d�un facteur trans qui passe la membrane nucl�aire.
Chez
les lymphocytes B, la fixation de l�antig�ne sur l�IgM (ou D) entra�ne
l�activation de la prot�ine kinase C et la phospholipase C via les m�mes
d�action au niveau de la membrane.
Les
lymphocytes T pr�sentent des prot�ines adaptarices qui font la jonction entre
l�enzyme et le substrat (GRB2, SOS, LAT, etc.)
� Sp�cificit�
aux lymphocytes :
Il y a 2 grandes cat�gories de kinases :
-
Celles
fix�es � la membrane : la famille SRC (= SARC) comme P59PLck, P59Fymn,
Yes, etc.
-
Celles
non fix�es � la membrane (ne pr�sentant pas de sites de fixation) : la
famille ZAP�70 dans la lign�e T, la famille SIC dans la lign�e B.
Le CD45 :
Il
est exprim� autour d�un r�cepteur T ou B. Il permet la r�versibilit� de la
r�ponse immunitaire gr�ce � son activit� phosphotasique.
Il existe des mol�cules de surface CD (= mol�cules
de co�stimulation) qui vont renforcer la r�ponse immunitaire (prolif�ration,
synth�se d�interleukine)
Il
y a la reconnaissance sp�cifique de l�antig�ne par TCR�CD3 (1er
signal)
Ensuite, un
second signal est cr�� par des mol�cules de co�stimulation.
v Mol�cules de co�stimulation :
� Lymphocyte
B :
Un
2nd signal est n�cessaire pour une r�ponse immune efficace. Il est
d� � la fixation de couples de mol�cules membranaires sp�cifiques entre le
lymphocyte T et
Les
lymphocytes pr�sentent :
-
Des
CD28 (= lipoprot�ines) dont le ligand est le CD80 ou le CD86 (encore appel�s
B7.0, B7.1, B7.2)
Le CD28 est exprim�
sur 100% de la membrane des LTCD4+ et 50% de la
membrane des LTCD8+.
La
fixation entra�ne une augmentation de la synth�se d�interleukine IL�2
(favorisant la prolif�ration cellulaire)
-
Des
CTLA�4 (forte homologie g�nique de s�quence avec CD28) dont les ligands sont
les CD80 et CD86, avec une affinit� plus grande pour CD86.
Il est exprim�
sur les LTCD4+ non natifs.
La
fixation entra�ne un r�le important dans les m�canismes d�allergie et de
tol�rance immunitaire.
Il existe une r�gulation, notamment par
r�trocontr�le (via des prot�ines � activit� phosphatasique)
Il existe un
travail sur l��limination des cellules tumorales en renfor�ant le signal.
� Coop�ration
T�B :
Il
y a la liaison de CD40 et CD40L.
-
CD40 :
mol�cule de surface qui appartient � la famille du TNF. Elle est exprim�e
essentiellement � la surface des CPA et lymphocytes B. Les lymphocytes B
activ�s peuvent jouer le r�le de CPA.
Elle
a un r�le dans la synth�se d�IL�4 (= cytokine dans la commutation de place des
Ig ou switch)
-
CD40L :
mol�cule appartenant � la famille des TNF. Elle est exprim�e surtout � la
surface. Lors de l�activation de LT CD4+, il y a la
synth�se de CD40L par la fixation de
S�il
y a un blocage de l�interaction CD40�CD40L, il y a une absence de r�ponse
positive (apoptose ou anergie)
v Voie de signalisation
JAK�STAT :
La
coop�ration B�T correspond � la mise en place d�un 1er signal, d�un
2�me signal et � la synth�se de cytokine.
Le
syst�me JAK�STAT (Janus Kinase � Signal Transducer and Activator of
Transcription) est beaucoup plus rapide et plus simple de la voie MAP Kinase.
-
La
famille de kinase de type JAK (JAK1, 2, 3 et Tyk2) poss�de 2 domaines kinases,
mais aucun domaine SH2 ou CH3.
-
Les
prot�ines de type STAT (STAT1, 2, 3, 4, 5A, 5B et 6) poss�de un domaine SH2 (= site de
tyrosine kinase) et un domaine de liaison � l�ADN.
Les STAT sont cytoplasmiques. Les prot�ines JAK sont
associ�es de mani�re constitutive au r�cepteur (ex. : r�cepteur � INFg) et provoquent une
autophosphorylation du r�cepteur, entra�nant la fixation de 2 STAT. Cela permet
dim�risation des 2 STAT, via leur phosphorylation. Le dim�re active la
transcription.
Il existe un
r�trocontr�le par des mol�cules fixant les STAT.
L�avantage
est sa rapidit� (absence de cascade et mol�cules adaptatives) L�observation de
cette voie a �t� possible par la mise en place de mod�les animaux d�ficients.
Il renforce la r�ponse immune et d�pend des
immunoglobulines. Il participe � l��limination par phagocytose. Il est compos�
d�un ensemble de prot�ines que l�on peut retrouver sous 2 formes (forme soluble
5% et forme membranaire 95%)
Il
compl�mente la r�ponse immune (r�ponse Ag�Ac) par la mise en place de r�actions
en cascade. Il a un r�le dans le processus inflammatoire, en augmentant la
perm�abilit� vasculaire par chimiotactisme. Il a aussi un r�le dans le
processus dans la phagocytose en stimulant le m�canisme d�opsonisation.
Il est capable
de lyser les cellules cibles par le biais de r�actions phagocytaires. Il est utilis�
� la neutralisation certains virus. Il participe � l��limination du complexe
immun (complexe Ag�Ac)
v Nomenclature :
Il
y a 11 composants : C1q, C1r, C1s, C2, C3, C4, C5, C6, C7, C8 et C9. Leur
ordre d�action est :
-
C1q,
C1r et C1s,
-
C4
et C2,
-
C3,
-
C5,
C6, C7, C8 et C9.
Ce
sont des composants � propri�t�s pro�enzymatiques : propri�t�s
enzymatiques mais il y a la n�cessit� d�un clivage prot�olytique pour �tre
activ�)
![]()
Lorsqu�un de ses composants est activ�, il est
not� :��� C1q
Il est activ� par clivage (obtention de 2
fragments) :
-
C3� "� C3a (grand fragment) et C3b (petit fragment)
-
A
l�exception de C2 :� C2� "� C2a (petit fragment) et C2b (grand fragment)
Il
est inactiv� par m�canisme de r�trocontr�le, il est not� :��� C1ai
v Voies d�activation du compl�ment :
Il
existe plusieurs voies dont 2 voies essentielles :
-
La voie
classique du compl�ment,
-
La voie alterne
du compl�ment,
-
La
voie des lectines.
� Voie
classique :
Elle est activ�e par la formation du complexe Ag�Ac
ou la fixation d�un anticorps sur une cellule pathog�ne. Cela concerne les
anticorps de nature IgM pentam�rique, mais aussi de nombreuses IgG (3, 4 et 5)
Cette voie est
d�pendante d�une r�ponse sp�cifique. In
vivo, la stimulation de cette voie se fait par l�introduction de virus
oncog�nique, certaines bact�ries et de l�ADN de synth�se.
Elle n�cessite l�intervention des 11 composants qui
r�agissent en cascade :
-
Unit�
de reconnaissance : C1q�C1r�C1s
-
Unit�
d�action : C4�C2 ; C3
-
Unit�
d�attaque membranaire : C5�C6�C7�C8�C9
� Unit� de reconnaissance :
-
C1q
est � l�unit� de tulipe �. Elle a une structure tubulaire et une
autre fibrillaire (~ fleur et tige) Sa structure
tubulaire interagit avec le domaine constant C4 des IgM (3 domaines C) ou
�ventuellement avec le domaine C2 des IgG (3 domaines C)
-
![]()
![]() C1r et C1s se
fixent sur la r�gion fibrillaire de C1q :
C1r et C1s se
fixent sur la r�gion fibrillaire de C1q :
C1q �" �C1q�C1r�C1s� (complexe)
����������������������� �������� Ca2+
� Unit� d�action :
-
C1q
poss�de une fonction enzymatique de clivage sur C4 " C4a et C4b.
-
![]() C4b se fixe � la
membrane par liaison covalente thiol�ester.
C4b se fixe � la
membrane par liaison covalente thiol�ester.
C4b + C2 �" �C4b�C2 �" �C4b�C2a��������������� = C3 convertase
![]()
![]() ���������������������������������� ������ Mg2+������� ������� C1s
���������������������������������� ������ Mg2+������� ������� C1s
C4b�C2a :� C3 �"� C3a + C3b
-
![]() C3b se fixe � la
membrane au niveau de C4b�C2a.
C3b se fixe � la
membrane au niveau de C4b�C2a.
C4b�C2a�C3b������������� =
C5 convertase
� Unit� d�attaque :
![]()
C4b�C2a�C3b :� C5 �"� C5a + C5b
-
-
Il
en est de m�me pour C7.
-
C8
et C9 se fixe au complexe par des m�canismes encore inconnus. Ils forment un
pore.
-
Le
complexe form� entra�ne la lyse de la cellule cible et permet l�interaction
avec les cellules phagocytaires.
� Voie
alterne :
Elle est activ�e par le complexe Ag�Ac mais plut�t
avec la fixation d�IgA avec tr�s souvent avec certaines bact�ries qui poss�dent
sur leur membrane certains polysaccharides. Elle se met en place plus
rapidement que la voie classique.
![]()
![]()
![]()
![]() Il n�y a pas
l�intervention C1 et C2. Cette voie commence avec une d�viation de C3 de la
voie classique :
Il n�y a pas
l�intervention C1 et C2. Cette voie commence avec une d�viation de C3 de la
voie classique :
C3b + B �"� C3b�B �"� C3b�Bb �"� C3b�Bb�P
�"� (C3b)n�Bb
![]()
![]()
![]() ���������������������������������� ���� D + Mg2+�� ���������� P��������� ������� Amplification
���������������������������������� ���� D + Mg2+�� ���������� P��������� ������� Amplification
����������������������������������������������������� R�le
de
� R�gulation
de la voie classique :
Sur
Il
existe des intercalants entre C1q, C1r et C1s. Ce sont des prot�ines qui
peuvent se fixer ou non � la membrane. Il y a CD35 entre autres.
Sur
C�est
la plaque tournante. C�est un syst�me labile (peu stable) qui s�auto�inactive
directement. Il y a aussi des inhibiteurs de C3b et C4b.
Sur la cellule
cible :
Elle
met en place des d�fenses par rapport au compl�ment gr�ce � des mol�cules de
liaison entre C4 et C2, comme DAF (= CD55) et CD59.
� R�gulation
de la voie alterne :
Il y a une r�gulation sur C3b :
-
Le
facteur H se lie � C3b et l�inactive,
-
Le
facteur I clive C3b.
Il
y a aussi l�intervention de prot�ines membranaires du type DAF.
v Les r�cepteurs du
compl�ment :
Ils sont surtout pr�sents � la surface des
phagocytes et des globules rouges (tr�s sensibles au compl�ment)
En
g�n�ral, il y a 5 cat�gories de r�cepteurs : CR1, 2, 3, 4 et 5 (dont les
mieux connus sont CR1, 2 et 3) :
-
CR1
est un r�cepteur qui a une sp�cificit� pour C2b et C4 et intervient� dans l�oposonisation.
-
CR2
et CR3 ressemblent � un r�cepteur de mol�cules d�adh�sion,
Il
existe aussi un r�cepteur de type araphylatoxine qui permet le rapprochement
physique des macrophages par fixation de l�anticorps.
Le d�r�glement peut se faire sur :
-
Le
r�arrangement des lymphocytes B,
-
Le
r�arrangement des lymphocytes T (TCR),
-
Le
CMH via sa diversit� par un m�canisme mol�culaire (= polymorphisme de
l�ADN),
-
La
reconnaissance de l�antig�ne (1er et 2�me signal),
-
Sp�cificit�
de reconnaissance.
Le
d�r�glement peut �tre soit un d�ficit, soit une hypersensibilit�.
v D�ficit :
� D�ficit
primaire :
Il
s�agit d�un d�ficit pr�sent d�s la naissance.
|
Cellules |
R�ponse immunitaire |
Infections |
Traitements |
|
|
Tumorale |
Cellulaire |
|||
|
Cellules
souches |
(( |
(( |
Toutes
ci�dessous |
Greffe de
moelle �pini�re |
|
Lymphocytes B |
(( |
Normale |
Bact�ries
pyog�nes, Pneumocycks corini |
g�globulines |
|
Lymphocytes B |
( |
(( |
Certains virus
candidats |
Greffe de
thymus |
|
Compl�ment |
Normale |
Normale |
Bact�ries
pyog�nes |
Antibiotiques |
|
Cellules
phagocytaires |
Normale |
Normale |
Bact�ries
pyog�nes |
Antibiotiques |
La
d�ficience g�nique en un r�cepteur � une cytokine a �t� le sujet de la 1�re
th�rapie g�nique consid�r�e comme positive.
� D�ficit
secondaire :
C�est
le cas du SIDA ou un d�ficit d� � une malnutrition.
v Hypersensibilit� :
Il
existe diff�rentes hypersensibilit�s : 3 d�pendantes d�anticorps (I, II,
III) et 1 retard�e (IV)
� Hypersensibilit�
d�pendante d�anticorps :
Elle
a besoin d�immunoglobulines fix� � l�anticorps de la cellule cible.
Hypersensibilit�
de type I :
Ce
sont les IgE qui y interviennent.

Hypersensibilit�
de type II et III :
Elle
est responsable des pathologies dues � des accidents de transfusion sanguines
et l�h�molyse du nouveau n� (d� au facteur rh�sus)
Ce
sont les IgM qui y interviennent (et �ventuellement les IgG) La liaison Ag�Ac
provoque des trous dans la membrane de la cellule cible. Cela fait augmenter le
processus d�inflammation.
Il
arrive que le complexe Ag�Ac circule dans le sang et se fixe sur une cellule de
l�organisme.
Hypersensibilit�
de type IV :
Elle est dite retard�e car elle se met en place en 1
� 3 jours du fait de l�implication des lymphocytes T. Il y a besoin d�une
pr�sentation de l�antig�ne par les CPA (cellules phagocytaires et macrophages)
Le probl�me est
l�incapacit� d��limination de l�antig�ne par le macrophage qui devient un
m�gacaryote.
v Pathologies au niveau de la
lymphoprolif�ration et de l�auto�innumit� :
� Lymphoprolif�ration :
Les
pathologies consistent en une erreur dans la maturation dans une cellule qui
�volue de mani�re clonale. On y trouve les leuc�mies.
� Maladies
auto�immunes :
Elles
consistent en un probl�me de tol�rance du soi dans la maturation. Il y a un
r�le des 1er, 2�me signaux et du polymorphisme du CMH
(facteurs d�association)