
Retour au sommaire des cours |

Une version pdf est à votre disposition ici. |
v N�cessit� d�un contr�le des
voies m�taboliques :
Une voie
m�tabolique est une r�action en cha�ne : le produit d�une r�action devient
le substrat d�une suivante. Il faut donc un contr�le fin.
De plus, les
voies m�taboliques cellulaires sont interconnect�es : elles doivent
fonctionner de fa�on coordonn�e.
Pour y parvenir,
il y a la mise en place de :
-
R�gulations
internes � chaque voie,
-
R�gulations
entre les voies m�taboliques,
-
R�gulations
d�pendantes de l��tat physiologique de l�organisme.
Mais il est
inutile de contr�ler toutes les activit�s enzymatiques. La r�gulation la plus
importante � contr�ler est la r�action la plus lente ; ainsi on contr�le
le d�bit m�tabolique.
Ce contr�le
s�effectue donc sur des enzymes cl�s, appel�es enzymes allost�riques, qui se
situent souvent apr�s un carrefour m�tabolique.
" Ces enzymes
cl�s catalysent des r�actions irr�versibles.
L�adaptabilit�
des voies m�taboliques se fait gr�ce � un certain nombre de m�canismes
r�gulateurs (� court et � long terme)
v Les diff�rents niveaux de
r�gulation :
.Poly
p 1.
� Perm�abilit�
membranaire :
� Transport passif � travers
une membrane :
Il se fait en
fonction du gradient de concentration et ne n�cessite pas de prot�ines de
transport.
 ������������������ ���� Flux
������������������ ���� Flux
(Vitesse de
passage����������������������������������������������� ����������� Semi
perm�able
par unit� de
surface)
Le
transport passif est insaturable.
���������������������������������������������������������������������������������������� Gradient
de concentration
Exemple de
mol�cules utilisant ce transport : les st�ro�des.
� Transport facilit� (ou
exergonique) :
Il se fait
toujours en fonction du gradient de concentration et mais n�cessite un
transporteur pour facilit� le transport.
 ������������������ ���� Flux
������������������ ���� Flux
(Vitesse de
passage����������������������������������������������� ����������� Semi
perm�able
par unit� de
surface)
���������������������������������������������������������������������������������������� Gradient
de concentration
Le transport facilit� est saturable. Les
prot�ines transporteurs se comportent comme des enzymes : les sites de
fixation peuvent tous �tre satur�s.
Exemple d��l�ments utilisant ce
transport : les ions, nucl�otides, acides amin�s et m�tabolites.
� Attention !
Ne pas confondre avec le transport actif. Ce dernier est un
transport qui se fait contre le gradient de concentration ; c�est donc un
processus endergonique.
Les diff�rents types de transport
facilit�s :
Leur
classification se fait selon la stoechiom�trie du processus :
-
Uniport,
-
Symport,
-
Antiport.
� Disponibilit�
en substrat et coenzymes :
Il s�agit d�une
r�gulation indirecte qui permet la disponibilit� des �l�ments de la r�action.
� R�gulateurs
exog�nes du m�tabolisme cellulaire :
Les agents
sont :
-
Les
hormones (pr�sentes dans la circulation),
-
Les
facteurs de croissance (action locale, produits par les cellules proches),
-
Les
cytokinines (dans le processus anti�inflammatoire, m�me m�canisme que les
facteurs de croissance),
-
Les
m�diateurs nerveux.
� Les r�gulateurs hormonaux de
l�hom�ostasie glucidique :
-
Insuline,
s�cr�t�e par les cellules b des �lots de Langerhans
pancr�atiques ;
-
IGF�I,
glucocortico�de s�cr�t� par le cortex surr�nalien (= couche externe de la
glande surr�nale) ;
-
Glucagon,
s�cr�t� par les cellules a des �lots de Langerhans
pancr�atiques ;
-
Adr�naline
(ou �pin�phrine), cat�cholamine s�cr�t�e par la m�dulla surr�nalienne (= partie
int�rieure de la glande surr�nale) ;
Cat�cholamine =���� Adr�naline (ou �pin�phrine)���� &��
Noradr�naline (ou nor�pin�phrine)
-
Hormone
de croissance (GH), s�cr�t�e par l�hypophyse ant�rieure, r�le important dans la
mobilisation des voies du m�tabolisme glucidique.
� R�gulation hormonale de la
glyc�mie :
|
Hormone |
Action |
|
|
Insuline |
(
Glucose |
Hormone
hypoglyc�miante |
|
Glucocortico�des |
& Glucose |
Hormones hyperglyc�miantes |
|
Glucagon |
& Glucose |
|
|
Hormone de
croissance |
& Glucose |
|
|
Adr�naline |
& Glucose |
|
Les cibles
tissulaires principales :� le foie,
les muscles squelettiques et le tissu adipeux.
La sensibilit�
de la cellule aux agents de r�gulation est fonction de sa disponibilit� en
r�cepteurs � ceux�ci.
� Transmission de l�information
de l�ext�rieur vers l�int�rieur de la cellule :
Hormone

![]() ����������������������������������������������������������������� R�cepteur
����������������������������������������������������������������� R�cepteur
����������������������������������������������������� � Transducteur (par exemple : prot�ine G)
![]() ����������������������������������������������������� Effecteur
(par exemple :
Ad�nylate cyclase)
����������������������������������������������������� Effecteur
(par exemple :
Ad�nylate cyclase)
������������������ ATP�������������������������������������� "
Activit� enzymatique
����������������������������������������� Messager
secondaire
����������������������������������������� ou
2nd messager��������� (exemple :
AMPc)
![]()
Apport des informations
dans la cellule��� par Activation�Stimulation
de :
����������������������������������������� Prot�ine
kinase A� (activ�e)
����������������������������������������������������� $
����������������������������������������� Phosphorylation de prot�ines
����������������������������������������������������� $
����������������������������������������� Modification
d�activit�
����������������������������������������������������� $
����������������������������������������� Effets
biologiques
La transduction
du signal hormonal � travers la membrane plasmique induit une cascade
d��v�nements intracellulaires qui servent � amplifier le signal et � le
distribuer aux diff�rents compartiments cellulaires pour modifier plusieurs
fonctions cellulaires en parall�le.
.Poly
p 1.
Les hormones
induisent des r�ponses cellulaires lentes et rapides.
.Poly
p 1.
�
Voie
de signalisation de l�adr�naline :
.Poly
p 2.
Fixation
de l�hormone sur le r�cepteur
$
Changement
conformationnel
$
Communication
de ce changement � la prot�ine G
= h�t�ro�trim�re � activit� ATPasique
$
Perte de
conformation
$
Activation
de l�adr�nylate cyclase
$
Synth�se
en grande quantit� d�AMPc � partir de l�ATP
$
Activation
de la prot�ine kinase A par l�AMPc
+
Hydrolyse
de la partie GTP de la sous�unit� a par les
propri�t�s intrins�ques de celle�ci
" Verrou de s�curit� �vitant une situation permanente
Activation de la prot�ine kinase A par
l�AMPc :
.Poly
p 2.
����������������������������������������������������������������� Sous�unit�
r�gulatrice
���������������������������������������������������������������������������������������������������� ������ Sous�unit� catalytique
![]()
S�quence
� Pseudo�substrat �
���������������������������������������������������������������������������������������������������������������������������� AMPc
Fixation
de l�AMPc
$
Changement
conformationnel
au niveau du la
s�quence � Pseudo�substrat �
$
Lib�ration
de la sous�unit� catalytique

" Phosphorylation de prot�ines sur la s�quence peptique :
Arg
� Arg � quelconque � Ser ou Thr
La
phosphorylation se fait sur le dernier acide amin� de cette s�quence (Ser ou
Thr).
"� Cette prot�ine kinase A est donc appel�e
Ser_Thr kinase.
Au final, la
sous�unit� catalytique est lib�r�e.
�
Voie
de signalisation de l�insuline :
Il y a une
r�ponse dim�ris�e reli�e par un pont disulfure :

�
Activit� de
�
Phosphorylation
de
Et
Cascade de
d�phosphorylation
�
Activit�s
phosphoasique et kinasique alt�r�es
�
Effets
biologiques terminaux :
-
Synth�se
de glucose, de prot�ines, lipides, glycog�ne ;
-
Croissance
et transport ;
-
Synth�se
de l�expression des g�nes.
�
Les
st�ro�des :
Il n�existe que
des r�cepteurs intracellulaires.
Une fois que
l�hormone est fix�e, il int�gre le noyau de la cellule et active un certain
nombre d�expressions de g�nes (transcription)
� R�gulation
du nombre de mol�cules enzymatique actives :
Transcription��������������������� Traduction������������������� R�gulation post�synaptique
ADN�������������� ARN�������������� Enzyme
����������������������� (�pissage
alternatif� "� Isoenzymes)
 ���������������������������������������������������������������������������������������� D�gradation
���������������������������������������������������������������������������������������� D�gradation
�
R�gulation
par phosphorylation�d�phosphorylation,
�
Transition
allost�rique,
"� Les plus
importantes.
�
Activation
par prot�olyse limit�e
"� Suppression du pr�curseur prot�ique,
�
R�gulation
par combinaison des sous�unit�s.
� Contr�le
transcriptionnel :
Le contr�le se
fait sur la vitesse de la transcription et sur la stabilit� de l�ARN.
�
Isoenzymes
:
Elles diff�rent
dans leurs s�quences peptidiques mais catalysent la m�me r�action.
Elles poss�dent
des cin�tiques enzymatiques diff�rentes et/ou
ont des affinit�s diff�rentes vis���vis du substrat et/ou sont r�gul�es de mani�res diff�rentes.
L�utilisation
diff�rentielle de ces isoenzymes permet une r�gulation fine du m�tabolisme
adapt�e � chaque organe ou tissu cellulaire.
Exemple : la lactate
d�shydrog�nase :
C�est une
prot�ine t�tram�rique poss�dant 2 types de sous�unit�s (avec 75%
d�homologie) :� une appel�e H
(Heart) et une autre appel�e M (Muscle)
Il existe
diff�rentes combinaisons possibles :�������� H4 ; H3M ; H2M2 ; HM3 ; M4
����������������������������������������������������������������� ������� (c�ur)���������������������������� ��� (foie)
-
H4 a une forte
affinit� pour le pyruvate et est inhib�e allost�riquement par des
concentrations �lev�es de pyruvate.
"� Dans le c�ur, la glycolyse est importante,
donc H4 n�est quasiment pas active.
-
M4 a une faible
affinit� pour le pyruvate mais elle n�est pas inhib�e.
"� La sous�unit� M pr�domine dans les tissus
supportant les conditions ana�robies (muscle, foie) alors que la sous�unit� H
pr�domine dans les tissus a�robies.
Int�r�t des isoenzymes :
-
Obtenir
des profils m�taboliques diff�rents des diff�rents organes.
Exemple :�������� Les 2 isoformes de la phosphorylase du
glycog�ne pr�sentes dans les muscles et le foie poss�dent des r�gulateurs
diff�rents.
-
Assurer
des localisations subcellulaires diff�rentes et donc des r�les m�taboliques
diff�rents dans la cellule.
Exemple :�������� L�isocitrate d�shydrog�nase.
-
Adapter
les activit�s enzymatiques aux diff�rentes �tapes du d�veloppement.
Exemple :�������� Les tissus embryonnaires et f�taux sont
diff�rents des tissus adultes ;
����������������������� Les cellules canc�reuses
sont diff�rentes des cellules normales.
-
Assurer
des r�ponses diff�rentes (suivant les organes) aux effecteurs
allost�riques :
Exemple :�������� La glucokinase h�patique et les
hexokinases extra�h�patiques ont des sensibilit�s diff�rentes � l�inhibition
par le glucose_6�.
� Contr�le traductionnel :
Il se fait sur
la vitesse de traduction et sur la � vie de la prot�ine.
� Contr�le
post�traductionnel :
�
R�gulation
allost�rique :
Exemple d�enzyme allost�rique : L�aspartate
transcarboxylase (ATCase) :
Elle catalyse la
1�re �tape de la voie de synth�se des bases pyrimidiques :
![]()
![]()
![]() Carbamoyl��
+� Aspartate�������������� N_Carbamoylaspartate��������� ����������� Cytidine_Tri�
Carbamoyl��
+� Aspartate�������������� N_Carbamoylaspartate��������� ����������� Cytidine_Tri�
Sa cin�tique est
non mickaellienne : la courbe a une allure sigmo�dale (et non
hyperbolique)
 Taux de
formation
Taux de
formation
de
N_Carbamoylaspartate
[ Aspartate ] en
mM
����������������������������������������������������� ���� �10������������� 20������ ������ 30������������ 40
Cette cin�tique
est due � la structure polym�rique :�������� 6
sous�unit�s catalytiques
����������������������������������������������������������������������������� ������� +� 6
sous�unit�s r�gulatrices
L�ATCase oscille
entre 2 �tats conformationnels :
-
Un
�tat R (rel�ch�) poss�dant une forte affinit� pour le substrat� (Km faible),
-
Un
�tat T (tendu) poss�dant une faible affinit� pour le substrat� (Km �lev�)
L��tat
R pr�sente une dilatation de la conformation permettant un meilleur acc�s pour
les sites de r�action.
Le passage d�un
�tat conformationnel � l�autre s�appelle la transition allost�rique.
Il
existe 2 mod�les de transition allost�rique :
-
Un
mod�le dit concert�, dans lequel la
liaison de l�effecteur allost�rique modifie la conformation de toutes les
sous�unit�s (c�est le cas de l�ATCase),
-
Un
mod�le dit s�quentiel, pour lequel
il existe des �tats interm�diaires o� certaines sous�unit�s sont sous la forme
R et d�autres sous la forme T.
 Taux de
formation���������������������������������������������������������������������� ����������� �
Etat R
Taux de
formation���������������������������������������������������������������������� ����������� �
Etat R
de
N_Carbamoylaspartate����������������������������������� si toutes les enzymes restaient dans l��tat R
����������������������������������������������������������������� Courbe
r�elle
���������������������������������������������������������������������������������������������������� Etat
T
si toutes les enzymes restaient dans l��tat T
[ Aspartate ]
����������������������������������������������������� ����� 10�������������
20������ ������ 30������������ 40
La courbe
sigmo�de typique de l�enzyme allost�rique est une combinaison des courbes de
l�enzyme � l��tat R (forte affinit� pour le substrat) et de l�enzyme � l��tat T
(faible affinit� pour le substrat)
R�gulation allost�rique de l�activit�
enzymatique (mod�le concert�) :

����������������������������������������������������������������� Inhibiteur
���������������������������������������������������������������������������������������������������� Forme R�
(�tat
catalytique)
����������������������������������������������������������������������������� Substrat���������� ����������� � Affinit� plus�
importante
�� pour les
activateurs
![]()
![]()
Activateur��������������������������� �� Equilibre tenu par
�� les concentrations
������ des effecteurs
activateurs
et inhibiteurs
���������������������������������������������������������������������������������������� �������� ��
Forme T�� (�tat
inhib�)
���������������������������������������������������������������������������������������������������������������� Affinit�
plus� importante
���������������������������������������������������������������������������������������������������������������� ��� pour les inhibiteurs
L�effecteur
allost�rique peut��tre :
-
Homotrope :
il modifie sa propre affinit� vis���vis de l�enzyme. C�est le cas du substrat.
-
H�t�rotrophe :
il modifie l�affinit� d�une autre mol�cule, en g�n�ral le substrat, vis���vis
de l�enzyme.
-
Si
l�effecteur d�place l��quilibre conformationnel de l�enzyme vers la forme R, il
est dit activateur.
-
Si
l�effecteur d�place l��quilibre conformationnel de l�enzyme vers la forme T, il
est dit inhibiteur.
Pour l�ATCase :
-
L�aspartate
(substrat) est un activateur allost�rique homotrope,
-
L�ATP
est un activateur allost�rique h�t�rotrope,
-
Le
CTP est un inhibiteur allost�rique h�t�rotrope.
 Taux de
formation����������������������� + 2mM�����������
d�ATP����������������������������������� ����������� �
Etat R
Taux de
formation����������������������� + 2mM�����������
d�ATP����������������������������������� ����������� �
Etat R
de
N_Carbamoylaspartate�����������������������������������
����������������������������������������������������������������� Courbe
r�elle
(
Km ;� &
affinit�
(
Km ; &
affinit������������������������������������������������������������������������������ Etat
T
+
[ Aspartate ]
����������������������������������������������������� ����� 10�������������
20������ ������ 30������������ 40
Int�r�t biologique de la r�gulation
allost�rique de l�ATCase :
-
R�tro�inhibition
du CTP sur l�ATCase :
Elle permet de
freiner la synth�se des bases pyrimidiques et d��viter une accumulation de ces
bases quand les conditions propices � la production d�ARNM et � la
duplication de l�ADN sont absentes (par exemple : ATP faible)
-
L�activation par
l�ATP :
L�ATP, par ce
m�canisme, va promouvoir la production de l�ADN quand l��nergie et les bases
puriques sont pr�sentes en abondance.
Syst�me K :����������� Affinit� de l�enzyme pour R > T
Il suppose que
le substrat a plus d�affinit� apparente pour l�une des formes (R) que l�autre
(T) :���������� "� La constante de Mickaelis de R est inf�rieure
� celle de T.
������ " Des sites de T
peuvent aussi fixer le substrat et
-
Le
substrat se comporte comme un effecteur homotrophique ;
-
La
saturation de l�enzyme par le substrat n�est pas mickaelienne ;
-
La
fixation du substrat par l�enzyme est mickaelienne.
 Vitesse������� Avec activateur��� Sans effecteur��� Avec
inhibiteur
Vitesse������� Avec activateur��� Sans effecteur��� Avec
inhibiteur
Vm�����
[
Aspartate ]
Syst�me V :����������� M�me affinit� apparente de l�enzyme
pour R et T par rapport au substrat mais KCAT de R > KCAT de T
Il suppose que
le substrat a la m�me affinit� apparente pour les formes R et T ; mais
celles�ci sont diff�rentes par leur KCAT .
-
La
forme R a
-
Le
substrat ne se comporte pas comme un effecteur allost�rique ;
-
La
saturation de l�enzyme par le substrat est mickaelienne ;
-
Par
contre, les fixations coop�ratives des activateurs et inhibiteurs allost�riques
ne sont pas mickaelienne.
�
R�gulation
par modification covalente :
La liaison d�une
mol�cule � une enzyme peut modifier son activit�.
-
La
plus part de ces modifications sont r�versibles (phosphorylation, ac�tylation)
-
D�autres
sont irr�versibles (modifications lipidiques permettant la localisation de
l�enzyme � la membrane.
� R�gulation par phosphorylation �
d�phosphorylation :
L�action de
nombreuses prot�ines est modifi�e par phosphorylation (= addition d�un
groupement phosphoryle sur la fonction hydroxyle des r�sidus S�rine, Thr�onine
ou Tyrosine.
Les
phosphorylations sont catalys�es par des prot�ines kinases, elles�m�mes
soumises � r�gulations.
Dans les
conditions physiologiques, les r�actions de phosphorylation sont irr�versibles.
L�existence de phosphatases, elles aussi r�gul�es, assure les r�actions de
d�phosphorylation.
" Le niveau de
phosphorylation d�pend donc des activit�s relatives des kinases et des
phosphatases.
� Sp�cificit� des kinases :
�� R�sidu S�rine
���������������������������������������������� �O������� ��� H���
O
![]()
![]() �││�������� �����
│������ ││
�││�������� �����
│������ ││
Prot�ine non phosphoryl�e�������������������������� C � N � C � C � N
����������� │ ����� │������ ����������
│
����������������������������������������������������������������� ������� H �� CH2OH� H
![]()
![]()
![]()
![]() ����������������������������������������������������������������� ATP��������������������������� Pi
����������������������������������������������������������������� ATP��������������������������� Pi
����������������������������������������������������� Kinase�������� ����������� ����������� ����� Phosphatase
����������������������������������������������������������������� ADP�������������������������� H2O
���������������������������������������������� �O������� ��� H���
O
![]()
![]() �││�������� ����� │������ ││
�││�������� ����� │������ ││
���������������������������������������������������������������������� �C � N � C � C � N
����������� │ ����� │������ ����������
│
����������������������������������������������������������������� ������� H � CH2O��
H
�� R�sidu Tyrosine
���������������������������������������������� �O������� ��� H���
O
![]()
![]() �││�������� ����� │������ ││
�││�������� ����� │������ ││
Prot�ine non phosphoryl�e�������������������������� C � N � C � C � N
����������� │ ����� │������ ����������
│
����������������������������������������������������������������� ������� H �� CH2 �������H
� ���│�������
![]() �����������������������������������������������������������������������������
�����������������������������������������������������������������������������
���� │�������
����������������������������������������������������������������������������� � OH
![]()
![]()
![]()
![]() ����������������������������������������������������������������� ATP��������������������������� Pi
����������������������������������������������������������������� ATP��������������������������� Pi
����������������������������������������������������� Kinase�������� ����������� ����������� ����� Phosphatase
����������������������������������������������������������������� ADP�������������������������� H2O
���������������������������������������������� �O������� ��� H���
O
![]()
![]() �││�������� ����� │������ ││
�││�������� ����� │������ ││
���������������������������������������������� ����������������������� �C � N � C � C � N
����������� │ ����� │������ ����������
│
����������������������������������������������������������������� ������� H �� CH2 �������H
���� │�������
![]() �����������������������������������������������������������������������������
�����������������������������������������������������������������������������
���� │�������
����������������������������������������������������������������������������� � O���
Certaines
prot�ines kinases sont multifonctionnelles et peuvent phosphoryler diff�rentes
prot�ines cibles. D�autres ne peuvent phosphoryler qu�une prot�ine particuli�re
ou une famille de prot�ines structurellement proches.
Par exemple :
-
Arg � Arg � (petit acide amin� comme Gly)
� Ser � (acide amin� hydrophobe de grande taille)
-
Arg � Arg � (petit acide amin� comme Gly)
� Thr � (acide amin� hydrophobe de grande taille)
� S�rine � Thr�onine prot�ines
phosphatase :
-
Phosphatases de
type 1 (PP1) :
Elles sont
inhib�es par 2 prot�ines cytosoliques thermostables ( I�1 et I�2)
Elles
d�phosphorylent pr�f�rentiellement la sous�unit� b de la
phosphorylase kinase.
-
Phosphatases de
type 2 (PP2) :
Elles sont
insensibles aux 2 prot�ines cytosoliques thermostables ( I�1 et I�2)
Elles
d�phosphorylent pr�f�rentiellement la sous�unit� a de la
phosphorylase kinase.
Elles ont �t�
subdivis�es selon leurs diff�rences dans les m�canismes d�activation :
-
PP2�A
(spontan�ment actives),
-
PP2�B
(d�pendantes du Ca2+),
-
PP2�C
(d�pendantes du Mg2+),
� Comment la phosphorylation
modifie�t�elle l�activit� enzymatique ?
-
Par l�addition de charges n�gatives,
modifiant les interactions �lectrostatiques ;
-
Par formation de liaisons H, pouvant
alt�rer les capacit�s de liaison de la prot�ine ;
-
En se comportant comme un effecteur
allost�rique, d�pla�ant l��quilibre entre les formes T et R de l�enzyme.
Int�r�t biologique d�une telle
r�gulation :
-
M�canisme
rapide,
-
Amplification,
-
Liaison
du m�canisme � l��tat �nerg�tique de la cellule.
v Les transporteurs du
glucose :
Le transport est
facilit� par les transporteurs de glucose : GLUT.
"� C'est���dire que le transport se fait dans le
sens de la concentration.
Il existe 5
membres principaux :��� GLUT_1� �� GLUT_2.
Ce sont des
glycoprot�ines de 500 acides amin�s poss�dant 12 r�gions hydrophobes :
������ "� Insertion dans la membrane plasmique par 12
domaines transmembranaires.
Repr�sentation d�un GLUT :
y
 Glycosylation pour
prot�ger des glycoprot�ines.
Glycosylation pour
prot�ger des glycoprot�ines.
Ext
Int
NH3+����������������������������������������������������������������������������������������������������������������������������������� ��������� COO�
Dans les
�rythrocytes, il y a environ 500 000 mol�cules de GLUT_1.
La famille des transporteurs de
glucose :
|
Nom |
Localisation
tissulaire |
Km |
Fonction |
|
GLUT_1 |
Erythrocytes, Dans tous les
tissus Faible
concentration dans le foie et les reins |
|
Pr�l�vement
basal de glucose (minimum vital
pour le glucose) |
|
GLUT_2 |
Cellules b
pancr�atiques, Foie |
15 � |
Entr�e de
glucose proportionnelle � la glyc�mie dans le foie et les cellules b pancr�atiques |
|
GLUT_3 |
Environ tous
les tissus |
|
Pr�l�vement
basal (presque m�me
fonction que GLUT_1) |
|
GLUT_4 |
Cellules
musculaires, Adipocytes |
|
Pr�l�vement
insulinod�pendant du glucose |
|
GLUT_5 |
Intestin gr�le |
|
Transporteur
de fructose |
Biocapteurs du taux de glyc�mie :� GLUT_2
 Flux de glucose
Flux de glucose
Flux max
![]() ������������������ ���� 1���� �������� 5������������ � 10����� �������� 15���������� ���� 20
������������������ ���� 1���� �������� 5������������ � 10����� �������� 15���������� ���� 20
������������������������������ Glyc�mie normale
GLUT � faible Km :��������� Par exemple
GLUT_1
����������������������������������������� " Il
a une forte affinit� au glucose.
������ Dans les conditions physiologiques :
il y a une quasi�saturation des ces transporteurs.
������ "� Dans le cas d�une augmentation de la
glyc�mie, il n�y a aura pas une grande entr�e de glucose par ces transporteurs.
GLUT � moyen Km :������ Par exemple GLUT_4
������ Il sert � faire entrer du glucose quand
les r�cepteurs GLUT_1 saturent.
������ Il est le seul � �tre stimul� par l�insuline
pour le stockage sp�cifique du glucose dans les cellules musculaires et
adipocytes.
GLUT � fort Km :����������� Par exemple GLUT_2
����������������������������������������� " Il
a une faible affinit� au glucose.
������ Il sert � faire entrer du glucose quand
les r�cepteurs GLUT_1 saturent. L�entr�e est proportionnelle � la concentration
du glucose.
v M�canisme de transport du
glucose :
.Poly
p 3.
Il est dit du
� pore � soupape �.�����
"� Les prot�ines transmembranaires alternant
entre les 2 �tats conformationnels.
v R�gulation de l�entr�e du
glucose par l�insuline :
L�insuline
stimule l�entr�e du glucose dans les cellules (adipocytes et cellules
musculaires) en modifiant la distribution subcellulaire des transporteurs du
glucose.
Son action est tr�s rapide : en 15
min, le flux (= vitesse de passage par unit� de surface) est augment� de 6 � 12
fois.
Cette
stimulation n�est pas affect�e par les inhibiteurs de la synth�se prot�ique
(transcription ou traduction) Elle ne requiert pas de la synth�se prot�ique.
.Poly
p 3.
GLUT_4 :
Ces
transporteurs sont dans le cytosol. L�insuline provoque la mobilisation des
GLUT_1 vers la membrane plasmique et donc leur exocytose. Les transporteurs
s�int�grent � la membrane mais n�y restent pas : quand il n�y a plus de
stimulation, il y a une endocytose des v�sicules transportant les
transporteurs.
L�insuline a un
caract�re hypoglyc�miant car elle provoque l�entr�e du glucose dans les tissus
p�riph�riques.
R�gulation de la s�questration
intracellulaire de GLUT_4 :
.Poly
p 3.
Hypoth�se :
Les v�sicules
contenant GLUT_4 sont s�questr�es hors du syst�me constitutif de recyclage des
endosomes par l�association avec des � r�cepteurs de r�tention � (RR)
localis�s sur des structures tubulo�v�siculaires situ�es � proximit� de la
membrane.
v Le transport du glucose
dans l��pith�lium intestinal :
.Poly
p 3.
v Identification des enzymes
r�gulatrices :
Mise en �vidence des m�canismes
contr�lant le flux d�une voie m�tabolique :
-
Identification
des r�actions � vitesse limitante ;
-
Mesure
des DG des diff�rentes r�actions :
"� Les r�actions loin de l��quilibre sont des
points de contr�le potentiel ;
-
Identification,
in vitro, des effecteurs allost�riques
des enzymes catalysant ces r�actions :
"� M�canismes mis en jeu ;
-
Mesure
des concentrations in vivo des r�gulateurs pr�sum�s :
"� Compatibilit� des changements de
concentrations dans diff�rentes concentrations avec le m�canisme de contr�le
propos�.
v R�gulation de l�activit�
des enzymes cl�s :
� R�gulation
de l�hexokinase et de la glucokinase :
� Inhibition allost�rique par
le G�6� :
La
phosphorylation est assur�e par des kinases :
-
Le
Km pour le glucose :���
Hexokinase
"�
Glucokinase
"�
-
Comportement de
l�enzyme :
L�hexokinase :����������� mickaelien
Glucokinase :� allost�rique
La glucokinase
est l�exception des enzymes allost�riques car la glucokinase est monom�rique.
Stimulation par le glucose :
������ Vitesse / Vmax

������������������ �� 1����������������������������������������������������������������� ���� Hexokinase (ubiquiste)
������������������ ���������������������������������������������������������������������� � Glucokinase (cellules
h�pathiques,
������������������ 0,5���������������������������������������������������������������������������������������� cellules b
pancr�atiques)
���������������������������������������������������������������������������������������������������� �� [Glucose] en mM
������������������ ������ 0�������������� ��� 5����������������� 10������������������� 15
Inhibition par le glucose�6� :
������������������ Vitesse

����������������������������������������������������������������������������� ����������� ��
��Glucokinase (indiff�rente)
���������������������������������������������������������������������������������������� ���� Hexokinase
������ ��������������������������������������������������������������������������������������������� �� [Glucose�6�]
Le glucose_6� ne pr�sente aucune inhibition
sur l�activit� de la glucokinase, donc l�activit� glucokinase est
proportionnelle � la quantit� de glucose qui entre dans la cellule.
� Activation allost�rique par
le phosphate min�ral Pi :
Elle ne concerne
que l�hexokinase.
Cette activation
est indirecte : le Pi fait diminuer l�affinit� pour le glucose_6� et donc permet la lev�e de
l�inhibition par le glucose_6� de
l�hexokinase.
� R�gulation de la glucokinase
h�patique :
Exemple de cycle futile : le cycle Glucose � Glucose_6� :

������������������ � Pi����������������������������������������� Glucose��������������������������������� ������ ATP
������������������ ����� Glucose_6_phosphatase������������������������� � �Glucokinase
������������������ H2O��������������������������� ������ �Glucose_6����������������������������� ������ ADP
�� �� ATP� +� H2O� "� ADP�
+� Pi
La chaleur
d�pens�e dans ces r�actions permet � l�organisme de maintenir sa temp�rature
corporelle.
Le foie est
consommateur et producteur de glucose. Ce dernier ne doit donc pas �tre
consomm� par la glucokinase (GK) ; il faut �viter la mise en place de ce
cycle.
Pour cela, la cellule h�patique a mis en
place un m�canisme de r�gulation particulier o� elle s�questre cette activit�
dans le noyau.
-
-
L�augmentation
de la concentration intracellulaire en glucose entra�ne la translocation de
-
-
Il
y a ensuite une s�questration nucl�aire gr�ce � la fixation � une GKRP
(Glucokinase Regulatory Proteins)
Ce m�canisme
permet la limitation de l�action catalytique de
(le cycle futile
est minimis�)
Il y a ainsi une
s�cr�tion h�patique du glucose.
Ce r�le r�gulateur est limit� :
-
Le
glucose_6� est � l�origine
de plusieurs voies m�taboliques (synth�se du glycog�ne, voies des
pentoses�phophates)
-
Il
n�y a pas de r�le si le glucose est fourni par la d�gradation du glycog�ne, car
la glycog�nolyse fournit du glucose_1�.
Le glucose�� est un carrefour m�tabolique :
Glucose
 ����������������������������������������������������������������������������� �ATP
����������������������������������������������������������������������������� �ATP
����������������������������������������� ������ Hexokinase
����������������������������������������������������������������������������� �ADP
Glucose_6�
Glucose_1�������������������������������� Fructose_6������������������������ 6_phosphogluconate
Glycog�ne������������������������������������ Pyruvate�������������������������������� Ribose������������
������� " Stockage��������������������������� " ATP,
Biosynth�se������������� " NADPH, Synth�se
nucl�otidique
� La glucokinase = d�tecteur de
glucose dans les cellules b pancr�atiques :
.Poly
p 4.
� C�est une
v�ritable sonde m�tabolique qui renseignent sur la glyc�mie des cellules b.
Le glucose entre
dans la cellule
�
Il est
transform� en pyruvate avec la cr�ation d�ATP ;
�
L�ATP entra�ne
la fermeture de canaux K+ (sensibles �
l�ATP) ;
�
Une
d�polarisation membranaire est d�clench�e ;
�
Des canaux Ca2+ s�ouvrent,
permettant l�entr�e des ions Ca2+ ;
�
Le Ca2+ provoque
l�exocytose de v�sicules (migration vers la membrane) ;
�
Lib�ration
d�insuline.
Des mutations de
-
Aux
USA, 1 individu sur 2400 h�t�rozygotes porte des mutations de g�ne de
-
Ces
mutations seraient une des principales causes de l�apparition de diab�te non
insulino�d�pendant.
Baisse
d�activit� de
�
Augmentation du
seuil de sensibilit� vis���vis du glucose (pour la synth�se d�insuline)
�
Diminution de la
synth�se d�insuline
�
Baisse du
pr�l�vement h�patique du glucose et du catabolisme glucidique h�patique
concomitant � une augmentation de la production h�patique de glucose.
� R�gulation
de la phosphofructokinase 1 (PFK 1) :
Glycolyse :
Glucose
![]()
![]() ����������������������������������������������������������������������������� �ATP
����������������������������������������������������������������������������� �ATP
����������������������������������������� ������ Hexokinase
����������������������������������������������������������������������������� �ADP
Glucose_6�
![]() ����������������������������������������������������������������������������� �
����������������������������������������������������������������������������� �
������ ����������������������� ����� Phosphoisom�rase
����������������������������������������������������������������������������� �
Fructose_6�
![]()
![]() ����������������������������������������������������������������������������� �ATP
����������������������������������������������������������������������������� �ATP
����������������������������������������������������� � PFK 1��������������������������������� (=
PhosphoFructoKinase 1)
����������������������������������������������������������������������������� �ADP
Fructose_1,6 di�
![]() ����������������������������������������������������������������������������� �
����������������������������������������������������������������������������� �
����������������������������������������������������� Aldolase
����������������������������������������������������������������������������� �
Glyc�rald�hyde
![]()
DHA�
-
Elle
catalyse la r�action la plus lente ;
-
Elle
oscille entre 2 �tats conformationnels T et R.
Elle se situe
dans le cytosol et est compos�e de 4 sous�unit�s identiques (=
homot�tram�re) :
-
4
x 83 000
Da� (chez les eucaryotes),
-
4
x 41 000
Da� (chez les procaryotes)
� Inhibition
allost�rique :
Il s�agit d�un
r�trocontr�le n�gatif par des indicateurs de charge �nerg�tique forte :
ATP, citrate, NADH.
�
ATP :
Fructose_6�
![]()
![]() ����������������������������������������������������������������������������� �ATP
����������������������������������������������������������������������������� �ATP
����������������������������������������������������� � PFK 1��������������������������������� (=
PhosphoFructoKinase 1)
����������������������������������������������������������������������������� �ADP
Fructose_1,6 di�
������������������ Vitesse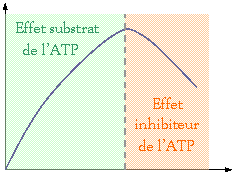
���������������������������������������������������������������������������������������������������� [
ATP ]
Sur
-
Un
site catalytique avec une forte affinit�, pour de faibles concentrations de
glucose et d�ATP ;
-
Un
site allost�rique avec une faible affinit�, pour de fortes concentrations de
glucose et d�ATP ;
Quand il y a de
fortes concentrations en ATP, ce dernier se fixe uniquement sur le site
allost�rique.
������������������ Vitesse
����������������������������������������������������������������� Faible
[ATP]
������������������ �� Vm
����������������������������������������������������������������������������� Forte
[ATP]
���������������������������������������������������������������������������������������������������� [fructose_6�]
����������������������������������������� ���� Km1������� Km2
L�ATP est un
inhibiteur allost�rique h�t�rotrope de
 " Quand il y a
fixation de l�ATP sur
" Quand il y a
fixation de l�ATP sur
Charge
�nerg�tique� =�
 Vitesse relative
des r�actions
Vitesse relative
des r�actions
���������������������������������������������������������������������������������������������������� ������ R�action utilisation de l�ATP
������������������ �
���������������������������������������������������������������������������������������������������� R�action
produisant de l�ATP
���������������������������������������������������������������������������������������������������������������� Charge
�nerg�tique
������������������������������ 0��������� ���
0,25������������ 0,5������ ������
0,75��������� 1
"� La glycolyse se r�alise dans n�importe quelle
condition ; elle r�gule la charge �nerg�tique de la cellule.
La concentration en ATP est maintenue �
peu pr�s constante gr�ce � 2 r�actions :
![]() ����������������������������������������������������� Cr�atine
kinase
����������������������������������������������������� Cr�atine
kinase
ATP� +�
cr�atine�������������������������������� ����� ����phosphocr�atine� +� ADP
����������������������������������������������������� ��� DG � 0
![]() ����������������������������������������������������� Ad�nylate
kinase (ou myokinase)
����������������������������������������������������� Ad�nylate
kinase (ou myokinase)
2
ADP����������������������������������� ����������� ATP�
+� AMP
|
|
Concentration avant la
consommation d�ATP |
Concentration apr�s la
consommation d�ATP |
Changement
relatif (en %) |
|
ATP |
|
|
10 % |
|
ADP |
|
|
0 % |
|
AMP |
|
|
600 % |
Probl�me :
La concentration
d�ATP varie peu� (� 10%) mais le
flux glycolytique varie de 1 � 100.
"� Il y a d�autre(s) m�canisme(s) que la
r�gulation allost�rique par l�ATP.
�
Citrate
et NADH :
Ce sont 2
inhibiteurs allost�riques de PFK 1 qui renforcent l�effet inhibiteur� d�ATP.
� Activation
allost�rique :
�
AMP :
C�set un
activateur h�t�rotrope : il modifie, en diminuant, l�affinit� de l�enzyme
vis���vis de son inhibiteur allost�rique : l�ATP.
 ������������������ Vitesse
������������������ Vitesse
����������������������������������������������������� Faible
[ATP]������������� Fort [ATP] + Faible [AMP]
����������������������������������������������������������������������������� Forte
[ATP]
���������������������������������������������������������������������������������������������������� [fructose_6�]
L�AMP se lie
pr�f�rentiellement � l��tat R.
Un signal
m�tabolique consistant en la diminution de la concentration de l�ATP,
insuffisant pour lever l�inhibition exerc�e sur
Mais
l�amplification de la stimulation de
"� Il existe donc un autre m�canisme activateur.
�
Fructose
2,6�biphosphate :
�
Activateur
allost�rique majeur de
Activit� de

������������������ �� 100��
������ ����������� � �������������������������������� +
Fruct 2,6 di�
������������������ ���� 75�� ����������� �
�������������������������������� ������� Fruct
2,6 di�
������������������ ���� 50��
������������������ ���� 25��
����������������������������������������������������������������������������������������������������������������
������������������ ������ 0
������������������������������ ��� 0,5������������������������������������� 2��������������������� [Fructose 6�]�
(en mM)
Ce n�est pas la
vitesse de r�action qui change, mais l�affinit� de l�enzyme pour son substrat.
"�
��
Vitesse�������������������������������������������� ����������� ����������� Vitesse

![]() ������������������������������ + Fruct 2,6 di�
������������������������������ + Fruct 2,6 di�

 ������
������
������ ���������������������������������������������������������������������� ����������� + Fruct 2,6 di�
������������������
������������������������������
������������������ ����������� ����������� � Fruct 2,6 di�������������������������������� �
Fruct 2,6 di�
![]()
����������������������������������������� [AMP]� (en mM) ������������������������������������������������������������������ [ATP]
"� Augmentation
de l�affinit� de l�enzyme pour son autre activateur allost�rique, l�AMP.
"� Diminution
de l�affinit� de l�enzyme pour son inhibiteur allost�rique, l�ATP.
�
M�tabolisme
assur� par une enzyme fonctionnelle :
�� ATP����������������������������������������������� ���� ADP
 Phosphofructokinase
2 (PFK 2)
Phosphofructokinase
2 (PFK 2)
Fructose_6�������� ���������������������������������������������������������� Fructose_2,6
di�
Fructose 2,6 diphosphatase
���� Pi�������������������������������������������������� ���� H2O

�
Absence
d�activation de
�
Diminution
de l�utilisation cellulaire du glucose
�
Diminution
du pr�l�vement du glucose circulant
�
Augmentation
de la glyc�mie

L�insuline
favorise l�activation de
&
La
diminution de l�activit� du catalyseur de
�
Augmentation
de la glycolyse
�
Augmentation
de l�utilisation cellulaire du glucose
�
Diminution
de la glyc�mie
Les 2 activit�s
enzymatiques distinctes sont port�es par une enzymatique unique bifonctionnelle.
Il s�agit d�une enzyme bifonctionnelle est un dim�re (2 sous�unit�s de 55 kDa),
dont chaque sous�unit� est bifonctionnelle.
La
bifonctionnalit� est d�montr�e par :
-
L�utilisation :
-
Des
agents oxydants :������
"� Diminution de l�activit� kinase, mais l�activit�
phophatase est �pargn�e.
-
Des
agents alkylants (para�mercuribenzoate) :���
"� Augmentation de l�activit� kinase, mais diminution
de l�activit� phophatase.
-
De
l�ADP :�����������
"� Diminution de l�activit� kinase, mais
l�activit� phophatase est �pargn�e.
-
L�application
d�une prot�olyse limit�e (thermolysine, trypsine) :�����������
"� Absence de l�activit� kinase, mais l�activit�
phophatase est �pargn�e.
-
La
d�termination de la s�quence primaire :�������
"� Mise en �vidence de 2 domaines ind�pendants.
�
R�gulation par
phosphorylation�d�phosphorylation des activit�s kinasique�phosphatasique :
AMPc
�
PKA
�
Phosphorylation
d�une s�rine par sous�unit�
�
Diminution de
l�activit� kinasique
&
Augmentation de
l�activit� phosphatase
Activit� kinasique
Activit� phosphatasique

����������������������������������������������������������������� �� Vmax
����������������������������������������������������������������� �� Vmax
������ ������
�Km�������� Km���������������������������������������������������� �� Km (constant)
Inhibition comp�titive
Inhibition non comp�titive
Propri�t�s de
-
Elle
a une stricte sp�cifique par rapport au D_Fructose_6�.
-
Il
n�y a pas d�inhibition par l�ATP, � la diff�rence de

Inhibition comp�titive
Inhibition non comp�titive
Double r�le du citrate :
Il est
l�inhibiteur allost�rique de
 Propri�t� du fructose�2,6 di� :
Propri�t� du fructose�2,6 di� :
R�gulation du
taux du F_2,6 di� :
.Poly
p 4.
Le Pi entra�ne
une augmentation du KInhibiteur du frutcose_6�
�
Lev�e partielle
de l�inhibition exerc�e par la fructose_6�
� L�activation de
cet inhibiteur allost�rique va stimuler la glycolyse.
Le niveau de
phosphorylation va r�gler les activit�s phosphatasiques et kinasique.
Int�r�t d�une r�gulation concert�e dans
les cycles futiles :
![]()
![]()
����������������������������������������� 12������������������������������������������������������ 10
����������������������� A��������������� B������������������������� A��������������� B
![]()
![]() ����������������������������������������� 13������������������������������������������������������ 16
����������������������������������������� 13������������������������������������������������������ 16
������������������������������ �� Flux net�
=� 1���������������������������������� ��
Flux net� =� 6
"� Une modification de 25% des activit�s
enzymatiques induit une augmentation de 500% du flux m�tabolique. Cela permet
une r�gulation tr�s fine des m�tabolismes cellulaires.
R�gulation h�patique de la
glycolyse :
.Poly
p 5.
2
hormones hyperglyc�miantes (adr�naline et glucagon) vont activer la prot�ine
kinase A (PKA) qui va phosphoryler l�enzyme bifonctionnelle :
-
Diminution
de l�activit� kinasique,
-
Augmentation
de l�activit� phosphatasique.
Le fructose_2,6
di� est incapable d�agir comme
inhibiteur allost�rique car sa concentration est trop faible.
������ "� Il participe � une �tape limitante.
La chute de la
vitesse du flux glycolytique permet de pr�server le glucose form� pour le
relarguer dans la circulation.
.Poly
p 5.
Le r�cepteur insuline entra�ne une
cascade de signaux � kinasiques � et l�activation de certaines
activit�s enzymatiques dont la phosphatase.
-
L�insuline
r�gule l�activit� phosphodiest�rase formant l�AMP non cyclique incapable
d�activer
-
Elle
s�oppose au glucagon et l�adr�naline :
-
En
diminuant le taux de l�AMPc.
En
d�phosphorylant l�enzyme bifonctionnelle, son activit� phosphatasique est
diminu�e.
Des
fortes concentrations [F_2,6 di�] stimulent
"� L�insuline a
un r�le hyperglyc�miant car elle favorise l�utilisation du glucose.
R�gulation h�patique de la
glycolyse :
.Poly
p 5.
Structure primaire des enzymes
bifonctionnelles dans le foie et le c�ur :
.Poly
p 5.
D�pendance du flux glycolytique
vis���vis de quelques enzymes :
 ������ Flux glycolytique :
������ Flux glycolytique :
������������������������������ 0,09
����������������������������������������������������������������� Glucokinase
������������������������������ 0,06
������������������������������ 0,04
����������������������������������������������������� ����������� PFK
1
������������������������������ 0,02����
������ ���������������������������������������������� ���������������������������������������������������������� Phosphokinase
isom�rase
������������������������������ ���� 0
����������������������������������������������������� ��� 1����������������� 2��������� ������
3�� ���� Quantit� d�enzyme ajout�e
Le facteur
limitant de la glycolyse (dans le foie) est la 1�re r�action,
c'est���dire la transformation du glucose en glucose_6�.
Conditions exp�rimentales :
-
Homog�nat
de tissu h�patique (quantit� fixe),
-
Additions
de concentrations croissantes d�enzymes purifi�es,
-
Mesure
de la quantit� de fructose_1,6 di� form�
Plus on ajoute
de la glucokinase, plus on stimule la transformation du glucose en fructose_1,6
di�.
� R�gulation
de pyruvate kinase (PK) :
� Les isoenzymes de
On trouve 3
isoenzymes :������������� M������� localis�e
dans le muscle et le cerveau,
����������������������������������������������������� A�������� localis�e
dans les tissus adipeux,
����������������������������������������������������� L��������� localis�e
dans le foie et le rein.
Seule
l�isoenzyme L est soumise � r�gulations allost�rique et par
phosphorylation.
� R�gulation
allost�rique :
�
Inhibiton
allost�rique (ATP, NADH, citrate, alanine) :

Le m�canisme de r�trocontr�le n�gatif
par l�alanine est tr�s important dans la p�riode de je�ne.
Cycle glucose � alanine :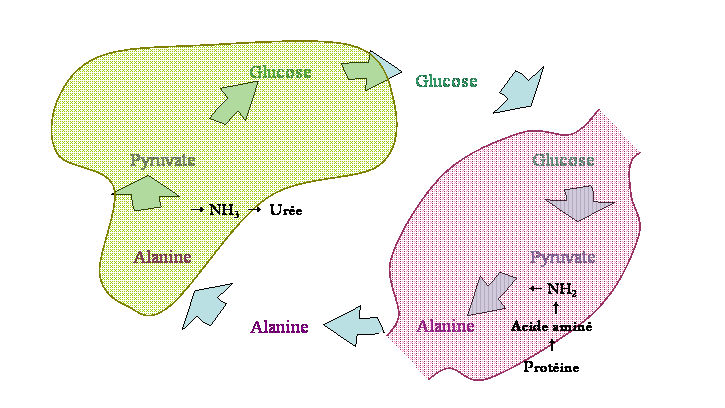
L�alanine va
servie de substrat dans la n�oglucogen�se et inhiber fortement la glycolyse
h�patique
�
Activation
allost�rique (ADP, fructose�1,6 di�) :
Vitesse
 ���������������������������������������������������������������������������������������� +
Fructose_1,6 di�
���������������������������������������������������������������������������������������� +
Fructose_1,6 di�
���������������������������������������������������������������������������������������� �
Fructose_1,6 di�
����������������������������������������������������������������������������� "
Augmentation de l�activit� de l�enzyme
���������������������������������������������������������������������������������������� [
PEP ]
Le
fructose_1,6 di� permet une activation par
anticipation.
� R�gulation par
phosphorylation�d�phosphorylation :
 R�gulation de
R�gulation de
.Poly
p 4.
Vitesse

Pyruvate kinase
d�phosphoryl�e
Pyruvate kinase phosphoryl�e
���������������������������������������������������������������������������������������� [
PEP ]
"� L�activation
fait augmenter l�affinit� pour le substrat.
-
La
forme d�phosphoryl�e est plus sensible aux activateurs allost�riques comme le
fructose_1,6 di�,
-
La
forme phosphoryl�e est plus sensible aux inhibiteurs allost�riques comme
l�alanine.
-
La
phophatase est stimul�e par l�insuline,
-
Le
fructose_1,6 di� freine la
phosphorylation de
� R�gulation
� long terme des enzymes cl�s :
Elle se fait sur
la glucokinase,
Influence de l�alimentation :
|
|
Glucokinase |
PFK 1 |
PK |
|
Alimentation glucidique |
& Augmentation |
& Augmentation |
& Augmentation |
|
Je�ne glucidique |
(( Forte
baisse |
( Baisse |
( Baisse |
R�le des hormones dans la r�gulation
transcriptionnelle des enzymes cl�s de la glycolyse :
|
|
Glucokinase |
PFK 1 |
PK |
Enzyme bifonctionnelle |
|
Glucagon |
( (induction
par l�insuline) |
? |
( (induction
par l�insuline et le glucose) |
( |
|
Insuline |
& |
& |
& (+
glucose) |
Restauration de l�activit� |
|
Diab�te |
(( |
( |
( |
( |
N. B :
La glucokinase
des cellules pancr�atiques est insensible � l�insuline.
La glucokinase
pancr�atique est un d�tecteur de glucose.
�
Contr�le du flux
glycolytique
�
Contr�le du
ratio ATP /ADP responsable de la synth�se d�insuline.
v Rappels :
� Structure
du glycog�ne :
Le glycog�ne
constitue la principale forme de stockage des glucides chez les animaux.
R�serves glucidique chez l�homme adulte
normal :
-
Glycog�ne
h�patique :���� ����������� 4%
du poids frais������� soit
-
Glycog�ne musculaire
:�� ����������� 0,7%
du poids frais���� soit
-
Glycog�ne
extracellulaire :��������� 0,1% du poids frais���� soit
Contenu h�patique en glycog�ne :
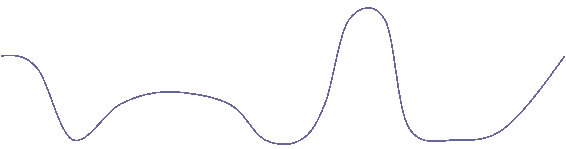
![]() ������������������������������ ����������� Variation nycth�m�rale du contenu
h�patique en glycog�ne
������������������������������ ����������� Variation nycth�m�rale du contenu
h�patique en glycog�ne
������ (� partir d�une population am�ricaine
normale)
![]() 8H�������������� 12H����������������� 16H����������������� 20H����������������� 24H����������������� 4H������������������� 8H�������
8H�������������� 12H����������������� 16H����������������� 20H����������������� 24H����������������� 4H������������������� 8H�������
R�serves �nerg�tiques d�un homme normal
(en kCal) :
-
Glycog�ne
h�patique :����� ������ 280
-
Glycog�ne
musculaire :���� ������ 480
-
Glycose
extracellulaire :��� �������� 80
-
Lipides :��������������������������� 135 000
-
Prot�ines :����������������������� � 24 000
Il existe 2 types de liaison
glucosidique :

-
 Liaison a_1,4 :
Liaison a_1,4 :

-
Liaison
a_1,6 :
La structure
ramifi�e du glycog�ne est due � ses 2 types de liaison.
Le glycog�ne est
stock� dans le cytosol sous forme de granules. Ces derni�res pr�sentent un
diam�tre de 100 � 400 � et contient
jusqu�� 120 000 unit�s de glucose.
Le PM du glycog�ne va jusqu�� 2.107 Da.
L�int�r�t
physiologique du glycog�ne est sa d�gradation rapide.
Mais alors,
pourquoi stocker le glucose pour les r�serves �nerg�tiques,
alors que l�on a
beaucoup plus de lipides ?
-
Mobilisation
plus rapide du glycog�ne dans le muscle,
-
Pas
de m�tabolisme des AG en ana�robiose,
-
Pas
de conversion des AG en glucose.
"� Le m�tabolisme
des lipides ne peut assurer seul le maintien de la glyc�mie.
� R�action
de la glycog�nolyse :
Phosphorylase du glycog�ne
![]() (glucose)N� +� Pi��������������������������������������������������� (glucose)N+1� +�
Glucose_1�
(glucose)N� +� Pi��������������������������������������������������� (glucose)N+1� +�
Glucose_1�
Dans
la cellule :��������� [Pi] / [G_I�]�
=� 100
������������������ "� R�action est
pratiquement irr�versible.
DG = 0 ���������� quand� [Pi] / [G_I�]�
�� 3,5
.Poly
p 6.
La phosphorylase
catalyse la coupure des liaisons a_1,4 du
glycog�ne des extr�mit�s non r�ductrices (= absence du C1�OH)
Il ne s�agit pas d�une hydrolyse, mais
d�une phosphoralyse.
L�action de la
phosphorylase du glycog�ne s�arr�te au voisinage dans les liaisons a_1,6 (quand il
reste 4 r�sidus glucose avant une ramification)
D�autres enzymes
interviennent :
-
a_1,4 glucanne
transf�rase :�� Transfert des 3
unit�s sur la cha�ne lin�aire,
-
a_1,6 glucosidase :�� Elimination du glucose li� � la cha�ne en a_1,6.
Ce sont des
enzymes bifonctionnelles. Elles sont dites des enzymes d�branchantes.
D�gradation du
glycog�ne :
-
90%
en glucose_1�,
-
10%
en glucose.
v R�gulation des enzymes de
la glycog�nolyse :
� Phosphorylase
du glucog�ne musculaire :
.Poly
p 6.
La
phosphorylase du glycog�ne est un dim�re constitu� de 2 sous�unit�s.
Le site de
fixation du glycog�ne peut �tre loin du site catalytique. La distance entre ces
2 sites correspond � 4 unit�s de glucose.
� R�gulation allost�rique de la
phosphorylase b :
.Poly
p 6.
La
phosphorylase b correspond � l��tat
d�phosphoryl� de la phosphorylase du glycog�ne.
� R�gulation par
phosphorylation�d�phosphorylation :
.Poly
p 7.
����������������������������������������� Phosphatase
![]() Phosphorylase a�������������������������������� ����
Phosphorylase b
Phosphorylase a�������������������������������� ����
Phosphorylase b
������������������ La phosphatase kinase
phosphoryle les r�sidus S�rine.
Il faut que la
phosphorylase b soit sous sa forme T pour qu�elle soit phosphoryl�e. Il y a, en
plus, des r�gulations allost�riques.
La phosphorylase
a phosphoryl�e est tr�s sensible � l�AMP.
� R�gulation de la phosphorylation
(phosphorylase kinase) :
La phosphorylase kinase phosphoryle les
r�sidus a
et b.
Par
cette cascade, il y a une forte amplification de
.Poly
p 7.
La
phosphorylase kinase est un h�t�rot�tram�re�
(4 sous�unit�s)
.Poly
p 7.
La sous�unit� d est la calmoduline (CaM) :
Sa fonction est
de fixer le Ca2+ de
l�organisme ; elle donc tr�s importante.
Elle est
constitu�e de 148 acides amin�s et est pr�sente dans toutes les cellules de
l�organisme.
 ������������������������������ Ca2+ ������������������������������������������������� �Ca2+
������������������������������ Ca2+ ������������������������������������������������� �Ca2+
������������������������������ Ca2+ ������������������������������������������������� �Ca2+
Les
4 ions Ca2+ viennent se fixer.
Le
Ca2+ qui se lie induit des
changements conformationnels :
-
D�voilement
d�une plage hydrophobe riche en M�tionine,
-
Formation
de liaison de forte affinit� avec le domaine de liaison � la calmoduline de certaines
prot�ines,
-
Modulation
de l�activit� de ces prot�ines.
La sous�unit� g porte le site
catalytique qui permet la phosphorylation de certains substrats.
Fixation du Ca2+ fix� avec la
sous�unit� d
�
Modification de
l�activit� de la sous�unit� g
�
Les r�sidus
S�rine des sous�unit�s a et b deviennent
accessibles
�
La prot�ine
kinase A peut alors phosphoryler la sous�unit� b
�
Autre changement
conformationnel
�
Phosphorylation
de la sous�unit� a
�
D�voilement plus
important de
�
Inhibition
de l�activit� de la phosphatase kinase
�� L�action des phosphatases (PP1) qui
d�phosphorylent le r�sidu S�rine entra�ne l�inhibition de l�activit� de la
phosphatase kinase.
A Noter :
La
structure de la calmoduline est similaire � celle de la troponine C (70%
d�homologie)
"� L�activation de la glycolyse et l�induction
de la contraction musculaire sont r�alis�es par des prot�ines similaires liant
le Ca2+.
�� Il y a
synchronisation des 2 processus.
� R�gulation de la d�phosphorylation
(PP1) :
.Poly
p 7.
�
Activation
:
Elle doit �tre
phosphoryl�e sur au moins 1 des 2 sites. Elle est phosphoryl�e par la prot�ine
kinase A sous l�action de l�insuline.
Mais il existe
un 2�me mode de phosphorylation par
Elle conduit �
une double phosphorylation qui entra�ne des modifications
�
�
Inactivation de
&
Activation de la
glycog�nolyse
�
Inactivation
de
.Poly
p 8.
Elle se fait par
l�action d�une prot�ine inhibitrice qui fixe avec une forte affinit� la
sous�unit� catalytique quand cette prot�ine est phosphoryl�e.
�
�
Consid�rations
g�n�rales sur les (Ser/Thr) phosphatases :
Il existe
beaucoup plus de Ser/Thr kinases (pour la phosphorylation) que de Ser/Thr
phosphatases (pour la d�phosphorylation) diff�rentes chez les vert�br�s.
Chez l�homme, le
rapport kinases/phosphatases = 20
"� L��volution
s�accompagne d�une diversit� croissante des Ser/Thr kinases mais pas des
Ser/Thr phosphatases (dont le nombre reste � peu pr�s constant au cours de
l��volution)
Comment assurer
une sp�cificit� d�action de ces phosphatases ?
Il y a peu de
diversit� des sous�unit�s catalytiques mais chaque sous�unit� catalytique est
capable de r�agir avec de multiples sous�unit�s r�gulatrices.
Exemple :
������
"� G�n�ration
d�holoenzymes diff�rentes avec des sp�cificit�s d�action et des localisations
diff�rentes.
�
Ciblage
subcellulaire des phosphatases :
Le contr�le
pr�cis du large spectre d�activit� des phosphatases est obtenu en restreignant
l�action de ces enzymes in vivo.
Ce contr�le est
exerc� par des prot�ines de nature vari�e qui, en interagissant � la fois avec
d�autres mol�cules et avec des phosphatases, vont se comporter comme des sous�unit�s
de ciblage (targeting subunit) des phosphatases.
La phosphatase
ne pourra d�phosphoryler que les substrats situ�s � proximit� imm�diate de la
sous�unit� de ciblage sur laquelle elle est fix�e.
Ces sous�unit�s
de ciblage contr�lent l�activit� catalytique des phosphatases.
Ciblage subcellulaire :
.Poly
p 8.
1)
En
confinant l�enzyme dans les zones pr�cises de la cellule.
2)
En
modifiant allost�riquement les propri�t�s catalytiques et/ou r�gulatrices de
l�enzyme.
"� Ces 2 effets �tant r�versibles.
D Il n�y a pas de r�gulation par le Ca2+ de la phosphorylase kinase,
contrairement �
� Phosphorylase
du glucog�ne h�patique :
Elle
pr�sente une structure diff�rente de la phosphorylase musculaire mais a une
r�gulation quasi identique :
-
R�gulation
par phosphorylation � d�phosphorylation,
-
R�gulation
allost�rique :
-
De
la phosphorylase b (comme avec la phosphorylase musculaire),
-
De
la phosphorylase phosphatase.

Phosphorylase a������������������������������������������������������� ����� Phosphorylase b
����������������������������������������������������� Phosphorylase
phosphatase
������ Inhibition
������������������������������ AMP������������������������������������������������������������������������� Glucose
����������������������������������������������������������������� Activations
����������������������������������������� Insuline��������������������� Glucocortico�des (cortisol)
L�action inhibitrice est majeure par
rapport aux autres actions.
v Rappels :
� R�actions
de la glycogen�se :
.Poly
p 9.
� M�canisme
de ramification du glycog�ne :
.Poly
p 9.
L�enzyme
branchante transf�re une partie du glucose de la cha�ne lat�rale sur la cha�ne
lin�aire en formant une liaison a_1,6.
� La
glycog�nine :
Il s�agit du
� primer � de la synth�se du glycog�ne, en permettant l�initiation de
la glycog�nogen�se.
C�est un
polypeptide de 332 acides amin�s.

����������������������������������������������������������������� 8
(UDP_glucose)
������ Glycosylation
spontan�e
����������������������������������������������������������������� 8
UDP
����������������������������������������������������������������� n
(UDP_glucose)
Glycog�ne synth�tase et
������ Enzymes
d�branchantes������������������� n UDP
v R�gulation de la glycog�ne
synth�tase :
� Par
phosphorylation :
.Poly
p 9.
-
La
glycog�ne synth�tase (GS) est active quand elle est d�phosphoryl�e :� GS a.
-
Quand
elle est phosphoryl�e, elle est inactive :�
GS b.
-
� Sites de phosphorylation
multiples dur
.Poly
p 10.
Tous les sites
de phosphorylation n�ont pas le m�me poids. Il existe :
-
Des
sites primaires,
-
Des
sites secondaires.
Les sites IAIRES entra�nent
aucune modification apparente de l�activit� de
"� Inactivation
de
Diff�rences
entre
-
La phosphorylation entra�ne la baisse de
la vitesse max.
-
La phosphorylation entra�ne la baisse
d�affinit� pour l�UDP�glucose.
Il y a aussi une
absence de 2 sites de phosphorylation apr
� Par
phosphorylation :
.Poly
p 10.
N.B :
L�insuline
stimule
� Par
contr�le allost�rique :
.Poly
p 10.
Seule la forme b
(phosphoryl�e) est contr�l�e allost�riquement.

La concentration
en glucose_6�, dans le
muscle, est de 0,2 �
"� La glycog�ne
synth�tase b in vivo est quasiment
inactive.
�� L�activit� de
v R�gulation coordon�e de la
glycog�nolyse et de la glycog�nogen�se :
.Poly
p 10.
La
mobilisation des r�serves glucidiques entra�ne une augmentation de la
glycog�nolyse et donc une inhibition de la glycog�nogen�se par les enzymes.
On observe le
ph�nom�ne inverse avec l�insuline :
������������������ Glycog�nogen�se favoris�e,
������������������ Glycog�nolyse inhib�e.
v Action glycog�nogen�se du
glucose :
.Poly
p 11.
� Inactivation
de la phosphorylase a et activation de
Dans le foie, la
phosphorylase a joue le r�le de la glucokinase :�� D�tecteur de glucose.
Une
fois le glucose fix� sur la phosphorylase a :
-
Inhibition
comp�titive du glucose,
-
Fixation
sur le site allost�rique.
" Changement conformationnel : � Meilleure accessibilit� des r�sidus Ser�� pour les phosphatases.
Les phosphatases
acc�dent � leur substrat��� "�
D�phosphorylation de la phosphorylase a.
En m�me temps de
l�inactivation de la phosphatase a :�������
"�
�� Il n�y a pas d�instauration simultan�e de la
synth�se et de la d�gradation du glycog�ne.
L�activation
de
Certains
analogues non m�tabolisables du glucose entra�nent une diminution d�activit�
sur la phosphatase mais n�ont pas d�action sur
Le 2_d�soxyglucose agit comme le
glucose :�� Baisse d�activit� de la
phosphatase,
���������������������������������������������������������������������� Augmentation
d�activit� de
"� Le glucose_6�
est requis.
L�inhibiteur
de la glucokinase entra�ne une baisse de
Le
glucose_6� stimule de la
d�phosphorylation de
Important :� L�inactivation de la phosphatase a est un pr�
requis pour l�activation de
Le glucose
augmente la transcription des g�nes impliqu�s dans son m�tabolisme.
� Augmentation
de l�expression de GLUT�2 :
Le
glucose cr�e une augmentation de l�expression de GLUT�2.
Les effets
transcriptionnels du glucose sont m�di�s par le xylulose_5� (interm�diaires du cycle des
pentoses�phosphates)
� R�gulation
des voies de signalisation :
Le
glucose activerait certaines voies de signalisation.
L�activation
de
� Contr�le
de la localisation subcellulaire de certaines enzymes glycog�nogen�ses :
Le glucose
contr�le la localisation subcellulaire de certaines enzymes glycog�nogen�ses
(glucokinase, GS) et de la glycog�nine.
"� Cr�ation
d�un complexe glycog�nogen�se regroupant la glycokinase, GS et glycog�nine
associ� aux microfilaments d�actine.
v Rappels sur les r�actions
de la glucon�ogen�se :
Sch�ma simplifi� des voies de la
glucon�ogen�se :
.Poly
p 12.
La
glucon�ogen�se se d�roule principalement dans le tissu h�patique et le rein.
2 cycles impliqu�s dans la
glucon�ogen�se h�patique :
.Poly
p 12.
N�oglucogen�se :
.Poly
p 12.
La
glucon�ogen�se est un gaspillage �nerg�tique indispensable.
����������������������������������������� +
6 ATP
![]() 2 Lactate������������������������������� 1 Glucose
2 Lactate������������������������������� 1 Glucose
Mais
l�ATP requis est fourni par oxydation des acides gras (AG)
Les conditions
m�taboliques requises pour l�initiation de la glucon�ogen�se correspondent aux
conditions, elles�m�me, correspondant � une libert� accrue d�AG dans la circulation.
"� Oxydation
mitochondriale h�patique :
����������������������������������������� "� Corps c�toniques,
����������������������������������������� "� ATP (glucose)
Voies de la glucon�ogen�se :
.Poly
p 13.
������������������ GOT =���������� Glutamate
Oxaloac�tate Transaminase
������������������ MDH =��������� Malate
D�Hydrog�nase
������������������ LDH =���������� Lactate
D�Hydrog�nase
R�gulation transcriptionnelle
coordon�e de la glycolyse et de la glucon�ogen�se :
.Poly
p 13.
v R�gulation des activit�s
des enzymes de la glucon�ogen�se :
�
C�est une enzyme
mitochondriale (chez les mammif�res) ou cytosolique (chez les levures et
bact�ries)
Chez les
mammif�res :
C�est
une prot�ine homo�t�tram�rique, avec 4 cha�nes identiques de 1178 acides
amin�s, et un PM de 4 x 130 kDa (= 520 kDa)
Elle
est r�gul�e par l�ac�tyl_CoA, comme la quasi�totalit� des carboxylases.
� Activation allost�rique :
�
Par
l�ac�tyl_CoA :
Chez les
mammif�res.
Enzyme_biotine� +� ATP� +� HCO3�
![]() + Ac�tyl_CoA
+ Ac�tyl_CoA
+ Mg2+
Enzyme_biotine�CO2� +� ADP� +� Pi
![]() + Pyruvate
+ Pyruvate
Enzyme_biotine� +� OAA
La
biotine permet la catalyse.
Par contre, chez
la levure, l�activation de
������������������������������ Vitesse������������ ����������� +
Ac�tyl_CoA
 ������������������ ������ Vmax
������������������ ������ Vmax
� � Ac�tyl_CoA
���������������������������������������������������������������������������������������������������� [HCO3�]
����������������������������������������� ���� Km ����� Km
"� Implication
dans l�autor�gulation du m�tabolisme interm�diaire.
-
Une
charge �nerg�tique cr�e un ralentissement du cycle de Krebs et donc une
augmentation de la concentration de l�ac�tyl_CoA.
"� Activation
de la pyruvate carboxylase (PC) et augmentation de la synth�se du glucose.
-
Un
d�ficit en OAA entra�ne augmentation de la concentration de l�ac�tyl_CoA.
"� Activation
de la synth�se d�OAA et augmentation du cycle de Krebs.
-
La
b_oxydation
(en p�riode de je�ne) entra�ne augmentation de la concentration de
l�ac�tyl_CoA.
"� Activation
de la pyruvate carboxylase (PC) et inhibition de la pyruvate d�shydrog�nase
(PDH)
�
Par l�ATP
:
� Inhibition allost�rique par
l�ADP :
� La
fructose�1,6 diphosphatase :
C�est une enzyme
t�tram�rique.
Il n�existe pas
de coop�rativit� vis���vis du substrat (fructose_1,6 di�)
������������������ "� Comportement
mickaelien vis���vis du sbstrat.
Elle a un comportement allost�rique vis���vis des
effecteurs allost�riques.
Il y a la
n�cessit� de Mn2+ et Zn2+ pour la
catalyse.
������������������������������ Vitesse������������
 ������������������ ������ Vmax
������������������ ������ Vmax
���������������������������������������������������������������������������������������� [Fructose_1,6
di�]
� Activation
allost�rique :
Elle
se fait par l�ATP, le NAD r�duit et le citrate.
Elle
favorise la transformation allost�rique de l�enzyme vers sa forme catalytique.
De plus, il y a une stabilisation de la
forme R (active) favoris�e par le substrat (fructose_1,6 di�) et le fructose.
� Inhibition
allost�rique :
Elle se fait par
l�AMP (et non l�AMPC) et le
fructose_2,6 di�.
�
L�AMP
:
Elle
favorise la transition de la forme R vers la forme T (moins active)
L�effet
est variable suivant les esp�ces.
L�AMP
est efficace chez les mammif�res, mais sa concentration varie peu.
������������������������������ Vitesse������������
 ������������������ ������ Vmax
������������������ ������ Vmax
���������������������������������������������������������������������������������������� [AMP]
�
Le
fructose�2,6 di� :
������������������������������ Vitesse������������
 ������������������ ������ Vmax
������������������ ������ Vmax
C�est
l�inhibiteur allost�rique majeur.
���������������������������������������������������������������������������������������� [AMP]
Le fructose_2,6
di� est � la fois activateur de la
glycolyse et inhibiteur de la glucon�ogen�se.
Cette
double r�gulation par la m�me mol�cule fait que la glycolyse et glucon�ogen�se
ne peuvent coexister.
L�inhibition
allost�rique par le fructose_2,6 di� est due
� :
-
L�inhibition
comp�titive par rapport au substrat (analogie avec le fructose_1,6 di�)
-
L�induction
d�une coop�rative n�gative pour la fixation du substrat,
-
Le
renforcement de l�inhibition induite par l�AMP, par augmentation de l�affinit�
pour l�AMP :
"� Le fructose_2,6�
agit comme un effecteur allost�rique h�t�rotrope
������������������������������ Vitesse������������
 ������������������ ������ Vmax
������������������ ������ Vmax
����������������������������������������������������� � � fructose_2,6 di�
����������������������������������������������������� ��� + fructose_2,6 di�
���������������������������������������������������������������������������������������� [AMP]
-
La
fragilisation (avec l�AMP) de la liaison prot�ine�m�taux (MN2+ et Zn2+) dans les sites
catalytiques, cr�ant une baisse d�activit�.
R�gulation indirecte par l�AMPc de la
fructose_1,6 diphosphatase :
![]()
![]() ������ ����������������������� Adr�naline���������������������������������������������������� Glucagon
������ ����������������������� Adr�naline���������������������������������������������������� Glucagon
( [AMPc]
”
Phosphorylation
de
”
( [Fructose_2,6
di�]
”
Restauration
de l�activit� du fructose_1,6 diphosphatase
”
Baisse
de la glycolyse
&
Augmentation
de la glycon�ogen�se
� La
glucose�6 phosphatase :
� Structure de l�enzyme :
L�une des
principales fonctions h�patiques est la fourniture de glucose.
La
glucose_6 phosphatase joue un r�le essentiel dans l�hom�ostasie glucidique
car :
![]() ������������������������������ Glucon�ogen�se
������������������������������ Glucon�ogen�se
����������������������������������������������������������������������������� Glucose_6�
������������������������������ Glycog�nolyse
Le glucose_6 � doit �tre
hydrolys� par la glucose_6 phosphatase pour �tre lib�r� dans la circulation.
� Localisation intracellulaire
de la glucose�6 phosphatase :
Il y a un
subfractionnement cellulaire : elle est associ�e au RE. C�est un caract�re
la distinguant de la plupart des phosphatases qui sont plut�t cytosoliques.
Ses propri�t�s
d�pendent de l�int�grit� des membranes des lysosomes (majoritairement de
RE) :
-
Microsomes
intacts�� "� Activit� phosphatasique 10 fois plus �lev�e
avec le glycose_6� qu�avec le
mannose_6�,
-
Traitement des microsomes
par des d�tergents�� "� Activit� phosphatasique identique mais qui
porte une sp�cificit� au glycose.
"� La glucose_6 phosphatase isol�e serait une
phosphatase relativement non sp�cifique.
�� Sa sp�cifique vis���vis du glucose dans la
cellule est due � sa localisation subcellulaire.
Complexe multienzymatique :
.Poly
p 13.
Le complexe est constitu� par T1, T2 et T3.
Il sert � la d�phosphorylation du
glucose.
GLUT_2 se charge de la lib�ration du
glucose.
v R�gulation de la synth�se
des enzymes cl�s de la n�oglucogen�se :
� R�gulation
� court terme de la glucose�6 phosphatase :
Le Km vis���vis
du glucose_6� vaut 2 �
"� L�action de
l�enzyme va d�pendre essentiellement de la concentration en substrat.
Le
glucose :
C�est
l�inhibiteur comp�titif in vitro,
mais le Ki =
������������������ "� Importance physiologique mineure ?
Le Pi :
C�est
l�inhibiteur non comp�titif dans le cas des microsomes intacts, et un
inhibiteur comp�titif dans le cas d�ajout de d�tergents.
"� Divergence
interpr�t�e comme indicateur de la pr�sence d�un transporteur de Pi dans les
microsomes.
� R�gulation allost�rique de la
glucose�6 phosphatase :
L�inhibition
se fait par le fructose_1�, mais sa
concentration physiologique est faible et n�entra�ne qu�une petite inhibition.
Elle
se fait aussi par l�a_c�toglutarate et les AG :
-
Tous
les acyl_CoA����������������������� "� Inhibition de la glucose_6 phosphatase,
-
Les
AG insatur�s (arachidonate)� "� Aussi inhibition,
-
Les
AG satur�s����� "� Pas d�effet.
Il y a des
effets inhibiteurs pour des concentrations faibles, mais ces effets sont nuls,
voire activateurs, pour des concentrations �lev�es.
� R�gulation
� long terme :
R�gulation
transcriptionnelle coordonn�e de la glycolyse et de la glucon�ogen�se :
.Poly
p 13.
������������������ "� R�gulation hormonale.
� D�ficience de l�activit�
glucose�6 phosphatase :
Une telle
d�ficience entra�ne la maladie de Von Gierke, ou Glycogen Storage Disease (GSD)
de type 1.
-
Dues � l�accumulation de glycog�ne
![]() H�patom�galie
H�patom�galie
-
N�phrom�galie
-
Hypoglyc�mie
-
Acidose
lactique
v Rappels de la
r�action :
Les 5 r�actions du complexe
multienzymatique de
.Poly
p 14.
Chez
les bact�ries, ces enzymes ont une localisation cytosolique, ce qui les rend
plus sensibles aux ars�niates que les enzymes humaines.
"� Les ars�niates ont �t� utilis�s comme � antibiotiques �
au 19�me si�cle. Ils sont rapidement abandonn�s en raison des
effets� secondaires.
v Organisation structurale du
complexe PDH d�E. coli :
PM = 4600 kDa.
-
E2 : 24
sous�unit�s associ�es en trim�res localis�s au coin d�un cube ;
-
E1 : 24
sous�unit�s PDH formant des dim�res dispos�s au centre de chacune des ar�tes du
cube ;
-
E3 : 12
sous�unit�s de dihydrolypoyl d�shydrog�nase formant des dim�res dispos�s au
centre de chacune des 6 faces.
Complexe
multienzymatique PDH� d�eucaryote :
-
30
dim�res E1,
-
6
dim�res E3,
�� Ils entourent un noyau central de 60
monom�res E2.
� Int�r�t
des complexes multienzymatiques :
Ils
permettent l�accroissement de l�efficacit� catalytique car :
j La distance que
doivent parcourir les substrats entre les sites actifs est minimis�e.
’ Augmentation de
la vitesse de r�action.
k Les
interm�diaires m�taboliques sont guid�s d�une enzyme � l�autre (�vitant aussi
qu�ils soient utilis�s dans des r�actions annexes)
l Les r�actions
catalys�es par ces complexes multienzymatiques peuvent �tre r�gul�es de fa�on
coordonn�e.
v R�gulation de
� R�gulation
allost�rique :


� R�gulation
par phosphorylation�d�phosphorylation :
.Poly
p 14.
R�gulation des activit�s PDH kinase et
PDH phosphatase :
.Poly
p 14.
-
La
kinase est insensible � l�AMPc ;
-
L�activit�
phosphatasique est stimul�e par l�insuline ;
-
Le
CoASH et le NAD+ activent la
kinase ;
-
La
phosphatase est d�pendante du Ca2+ ;
-
L�ac�tyl_CoA
joue un r�le central dans la r�gulation.
������ Glucose
�
Glucon�ogen�se
�
������� �OAA
 PC������������� �
PC������������� �
����� Pyruvate
PDH���������� ������ m� CO2
�� Ac�tyl_CoA
�
Cycle
de Krebs
�
����� Energie
v Rappels des r�actions et
identification des �tapes limitantes :
"� Caract�re amphibolique du cycle de Krebs
(anabolique et catabolique)
Identification des �tapes
limitantes :
����������������������������������������������������� Citrate
synthase
-
![]() OAA + Ac�tyl_CoA������������������������������������������� Citrate
OAA + Ac�tyl_CoA������������������������������������������� Citrate
������������������������������ �� Citrate synthase
-
![]() Isocitrate������������������������������������� a_C�toglutarate
Isocitrate������������������������������������� a_C�toglutarate
����������������������������������������� a_C�toglutarate d�shydrog�nase
-
![]() a_C�toglutarate������������������������������������������������� �� Succinyl_CoA
a_C�toglutarate������������������������������������������������� �� Succinyl_CoA
Ces r�actions sont
exergoniques :� DG < 0
v R�gulation :
� Disponibilit�
en substrats :
Dans les
mitochondries, l�ac�tyl_CoA et l�OAA sont en concentrations non saturantes pour
la citrate synth�tase.
PDH� (pyruvate d�shydrog�nase)������ "������� Ac�tyl_CoA
MDH� (malate d�shydrog�nase)�������� "������� OAA
La concentration
en OAA d�pend du rapport [NADH]/[NAD+]
![]()
![]()
![]()
![]() Malate�
+� NAD+������������������������������� OAA� +� NADH
Malate�
+� NAD+������������������������������� OAA� +� NADH

Passage d�une faible activit� � une
activit� intense :
-
Diminution
de [NADH]�� = R�oxydation par la cha�ne
respiratoire ;
-
Augmentation
de [NADH]�� = Loi d�action de masse ;
-
Augmentation
de la synth�se de citrate ;
-
Diminution
de [Citrate]�� = Utilisation plus
importante que la synth�se ;
-
Diminution
de l�inhibition exerc�e par la citrate sur la citrate synth�tase
"� Augmentation de l�activit� de la citrate
synthase.
-
Augmentation
de l�activit� a_c�toglutarate d�shydrog�nase�����
= Lev�e de l�inhibition exerc�e par le
NADH et le succinyl_CoA
Passage d�une activit� intense � une
faible activit� :
-
Ph�nom�nes
inverses initi�s par l�augmentation des concentrations en NADH et ATP.
Passage d�une activit� intense � une
faible activit� :
.Poly
p 15.
-
ADP :� Activateur allost�rique de l�isocitrate
d�shydrog�nase (= diminution du Km pour l�isocitrate)
-
ATP :� Inhibiteur allost�rique de l�isocitrate
d�shydrog�nase
-
Ca2+ :� 2 r�les distincts :
-
�Augmentation de
-
Activateur
allost�rique de l�isocitrate d�shydrog�nase et de l�aCG
d�shydrog�nase.
�� Dans le muscle, il y a un m�me signal pour
stimuler la contraction musculaire et une augmentation de la synth�se d�ATP.
v Rappel des r�serves
�nerg�tiques et �volution de la glyc�mie :
R�serves �nerg�tiques d�un homme
normal :
.Poly
p 16.
Evolution des concentrations
plasmatiques :
.Poly
p 16.
Quand
il y a une baisse de la glyc�mie, il y a la mise en place des corps c�toniques
qui peuvent �tre utilis�s par de nombreux organes.
Le taux
Insuline/Glucagon r�gule le m�canisme glucidique.
v Les m�canismes impliqu�s
dans la conversion du foie lipog�ne en foie glucog�ne :
� Caract�re
m�tabolique du tissu h�patique :
Foie
� aliment� �
Glycog�nique
Glycolytique
Lipog�nique
Foie � �
jeun �
Glycog�nolytique
Glucon�og�nique
C�tog�nique
Prot�olytique
�
Mise en r�serve
des calories
�
Mobilisation des
r�serves calorifiques
� R�gulation
allost�rique :
Contr�le du m�tabolisme h�patique par
les effecteurs allost�riques (alimentation normale) :
.Poly
p 17.
Contr�le du m�tabolisme h�patique par
les effecteurs allost�riques au cours du je�ne :
.Poly
p 17.
" M�canisme du glucose
orient� vers la glucon�ogen�se.
� R�gulation
des activit�s enzymatiques :
R�gulation des
activit�s enzymatiques (foie � lipog�ne �) :
.Poly p 17.
R�gulation des
activit�s enzymatiques (foie � glucog�ne �) :
.Poly
p 17.
� R�gulation
par induction de la synth�se prot�ique :
Enzymes inductibles dans le foie
nourri :
.Poly
p 18.
" Augmentation
importante d�acides gras.
Enzymes inductibles dans le foie �
jeun :
.Poly
p 18.
" Glucon�ogen�se
h�patique �
Synth�se de glucose.
v Diab�te
insulino�d�pendant :
Pathologies associ�es au diab�te :
-
Hypertension,
-
Ath�roscl�rose,
-
N�phroscl�rose,
glom�ruloscl�rose, art�rioscl�rose, pyclon�phrite,
-
Neuropathie
p�riph�rique,
-
R�tinopathie,
cataracte, glaucomie,
-
Infarctus
du myocarde,
-
Pertes
de cellules pancr�atiques,
-
Ath�roscl�rose
p�riph�rique,
-
Microangiopathie,
accidents vasculaires c�r�braux, h�morragie, etc.
�� Maladies graves.
Le diab�te est une maladie multifonctionnelle.

Masse des
cellules � ����������� j�� k
b
pancr�atiques :��� ������������������ ��� l
���������������������������������������������������� ���� m
������������������������������������������������������������� ����� n
������������������������������ 0��������� 5��������� 10������� 15������� 20������� 25
j Pr�disposition
g�n�tique ;
k Ev�nement
d�clencheur ?
l D�sordre
immunologique, s�cr�tion d�insuline normale ;
m Perte
progressive de la s�cr�tion d�insuline (glyc�mie encore � peu pr�s
normale);
n Diab�te
d�clar�.
�� Un d�faut de synth�se de l�insuline entra�ne
une forte diminution des cellules b pancr�atiques.
Diab�te insulino�d�pendant :
.Poly
p 18.
La cause est la
synth�se pancr�atique, des cellules b, d�insuline
d�ficiente.
Les
cons�quences :
-
Hyperglyc�mie,
-
C�toacidose,
-
Hypertriglyc�rid�mie.
Dans le tissu
h�patique, le taux de glucose augmente, comme si on �tait en p�riode de je�ne.
La prot�olyse musculaire augmente quand il y a un d�ficit d�insuline.
De plus, il y a
la mobilisation des r�serves lipidiques :
-
Beaucoup
d�acides gras,
-
Augmentation
des VLDL dans les triglyc�rides� " Exc�s de
triglyc�rides,
-
Augmentation
massive de lipides circulants.
Ce sont les
lipides qui sont � l�origine des probl�mes de sant�.
La synth�se
massive de corps c�tonique, combin�e � une diminution du volume sanguin,
entra�ne une acidification du sang � l�origine du coma diab�tique.
v Diab�te non insulino�d�pendant :
.Poly
p 18.
Il est d� � la
r�sistance des tissus � l�action de l�insuline (mutations)
������������������ "� Foie glycog�ne (foie orient� vers la mise en
r�serve des lipides)
La diminution de
l�entr�e du glucose dans les tissus p�riph�riques est � l�origine du diab�te
non insulino�d�pendant.
Les
cons�quences :
-
Hyperglyc�mie,
-
Hypertriglyc�rid�mie,
v Glycosylation des prot�ines
ou code sucr� :
� La
glycosylation, principale modification post�traductionnelle des prot�ines :
Il
y a plus de 500 modifications diff�rentes r�pertori�es, dont les principales
sont :
-
Modifications
N�terminales :
-
Acylation
(ac�tyl, formyl, myristoyl),
-
M�thylation.
-
Modifications
C�terminales :
-
Amidation.
-
Modification
des cha�nes lat�rales des acides amin�s :
-
Ad�nylation,
-
Pr�nylation,
-
Acylation,
-
Hydroxylation,
-
Carboxylation,
-
GLYCOSYLATION.
Les principaux
types de glycosylation des prot�ines (prot�ines O_glycosid�es et N_glycosid�es)
sont des r�sidus osidiques ajout�s sur un r�sidu S�rine ou Thr�onine.
Parfois,
l�addition d�un glycosyl_phosphatidyl inositol se fait sur des prot�ines
ancr�es dans la membrane. Cette addition fait que des prot�ines sans segment
hydrophobe peuvent s�ancrer dans la membrane.
Ces
modifications post�traductionnelles entra�nent des modifications :
-
Des
propri�t�s chimiques de la prot�ine,
-
Et/ou
sa localisation cellulaire,
-
Et/ou
sa protection contre les activit�s prot�olytiques.
Toutes
les prot�ines membranaires et les prot�ines s�cr�t�es sont glycosyl�es.
L�intensit� de la glycosylation est variable :
-
De
moins de 3%, comme les immunoglobulines (IgG)
-
A
plus de 40% de la masse totale, comme la crypthropoi�tine
?
Les prot�ines ne
sont pas les seules mol�cules � �tre glycosyl�es, comme les glycolipides.
![]()
������������������������������ Glycoprot�ines
����������������������������������������������������������������� =
Glycoconjugu�s membranaires
������������������������������ Glycolipides
� Les
oligosaccharides comme mol�cules informatives :
� Les oligosaccharides comme
mol�cules d�information : le code sucr� :
Les
cellules utilisent des modifications oligosaccharidiques pour coder des
informations importantes concernant :
-
Le
ciblage intracellulaire des prot�ines,
-
Les
interactions cellule�cellule,
-
Le
d�veloppement tissulaire,
-
Les
signaux extracellulaires.
Le code sucr�
reste un code secret. La structure ramifi�e entra�ne une extr�me complexit�.
Par
exemple :
-
20
monosaccharides�������� "������� 1,44.1015 oligosaccharides
hexam�riques,
-
20
acides amin�s�������������� "������� 6,4.107 hexapeptides,
-
4
nucl�otides������������������� "������� 4096 hexanucl�otides.
Si
on prend en compte la sulfatation affectant un ou plusieurs
oligosaccharides :
"� 1017
oligosaccharides hexam�riques diff�rents.
La densit�
d�informations contenue dans une mol�cule de petite taille est tr�s largement
sup�rieure � celle contenue dans les acides nucl�iques.
Chaque
oligosaccharide va constituer un mot du code qui va pouvoir �tre d�chiffr� par
les prot�ines interagissant avec eux, les lectines.
� La glycosylation modifie les
propri�t�s physicochimiques des prot�ines :
-
Elle
intervient dans l�acquisition de la conformation tridimensionnelle des
prot�ines,
-
Elle
fait augmenter le caract�re hydrophile des prot�ines,
-
Elle
modifie la charge �lectrique globale de la prot�ine
Exemple : Glycoprot�ine �
acide sialique " groupe COO� � pH neutre.
� Les cons�quences biologiques
d�une alt�ration de la glycosylation sont tr�s variables :
�
Approche
:
-
Inhibition
de la glycosylation,
-
D�glycosylation
chimique ou enzymatique,
-
Manipulation
g�nique (�limination de site de glycosylation, extonction de g�nes),
-
Etude
des variants ou des mutations naturelles.
�
Effets
observ�s tr�s variables :
-
Dans
l�amplitude (ind�tectable " perte de
fonction),
-
Dans
les effets � l��chelle de la prot�ine glycosyl�e (" disparition)
-
In
vivo versus in vivo,
-
Suivant
le type cellulaire,
-
Suivant
le stade embryonnaire,
-
Suivant
la situation physiologique.
� Il est difficile
de pr�dire � priori la (ou les) fonction(s) assur�e(s) par un oligosaccharide
donn�.
�
R�les
biologiques des oligosaccharides :
-
R�le
protecteur,
-
R�le
stabilisateur de la matrice extracellulaire (maintient de l�int�grit�
tissulaire),
-
R�le
anti�prot�asique (protection du domaine extracellulaire),
-
R�le
dans le repliement et le trafic intra�cellulaire des glycoprot�ines,
-
Dans
la transcription de certains signaux hormonaux :
bhCG peut �tre
glycosyl�e ou non ; elle a la m�me affinit� pour r�cepteur. Mais quand la bhCG est deglycosyl�e,
il n�y a pas de stimulation de l�ad�nylate cyclase.
-
Dans
les interactions cellule�cellule et cellule�matrice cellulaire,
-
Dans
la fixation p�ri�cellulaire des virus, bact�ries, parasites, toxines (v�g�tales
et bact�riennes)
-
Dans
le syst�me immunologique (par exemple : les antig�nes des groupes
sanguins)
� Les lectines, prot�ines de
reconnaissance des oligosaccharides :
L�oligosaccharide
est un �l�ment de reconnaissance qui interagit avec des prot�ines
sp�cialis�es : les lectines.
Les 2 plus grands types de lectines
animales :
Les lectines de
type S :
-
Leur
localisation est intra�cellulaire.
-
Elles
pr�sentent une distribution tr�s large.
-
Ce
sont des prot�ines solubles.
-
La
liaison est sp�cifique aux glucides, ind�pendante du Ca2+.
Les lectines de
type C :
-
Leur
localisation est membranaire ou extra�cellulaire.
-
Elles
pr�sentent des domaines CRD (Carbohydrate Recognition Domain) plus ou moins
pr�serv�s (~120
aa)
-
La
liaison est d�pendante du Ca2+.
v Introduction � la
glycosylation :
� Les
organites cellulaires impliqu�s :
Ce sont le
r�ticulum endoplasmique et l�appareil de Golgi.
Dans l�appareil
de Golgi, il y a 3 compartiments qui se caract�risent par un jeu
d�enzymes :
-
Citernes
cis,
-
Citernes
m�dianes,
-
Citerne
trans.
� Les
principales liaisons :
Les principales types de liaison
saccharide�polypeptides :
.Poly
p 19.
-
La
liaison N_glycosidique������������ "� Les plus nombreuses,
-
La
liaison O_glycosidique,
-
La
liaison O_glycosidique avec le collag�ne�������� (plus
rare),
-
L�ancre GPI (=
Glycosyl Phosphatidyl Inositol),
Les grandes familles selon le type de
liaison :
.Poly
p 19.
-
Type
mannose pr�dominant (structure minimale),
-
Type
hybride,
-
Type
complexe.
� Les
diff�rents types de liaisons dans un oligosaccharide N�li� :
.Poly
p 19.
� Les
d�riv�s nucl�otidiques impliqu�s dans la biosynth�se des oligosaccharides :
La
formation d�une liaison glycosidique demande un apport d��nergie libre.
Dans les
conditions physiologiques :� DG = +16 kJ.mol�1.
Cette
�nergie libre est acquise par la transformation des unit�s monosaccharidiques
en d�riv�s nucl�otidiques, comme l�UDP�glucose qui est n�cessaire �
l�allongement des cha�nes de glycog�ne.
Ces d�riv�s
nucl�otidiques permettront ensuite le transfert de l�unit� monosaccharidique
sur la prot�ine en cours de glycosylation, transfert catalys� par une
glycosyl_transf�rase.
Synth�se cytosolique des d�riv�s
nucl�otidiques glucidiques :


Probl�me :
La glycosylation
s�op�re dans le r�ticulum endoplasmique et l�appareil de Golgi.
Importation des
d�riv�s nucl�otidiques dans les v�sicules de l�appareil de Golgi :
.Poly
p 19.
v La biosynth�se des
oligosaccharides N�li�s :
� Les
grandes �tapes :
La
synth�se des glycoprot�ines N�li�es se passe dans le r�ticulum
endoplasmique, puis dans l�appareil de Golgi.
C�est un
ph�nom�ne co�traductionnel qui se d�roule en 4 �tapes :
j� Synth�se d�un pr�curseur oligosaccharide li�
� un lipide,
k� Transfert de ce pr�curseur au groupe NH2 d�un r�sidu
Asparagine du peptide en croissance,
l� Elimination de quelques r�sidus glucidiques,
m� Addition de r�sidus glucidiques au noyau
oligosaccharidique restant.
Ces �tapes ont
pu �tre d�finies gr�ce � l��tude du virus de la stomatite v�siculaire (VSV � grippe bovine)
� Construction
de dolichol :
.Poly
p 20.
Chez
les animaux :���������������� 17 � 21
unit�s isopr�niques ;
Chez
les v�g�taux :���������������� 14 �
24 unit�s isopr�niques ;
Le pr�curseur du
dolichol est le m�valonate ; il est aussi le pr�curseur du cholest�rol.
Synth�se du
dolichol_P�P_oligosaccharide :
j��������������������������������������������������������������������������������������������������� .Poly
p 20.
1�
Addition de N_acetylglucosamyl��
2�
Idem
3�
Addition de 5 r�sidus mannose (sous forme de GTP�mannose)
k��������������������������������������������������������������������������������������������������� .Poly
p 20.
-
Puis,
il y a un basculement total de la mol�cule qui ne baigne plus dans le cytosol mais
dans la lumi�re du RE (flip�flop),
par une lectine.
-
Puis,
il y a l�addition successive de r�sidus mannose. Cette addition se fixe sur un
dolichol� et entre par
flip�flop. Ce mannose fix� est transf�r� sur le dolichol_P�P_oligoszccharide
pour allonger la cha�ne.
l��������������������������������������������������������������������������������������������������� .Poly
p 20.
Il y a ensuite
addition de r�sidus glucose. Le dolichol�_glucose bascule
� l�int�rieur de la lumi�re du RE.

� Transfert
de l�oligosaccharide sur la prot�ine :
.Poly
p 21.
Cet
oligosaccharide est transf�r� sur un r�sidu Asparagine�aaX(sauf proline)�S�rine
(s�quence consensus)
du peptide en croissance.
Il s�agit d�un ph�nom�ne
co�traductionnel. L�oligosaccharide est transf�r� sur l�Asparagine.
L�oligosaccharide prot�ine transf�rase
(OPT) :
.Poly
p 21.
Les
ribophorines se lient facilement au ribosome. Il y a la formation d�un canal
par lequel la cha�ne peptidique entre dans le RE.
L�OST se situe
sur la membrane interne de la mitochondrie, proche du substrat de la r�action
et de la cha�ne peptidique en croissance. Elle transfert l�oligosaccharide sur
la prot�ine.
� Remaniement
de l�oligosaccharide :
.Poly
p 21.
Il consiste en
la lib�ration de 3 glucoses et 1 mannose.
"� L�oligosaccharide est donc constitu� de 2
N_ac�tylglucosamines et 8 mannoses.
Le r�le des 3
r�sidus glucose est de signaler que l�oligosaccharide est complet et pr�t
� �tre transf�r� sur la prot�ine.
Il existe des
transformations ult�rieures dans l�appareil de Golgi.

v La biosynth�se des
oligosaccharides O�li�s :

������������������������������ UDP_GlcNAc

������������������������������ UDP
������������������������������ UDP_Gal
������������������ ����������� UDP
������������������������������ CMP_SA
������ ����������� ����������� CMP
����������������������������������������������������������������� ���
������������������������������ GDP_Fruc
������������������ ����������� GDP
-
Addition
successive de r�sidus sur le peptide d�j� synth�tis�.
-
Il
n�y a pas de s�quence peptidique consensuelle.
" Les sites de
glycosylation seraient d�termin�s par les structures IIAIRE et IIIAIRE du polypeptide.
v Facteurs contr�lant la
glycosylation des prot�ines :
j� La structure IAIRE d�termine le
nombre et la localisation des sites potentiels de glycosylation. La s�quence
consensus pour
k� Il y a une sp�cificit� d�esp�ce et
tissulaire. Le type cellulaire influence la glycosylation par un �quipement
enzymatique particulier.
l� La structure tridimensionnelle de la prot�ine
influence l�ampleur et le type de glycosylation. 10 � 30 % des sites de
glycosylation ne sont pas occup�s.
La
r�partition des diff�rentes classes des oligosaccharides N�li�s est souvent tributaire
de sites particuliers de la prot�ine.
v Inhibition de la
glycosylation et de la synth�se des glucoprot�ines :
Inhibition des
principales �tapes :
-
Synth�se
de dolichol��,
-
Synth�se
de l�oligosaccharide au dolichol��,
-
Synth�se
de la prot�ine,
-
Action
des glucosidases et des mannosidases,
-
Inhibition
du transport entre les diff�rents compartiments cellulaires et du transport
vers la membrane.
�  Inhibition
de la synth�se du dolichol :
Inhibition
de la synth�se du dolichol :
Les cellules,
cultiv�es en pr�sence de 25_OH Cholest�rol ou de compactine, pr�sentent une
r�duction de 75 � 90% de la glycosylation des prot�ines simultan�ment � une
r�duction de m�me amplitude de la synth�se de cholest�rol et de dolichol��.
L�inhibition est
lev�e par l�addition exog�ne de m�valonate.
" Le dolichol�� est synth�tis� de novo � partir de l�ac�tate.
� Inhibition
de la synth�se de l�oligosaccharide :

La tunicamycine
inhibe da r�plication des virus � enveloppe. Elle est tr�s sp�cifique de l�UPP�GlcNAc.
C�est un inhibiteur comp�titif de tr�s forte affinit� pour l�enzyme (plus forte
affinit� que le substrat naturel)
Elle pr�senterait une structure
analogue � celle de l��tat de transition du substrat.
������ UDP�GlcNAc : KM = 2,9 . 10�6 M
Tunicamycine :
KI = 5 . 10�8 M
Il y a 2
probl�mes dans l�emploi de la tunicamycine :
� L�inhibition
de la synth�se prot�ique (d�pend du type cellulaire),
������ � Les cellules sont +/� sensibles � la
tunicamycine. Par exemple, les cellules tumorales ou transform�es pr�sentent
une grande sensibilit�.
Les analogues structuraux
du glucose peuvent �tre convertis par les cellules animales en
UDP�2_d�soxyglucose, GDP�2_d�soxyglucose et en dolichol�P�2_d�soxyglucose.
L�inhibition de
la glycosylation des prot�ines par le 2_d�soxyglucose est due principalement au
GDP�2_d�soxyglucose qui exerce une inhibition comp�titive sur l�action de
Cette inhibition est lev�e par
l�addition de mannose qui va agir � la fois en augmentant la concentration en
substrar (GDP�mannose) et en diminuant la synth�se de GDP�2_d�soxymannose.
Le
GDP�2_d�soxyglucose peut �galement servir de donneur de glucide pour la
formation de dolichol�P�P�(GlucNAc)2�DOG :
"� Pas d��longation ult�rieure possible,
"� Inhibition de la glycosylation en d�tournant
le dolichol�P vers la synth�se de cet oligosaccharide normal qui ne peut �tre
transf�r� aux prot�ines.
Remarque :
-
Il
faut se m�fier lors de l�utilisation de ces analogues structuraux.
-
Les
effets observ�s peuvent �tre m�taboliquement induits par ces mol�cules qui,
indirectement, perturbent la glycosylation.
� Inhibition
du trafic golgien :
-
Monensine
(ionophores)
-
Brefeldine
(antibiotique)
" Inhibition de
la glycosylation terminale en bloquant le transport intracellulaire entre le RE
et l�appareil de Golgi.
Inhibition de l�ancre GPI :
-
Le
mannosamine (comp�titeur du mannose)
v Contr�le qualit� des
prot�ines glycosyl�es :
La d�gradation
des glycoprot�ines N�li�es par
Contr�le qualit� du repliement des
prot�ines dans le RE :
.Poly
p 22.
La
formation de ponts di�sulfure dans les prot�ines par ERP57 stabilise la
structure IIIAIRE des prot�ines.
Les lectines
reconnaissent l�oligosaccharide.
v Aiguillage et adressage des
prot�ines glycosyl�es :
� R�le
des r�sidus mannose�6� dans
l�aiguillage des prot�ines :

.Poly
p 22.
Dans
le cis�golgi, les enzymes subissent des phosphorylations.
Cela leur sert �
�tre reconnu par des r�cepteurs sp�cifiques : r�cepteurs de mannose_6�.
.Poly
p 22.
Puis, il y a un bourgeonnement gr�ce �
des mol�cules : les clathrines.
Les
clathrines forment des tuskelions, qui s�assemblent entre eux. Il y a la
formation de mol�cules qui se d�tachent.����������� " Les v�sicules
sont recouvertes de clathrine.
 La mol�cule est
dirig�e vers le CURL (Comportement of Uncoating Receptor and Ligand), o� les pH
sont plus acides.
La mol�cule est
dirig�e vers le CURL (Comportement of Uncoating Receptor and Ligand), o� les pH
sont plus acides.
Puis,
le mannose est recycl� et va vers le trans�golgi.
� Adressage
des prot�ines glycosyl�es : p�le basal contre p�le baso�lat�ral :
Une
cellule polaris�e pr�sente des interactions par rapport au p�le basal et 2
domaines principaux s�par�s en fonction des jonctions serr�es (le domaine
apical et le domaine baso�lat�ral)

Tri
des prot�ines apicales et baso�lat�rales dans les cellules �pith�liales
MDCK :
Au trans�golgi, on retrouve des
v�sicules destin�es � aller au p�le apical et des v�sicules destin�es � aller
au p�le baso�lat�ral.
Tri
des glycoprot�ines apicales et baso�lat�rales dans les h�patocytes :
Toutes les prot�ines sont exp�di�es � un
seul des p�les de la cellule.