
Retour au sommaire des cours |

Une version pdf est à votre disposition ici. |
v M�thodes
de d�termination :
� M�thodes
analytiques :
� Principe :
-
Si un �l�ment est pr�sent dans un
tissu, c�est que la plante en a besoin. (quelques
exceptions)
-
Si un �l�ment est pr�sent en plus
grande quantit� qu�un autre, c�est que la plante en plus besoin qu�un autre.
� R�sultat :
|
9 macro
�l�ments =
�l�ments plastiques ou
constitutifs |
CO H N K, P, Ca, Mg, S |
(% de la mati�re s�che) 40
� 45 % 40
� 45 % 6
� 7 % 1
� 3 % 0.5
% chacun |
4
�l�ments ≈
90 � 95 % 5
�l�ments�� inf. � 5 % |
|||
|
≈
60 micro
�l�ments =
traces ou oligo-�l�ments ou
�l�ments dynamiques |
Fe,
Mn, Cu,
Zn, Mo,
Bo, Al,
I, etc. |
|
Inf.
� 0.5 % |
�
Variabilit� selon
l�esp�ce :
Na, Cl, Si :
difficiles � placer :
-
Ils ne sont pas constitutifs,
m�me en grande quantit�.
-
Ignorance d�un quelconque r�le
dans le dynamisme du v�g�tal.
-
Taux tr�s variable :
Exemple des gramin�es :
pr�sence importante de Si dans les feuilles
(1% de la masse foliaire)
�
Variabilit�
environnementale :
Exemple
du littoral : les plantes se sont habitu�es �
une salicit� importante en s�questrant le sel (NaCl) de mani�re � ce qu�il ne
soit pas toxique.
�
Probl�mes de cette
m�thode :
-
Chacun des �l�ments list�s est-il
r�ellement indispensable ?
-
Si oui, sous quelle forme alimentaire
doit-il �tre administr� ?
Les plantes peuvent �tre hyper
accumulatrices de traces (m�talliques) ; celles-ci sont donc utilis�es
pour d�polluer des sols satur�s (exemple du fer)
 �� Mati�re fra�che
�� Mati�re fra�cheDessiccation
� �
���������������������������������������������������������� Mati�re s�che������������ Incin�ration��������������� +
���������������������������������������������������������� � �10 � 20 %��� ����������� ��
��������������������������������������������������������������������������������������������������������������������� Mati�re min�rale
≈ 5 %
� M�thodes
synth�tiques :
� Principe :
R�ponse � la question :
sous quelle forme alimentaire ?
C�est m�thode empirique : on recherche la croissance optimale en changeant la composition du milieu. Elle impose un tr�s grand nombre d�essais, avec quelques contraintes :
����������� � l�obligation de conditions st�riles, pour �viter les interactions n�fastes de microorganismes se nourrissant du milieu et excr�tent des toxines.
����������� � le contr�le des �l�ments utilis�s : diff�rents niveaux de puret� du milieu et apports de traces avec les flacons et la verrerie.
� M�thode :
�
Pour les
champignons :
On
effectue des cultures de conidies (spores asexu�es) en bo�tes de p�tri (Pasteur et Raulin)
�
Pour les v�g�taux
chlorophylliens :
On effectue des cultures de plantes
enti�res sur milieu solide (Liebig
et Boussingault)
Probl�me de la composition initiale de
la terre.
����������� �
obligation de calciner la terre pour d�truire la mati�re organique (MO) et
laver la mati�re min�rale (MM)
Apparition de la culture hydroponique (=
aquiculture)
avec Javillier (pr�curseur de la culture � hors sol �)
= milieu
exclusivement liquide :
-
obligation d�asepsie (� graine
l�g�rement nettoy�e � la javel),
-
a�ration (� �viter
l�asphyxie),
-
renouvellement le plus
fr�quemment possible.
Contrainte majeure :
composition de la graine �
pr�sence d��l�ments dans sa r�serve
����������� Cette
r�serve ne pose pas un gros probl�me pour les macro �l�ments mais est tr�s
importante quant � la pr�cision des traces.
Exemple de l�Iode :
on effectue une �tude sur plusieurs g�n�rations o� l�on appauvrie de plus en
plus le milieu ce qui permet de r�duire au fur et � mesure la quantit� de
l�iode dans les graines produites.
� R�sultats :
�
Cas des
champignons :
On a d�fini un milieu de Raulin (= le
plus favorable � la croissance)
Exemple de Aspergillus niger :
|
Aliment |
Quantit� |
El�ment |
8
macro �l�ments chez
le champignon : le Mg compense l�absence du Ca. |
Eau |
1500 mL |
O,
H |
|
|
Saccharose |
|
C |
|
|
Acide
tartrique Pas tr�s utile en soi : effet bact�ricide |
|
/ |
|
|
NH4NO3 |
|
N |
|
|
NH4PO4H2 |
|
P |
|
K2C03Carbonate de potassium |
|
K |
|
|
MgCO3 Carbonate de magn�sium |
|
Mg |
|
|
(NH4)2SO4 sulfate d�ammonium |
|
S |
|
|
|
|
Zn,
Fe et Si |
Principaux
micro �l�ments |
�
Cas des v�g�taux
chlorophylliens :
Aliment
|
Quantit� |
El�ments |
8
macro �l�ments + Carbone
produit lors de la photosynth�se |
|
Eau |
1000
mL |
O,
H |
|
|
NH4NO3 |
|
N |
|
|
KPO4H2 |
|
P,
K |
|
|
Ca(NO3)2 |
|
Ca |
|
|
MgSO4 Sulfate de magn�sium |
|
Mg,
S |
� Action d�un �l�ment sur la croissance et interaction entre
�l�ment :
Courbe d�action de E :
 Croissance
Croissance
���������������������������������� ��� E est d�ficient�������������������� E
est exc�s
���������������������������������� ���� = carence��� �������
Doses�����
���������� =
toxicit�
���������������������������������������������� en E���� ����� optimales������������� de E
(+ quelques traces)������������������������������� ��� e1��������������� e2�������� [ E ]
 Carence��������� ���� Sub-carence���� e1 �(agriculture������� Luxe alimentaire e2��� Exc�s
Carence��������� ���� Sub-carence���� e1 �(agriculture������� Luxe alimentaire e2��� Exc�s
���������������������������������������������������������� raisonn�e)
Micro-�l�ments :� 10�8 g.L�1������������������������������������� �� 10�6
g.L�1
Macro-�l�ments : 10�4�������� g.L�1������������������������������ � 10�2 g.L�1
Constatation vis-�-vis
de la situation d�exc�s : la plante ne
� trie � pas les �l�ments en fonction de ses besoins mais absorbe
tout ce qui se pr�sente � elle.
�
Sympt�mes
diagnostics :
= observation de la plante pour constater une situation alimentaire.
-
Carence :
�
Chloroses (= zone d�fra�chie)
����������� �
Sensibilit� aux pathog�nes
Exemple
de la betterave sucri�re : la carence en
Bohr (Bo) entra�ne une fragilisation de la plante qui favorise l�envahissement
du Phoma (champignon)
�
Mise en place de m�thodes alternatives de lutte qui permettent d��viter les
fongicides.
-
Exc�s (en particulier
l�azote) :
�
Verse
Exemple du bl� :
exc�s de NH4+
(ion ammonium) La plante emploie des m�canismes de d�sintoxication utilisant du
Carbone pour fabriquer les acides amin�s. Celui-ci n�est donc plus disponible
pour la solidification en cellulose des parois. De plus, l�ammoniaque entra�ne
une mont�e rapide en longueur.
�
Interactions :
� Facteur
limitant :
=
El�ment dont la concentration p�nalise le rendement alors que les
concentrations des autres �l�ments sont optimales.
 ����������������������� Croissance
����������������������� Croissance
����������� C.max����������������������������������������������� Courbe
d�action de r�f�rence de A
����������������������� ���� d C.max��������������������������������������� (= avec [ B ] non limitant)
����������� C.max
��������������������������������������������������������������������������������� Courbe
d�action de A
��������������������������������������������������������������������������������������������� avec [ B ] limitant (= B d�ficient)
��������������������������������������������������������������������������������� ���� [ A ]
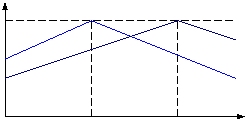
� Interaction
antagoniste :
1
��������������������������������������������������������������������������������� ��� Courbe d�action du Ca2+
������� 0,6�������������������������������������������������������������������� avec
[ Mg2+ ] =
������� 0,4��������������������������������������������������������� ��� Courbe d�action du Ca2+
��������������������������������������������������������������������������������� avec
[ Mg2+ ] =
1��������� ��������� 2����������� [
Ca2+ ] en
mM
C.max pour : � Ca2+/
Mg2+ =
1/1,5 = 2/3 = constante
Ca2+ et Mg2+ = ions bivalents (= leur sites
d�absorption racinaires identiques)
Si, dans le sol, [ Ca2+
] augmente sans que [ Mg2+
] augmente, on observe une d�ficience par saturation vis-�-vis du ratio Ca2+/
Mg2+.
On utilise ce genre d�interaction pour
d�polluer une terre satur�e en effectuant plusieurs niveaux de culture. Il
suffit de traiter la plante en fin de d�pollution pour qu�elle retrouve un
ratio �quilibr�.
|
Polluant |
Antagoniste |
||
|
Rubidium |
Rb+ |
Potassium |
K+ |
|
S�l�niate |
SeO42� |
Sulfate |
SO42� |
|
Ars�niate |
H2As04� |
Phosphorate |
H2PO4� |
|
Chlore |
Cl� |
Iode |
I� |
� Interaction
antagoniste inverse (= synergie) :
Exemple :
|
Fertilisation phosphor�e
(2 niveaux) Fertilisation azot�e (2
niveaux) |
P 1 (inf.) |
P2 (sup.) |
|
N1 (inf.) |
x |
+ 150 quintaux/ha |
|
N2 (sup.) |
+ 150 quintaux/ha |
+
60� quintaux/ha |
� Difficult� : �tablissement d�un crit�re de rendement :
Exemple :
la betterave sucri�re :

MF (tonnes. ha�1)����������������������������������������������������� ����� Sucre (tonnes.
ha�1)
��������������������������������������������������������������������������������� ������� 10
![]() ���� 100���������������������������������������������������������������������������������������������������������� Racine
���� 100���������������������������������������������������������������������������������������������������������� Racine
��������������������������������������������������������������������������������� ������� 5
���������������������������������� ���
������200������� 250���� ��� 300� ������� Azote (kg. ha�1)
-
-
Les 50 derniers kg. ha�1
sont en surplus, la plante fabrique des feuilles pour pi�ger l�azote dans des
squelettes carbon�s (acides amin�s) ����� � D�toxication
Les
cultivateurs sont pay�s en fonction de la concentration en sucre dans la
betterave :
-
-
Le r�servoir est plein �
� La concentration diminue et la r�colte devient
moins rentable.
� Correction avec des engrais :
Souvent
les �l�ments : Azote, Phosphore, Potassium.
Pour
les autres �l�ments, on ne se pose des questions qu�apr�s avoir surexploit� le
terrain.
 ����������� a + b + c = constante
����������� a + b + c = constante
���������������������������������� �� A����� a2������� ��
B
���������������������������������� ������� a1����
b1
���������������������������������������������������������� b2
������� c1����������� �������� c2
�� C
� N����������������� ���� P
|
���� N����
P���� K���� |
|
����� 8���� 8����
8 |
|
���� 12��� 4����
8 |
�K
� N ���������������� �������P
��������������������������������������������������������������������������������� 6, 9, 9 : dosage optimal
��� K
Seul
probl�me : on ne poss�de aucune explication
avec r�sultats.
� M�thodes
physiologiques :
� Analyse chimique :
Exemple :
la ferrodoxine :
 e ˉ
e ˉ
(donneur)�
Fe2+����������������������������������� Fe3+
(accepteur)
����������� �����
(Red.)������������������������������������������ � (Ox.)
e ˉ
� Emploi de radio�l�ments :
=
marquage d��l�ments.
�  Sympt�me diagnostic :
Sympt�me diagnostic :
N
���������������������������������������������������������������������� ������ � � verse � des c�r�ales
��������������������������������������������������������������������������������� �
���������������������������������������������� N�������� ����������������������� ������ Ca
� Chlorose�������������� � chlorose��� calcique
����������������������� � �����Bo
��������� � Phoma
(pour la betterave)
Mg =
m�talochlorophyllie (= m�tal pr�sent au corps de la chlorophylle)
Ca2+ = divalent. �������� Si [Ca2+
] augmente,
[ i 2+
] diminuent ������ � carence en ces autres divalents.
Ca2+
sert dans le rev�tement ionique (rigidit� de la membrane)
Un exc�s de Ca2+entra�ne
un d�ficit de fluidit� des membranes.
Ca2+

v Alimentation carbon�e
:
� Autotrophie
pour le Carbone :
� Les plantes lithotrophes :
Energie
lumineuse ou chimique
CO2 + H2O + AH2 ��� ������� �����
�HCHO�� +
������� Oxydant������������������������� ����������� ��� (produit r�duit)� �forme oxyd�e
 ����������� ����������� = CMin�ral����� ������
= pouvoir������������������������ = COrganique
����������� ����������� = CMin�ral����� ������
= pouvoir������������������������ = COrganique
-
gazeux,����������������������� ����������� r�ducteur������������������� =
maillon d�hydroxyde carbonique
-
dissous
���������������������� (H2O ou min�raux)��������������� (exemple : cha�ne de sucre)
(ou recombin� dans l�eau
comme le carbonate)
��� ������� Que
des substances min�rales
�
Les plantes photo �
lithotrophes :
�
Les v�g�taux chlorophylliens :
=
algues, bryophytes et plantes vasculaires.
A�robiose
![]() CO2 + H2O + 2 H2O ���
��� ��� �HCHO��
+ 2 O2 = + H2O
CO2 + H2O + 2 H2O ���
��� ��� �HCHO��
+ 2 O2 = + H2O
�
Les bact�ries primitives :
=
Chlorobact�riales (bact�ries vertes) et Thiobact�riales (bact�ries pourpres)
Ana�robiose
![]() CO2 + H2O + 2 SH2� ��� ��� ��� �HCHO��
+ 2 S + H2O
CO2 + H2O + 2 SH2� ��� ��� ��� �HCHO��
+ 2 S + H2O
�
Les plantes chimio �
lithotrophes :
Pouvoir r�ducteur quelconque
![]()
![]() CO2
+ H2O
+ (4 H+)� ��� ��� ��� �HCHO�� +
H2O
CO2
+ H2O
+ (4 H+)� ��� ��� ��� �HCHO�� +
H2O
���������
Substances
���������� min�rales
[ R�d. ]����������������������� [ Ox. ]
Ressources
�nerg�tiques ( �
pouvoir r�ducteur) :
-
NH4+ : Nitrobact�riales,
-
SH2 : Thioleucobact�riales
(� leuco � = blanc �
pas besoin de pigments),
-
FeCO3 : Ferrobact�riales,
-
H2 : Hydrog�nobact�riales.
� H�t�rotrophie
pour le Carbone :
=
le Carbone est d�j� sous forme organique.
� Plante chimio � organotrophes.
3
types de comportements alimentaires :
� Les parasites :
�
Les v�g�taux
sup�rieurs :
Exemple
du Gui (Viscum album) :
Il
n�est pas h�t�rotrophe obligatoire (pr�sence d�un feuillage vert et persistant)
Printemps
� �t� (pommier en feuille) �
pompage.
Hivers
�
autotrophie.
�
Les Champignons :
Exemple
d�Auricularia judae.
� Les saprophytes :
=
nutrition de corps morts avec l�aide de micro-organismes qui s�occupent de la
d�composition.
�
Les v�g�taux
sup�rieurs :
Exemple
de Limodorum arbortivum (orchid�e)
�
Les Champignons :
Exemple
de Pleurotus eryndii.
� Les symbiotes :
= les Lichens (associations
champignon � algue)
L�algue
fixe et distribue le Carbone.
v Alimentation
Azot�e :
� Autotrophie
pour l�Azote :
Nitrate����� Ammonium
N2��
/�� NO3ˉ��
/�� NH4+
��������� Atm. / en solution� ��
forme r�duite
� H�t�rotrophie
pour l�Azote :
On
retrouve les 3 m�mes types de comportement alimentaire que pour le Carbone.
|
AZOTE |
|
CARBONE |
|
Autotrophie |
Pas de corr�lation avec |
H�t�rotrophie |
|
H�t�rotrophie |
Donc forc�ment : |
H�t�rotrophie |
v Principe :
� G�n�ralit�s
et rappels :
150
milliards de tonnes de Carbone fix�es par an :
-
135 milliards de tonnes par le
plancton,
-
15 milliards de tonnes par les
v�g�taux terrestres :
-
11 par les for�ts,
-
4 par les prairies.
La
fixation se fait par des pigments assimilateurs.
� Les
pigments assimilateurs :
� Les pigments actifs :
� acte photochimique :������ Energie
photonique �
Energie chimique
����������������������� X l������ l
= longueur d�onde du pic d�absorption
�
Chez les v�g�taux
sup�rieurs et les algues :
� La chlorophylle a (sur les
chloroplastes)
2
types dont la composition mol�culaire est identique : on parle de polym�res de la chlorophylle a
ou d�holochromes (quand il y a
association avec des prot�ines) :
P 700
et P 680
�
Chez les
bact�ries :
� La chlorophylle a (sur les
chromoplastes, corps un peu granuleux adh�rant la membrane)
����������������������� B860
(bact�riochlorophylle pour bact�ries pourpres)
et B890
(bact�rioviridine pour bact�ries vertes)
�
La chlorophylle :

Chlorophylle
a :��������� R
= CH3
4 noyaux pyrroles reli�s par des ponts carbon�s
= H�me
= T�trapyrrole ferm�
Partie
non prot�ique
La
mol�cule sch�matis�e s�appelle le Chromophore
et fait partie de
� Les pigments accessoires :
Energie
photonique �� �������� �������� (Pigments
actifs)��������� ���������� ��������� Energie chimique
�� R�le de transmetteur
�
Les v�g�taux
sup�rieurs :
-
Ca
670,
-
Ca
690,
-
Chlorophylle
b,
-
Carot�no�des.
�
Les algues :
-
Chlorophylle
b : chlorophyc�es (= algues vertes),
-
Chlorophylle
c : ph�ophyc�es (= algues brunes),
-
Chlorophylle
d : rhodophyc�es (= algues rouges),
-
Carot�no�de
(
-
Biliprot�ines :
-
-
et
�
Les bact�ries
pourpres :
-
Carot�no�des.
�
Les
Carot�no�des :
Xanthophylle,
b �
carot�ne, etc.
Ils
font partie de la famille des lipides et pr�sente une structure terp�nique (= isopr�ne) :

b �
carot�ne : C40H62
1 vitamine A������������������������� 1
vitamine A
Provitamine
A
�  R�le des pigments accessoires :
R�le des pigments accessoires :
Pigment accessoire (= antenne
collectrice)
����������� ��
hl
��������������������������������������������������������������������������������� Pigment
actif (= centre r�actionnel)
Excitation par vibration
��������������������������������������������������������������������������������� �
transmission de l��nergie par vibration
���������������������������������������������� =
r�sonance de l��nergie photonique (hl)
par vibration
Puis
le pigment actif convertit cette �nergie en �nergie chimique en lib�rant des
�lectrons.
� Spectre d�absorption des pigments :
e = f( l )
 �
e������� 410 � 430 ����������������� ����660
�
e������� 410 � 430 ����������������� ����660
����������������������� inf. 560����������������������
���������������������������������������������������������������������������������
��������������������������������������������������������������������������������� Longueurs d�onde �teintes (= absorb�es)
��������������������������������������������������������������������������������������������� (bleu et rouge)
���������������������������������������������������������������������������������
��������������������������������������������������������������������������������� Longueur
d�onde r�fl�chie
��������������������������������������������������������������������������������������������� (vert
� jaune)
����������� 400����������������� ���� 600����������������������� l (nm)
Spectre d�absorption de la feuille d��pinard
Spectre d�absorption de
Spectre d�absorption de la b � Carot�ne������������������ ����������������������������������������������������������������������
�����������
 ���������������������������������������������� 650����������������������������
���������������������������������������������� 650����������������������������
���������������������������������� 560���������������������������������������� Spectre d�absorption de
����������� 400���������������������������������������������������� ����������� Spectre d�absorption de
��������������������������������������������������������������������������������� Spectre d�absorption de
��������������������������������������������������������������������������������� un pic dans les
UV (400) et un autre dans les IF
���������������������������������������������������������������������� La
vie en eaux profondes entra�ne le besoin
���������������������������������������������������������������������� d�une
longueur d�onde qui parvienne jusque dans
��������������������������������������������������������������������������������� les
fonds marins.
� Spectre d�action de la photosynth�se :
�
Techniques
d��tablissement des spectres :
Exp�rience
de T. W. Engelman (1843 � 1909) sur Bacterium
thermo (algues vertes)
����������� (chimiotactisme positif � l�O2)
On
effectue un suivi d�une algue verte avec une culture de bact�ries. S�il y a une
activit� photosynth�tique, il y a un d�gagement d�O2
et donc une prolif�ration bact�rienne.
L�algue
est �clair�e � plusieurs longueurs d�onde.
� la
photosynth�se est plus importante dans une lumi�re rouge que dans une lumi�re
bleue.
Lumi�re
= �nergie photonique (contient des photons)
����������������������� 1 photon � 1
quantum (�nergie �lectrique, en Joules)
Max
Planck (1858 � 1947) : �tablissement de la constante de Planck, h = 6,626 . 10�31
Quantum
= q = h.n ������������� n (en Hertz) = c / l = 3.1010 / l
����������� q = 6,626 . 10�31. 3.1010 / l
����������� ��
= 19,878 . 10�21 / l
1
mole de photons � bleus � : Nq470 = 255 kJ
1
mole de photons � rouges � : Nq670 = 179 kJ
Alors que l�on s�attend � : Nq670
> Nq470
Photosynth�se :��������� 1 photon expulse 1 �lectron.
Si
on se met � �nergie (ou intensit�) �lectrique constante : q670
= q470
,
il
faut�� plus d��nergie
� rouge � que d��nergie
� bleue �
�
plus de photons
� rouges � que de photons
� bleus �
�
il y aura plus d��lectrons
expuls�s avec la lumi�re rouge qu�avec la lumi�re bleue (� m�me intensit�)
�
la photosynth�se est plus
importante avec la lumi�re rouge qu�avec la lumi�re bleue.
�
R�sultats :
Exemple
d�une algue rouge : Delesseria sanguinea.
Pr�sence
de 3 pigments : 1 pigment actif (la chlorophylle a) et 2 pigments
accessoires (la chlorophylle b et la phyco�rythrine)

���������������������������������������������������������������������� Il
faut travailler � intensit� constante.
���������������������������������������������������������� Spectre
d�absorption des pigments
���������������������������������������������������������� Spectre
d�action de la photosynth�se
400����� 500����� 600����� 700����� 800����� ��� l (en nm)
� Le devenir de l��nergie absorb�e :
Soit
PE0 : un pigment � l��tat
fondamental, stable, avec une �nergie potentielle E0.
Et P�E1 : le m�me pigment � l��tat excit�,
instable, avec une �nergie potentielle E1
 hn�������������������������������������������� �� (E1
sup�rieure � E0,
soit par surplus d��nergie,
hn�������������������������������������������� �� (E1
sup�rieure � E0,
soit par surplus d��nergie,
PE0��� ��� 10
-15 sec.��������������������� �� soit par une
structure �lectronique modifi�e)
���������������������������������������������� P*E1
��������������������������������������������������������������������������������� � PE0� +�
hn� �� P*E1
�nergie de restitution
(sous diff�rentes natures)
� Restitution par fluorescence :
 10
-8 � 10 -12
sec.
10
-8 � 10 -12
sec.
Effet Joules (perte de chaleur w0)����������������� � P*E1� �� PE0� +� w0�
+� hn�
����������� + �mission d�un photon hn�
��������������������������������������������������������������������������������������������������������������������� = hn
��������������������������������������������������������������������������������������������� Donc :� hn��
<�
hn
��������������������������������������������������������������������������������������������� Donc :�� q� ��<� �q
��������������������������������������������������������������������������������������������� Donc :�� l�
��>�
�l
Exemple
de la chlorophylle a :
-
�clairage � 460 nm
-
Fluorescence � 560 nm.
Cette
exp�rience n�est possible in vivo, mais impossible � reproduire in
situ.
� Restitution par r�sonnance :

� P*E1 ����� PE0� +� w0� .
hn������������������������������������������ ������ P�E�0����� P�*E�1
� ���PE0��������������������������������������������� �
���������������������������������������������������������� ����� P*E1
����������������������������������������������������������������������
����������� P�*E�1
����������������������� ����� Chaleur w0
���������������������������������������������������������� P�E�0
Et
ainsi de suite�
� Restitution par conversion de l��nergie :
= �mission d�un proton
(caract�ristique des v�g�taux sup�rieurs)

� P*E1� �� PE0� +� w0�
+� eˉ
����� hn������� ��
PE0����������������������������������������� ��
����������������������� ����������� ����������������������� P*E1��������������������������
���������������������������������� PE0��������������������������������������������������������������� pigment
m�tastable
� eˉ![]() ���������������� Pigment�������������������������������������������������������� =
stable en �nergie
���������������� Pigment�������������������������������������������������������� =
stable en �nergie
![]() Mol�cule�������� ��������
m�tastable�������� ��� Chaleur w0 ���������������������������������� et
instable en �lectron.
Mol�cule�������� ��������
m�tastable�������� ��� Chaleur w0 ���������������������������������� et
instable en �lectron.
r�ductrice������ ���������������������������������� +
(pouvoir r�ducteur)��������������������������� ������� eˉ
���������������������������������������������������������������������� � cha�ne de transporteurs d��lectrons
![]() Synth�se
de glucides :
Synth�se
de glucides :
Test
de Dugol :
Exemple
de Pelargonium sp. (g�ranium ornemental)

����������� �
���� R�colte le matin�������������������������������������������������������������������� �
����������������������� (pas de lumi�re)
����������� ���
�� R�colte le midi����������������������� �
�thanol,
����������������������� (12H d��clairement)
����������� ���
�� R�colte le midi���������������������������������������������������������������������� �
����������������������� (12H d��clairement avec
un cache)
v M�canisme
de la photosynth�se :
� Existence de 2 grands types de r�action :
� Effet de la temp�rature sur la photosynth�se :
Exemple de
Chlorella pyrenoidosa :�������������
������� Intensit� ����������������������� Courbe d�action de la temp�rature :
 de
la photosynth�se :
de
la photosynth�se :
���������������������������������������������������������������������� Lumi�re forte (temp�rature limitante)
��������������������������������������������������������������������������������� � r�action photochimique, dite � claire �
���������������������������������������������������������������������� Lumi�re
faible (hn limitant)
��������������������������������������������������������������������������������� � r�action thermochimique,
����������������������� 12������� 16������� 20������� 24������� ����������������������� dite � obscure � ou � sombre �
���� Temp�rature (en �C)�������� ����������� (s�effectue aussi en phase lumineuse)
�
temp�rature constante, c�est la lumi�re qui d�termine l�intensit� de la
photosynth�se.
� Effet de la lumi�re intermittente sur la photosynth�se :
Exp�rience
de la lumi�re R. Emerson (1932) :
����������� �
�clairage par flash est meilleur que continu.

���������������������������������������������������������� �������� On conserve les m�mes dur�e et
intensit� des flashs.
����� VO2 (en mL)
|
Phase
obscure (en sec.) |
Nombre
d��clair |
Rendement
par �clair |
|
1/1000 |
5 |
VO2
/5 |
|
1/500 |
3 |
VO2
/3 |
|
1/100 |
2 |
VO2
/2 |
|
1/50 |
1 |
VO2
/1 |
|
1/10 |
1 |
VO2
/1 |
Plus
les �clairs sont espac�s, plus le rendement est bon.
���������������������������������������������� Courbe
d�action de la phase obscure :
Rendement
de
la photosynth�se
 ���������������������������������������������� Dur�es
optimales
���������������������������������������������� Dur�es
optimales
� 100%���������������������������������������������������������������������������������� ����������� 25� C
���������������������������������������������������������������������� 1� C
����������� 0��������� 0,1������ 0,2������ 0,3������ 0,4������ 0,5������ Phase obscure (en sec.)
Jusqu��
0,2 seconde, la phase obscure est limitant. � 1� C, le m�tabolisme est au
ralenti et il faut une phase obscure plus longue pour que les r�actions
thermochimiques aient le temps de se faire (assimilation du Carbone min�ral en
Carbone organique) La lumi�re ne sert qu�� exciter les pigments et apporter le
pouvoir r�ducteur (r�actions photochimiques)
� Scission de la mol�cule H2O :
� Mise en �vidence du r�le de H2O :
Rappel sur
les v�g�taux chlorophylliens (algues, bryophytes, plantes vasculaires) :

CO2� +� 2 H2O� �� �HCHO�� +�
O2=� +� H2O
���������������������������������������������������������������������� � A�robiose
�
priori :�������� Photo
� oxydor�duction.
����������������������� CO2��������������������������� � �HCHO�
����������� H2O��� +�������������������������������� +��� H2O
����������������������� H2O��������������������������� � O2���������������������������� H2O :
pouvoir r�ducteur originel.
Exp�rience
de R. Hill (1937) :
Suspension
de chloroplastes fonctionnels + milieu isotonique.
�
Incubation sous vide (pas de CO2
ni de O2)
![]() + ajout
d�h�moglobine ��������������������� ������oxyh�moglobine (avec un spectre
d�absorption
+ ajout
d�h�moglobine ��������������������� ������oxyh�moglobine (avec un spectre
d�absorption
��
Fixation d�O2��������������������� diff�rent
de l�h�moglobine)
Observation :
D�gagement
d�O2 que
s�il y a un broyat cellulaire, en fait qu�en pr�sence d�un oxydant puissant.
Exemple :������� 2 Fe3+� +�
H2O� �� 2 Fe2+� +�
� O2� +�
2 H+
� Mais�
Si �a marche avec Fe3+,
alors l�eau rentre dans l�oxydor�duction pour la formation de l�O2 �
� Donc, il y a scission de la mol�cule de l�eau ! �
![]()
![]() �2 H2O� �� 2 H+�
+� 2 OHˉ� �� H2O� +�
2 eˉ� +� � O2.
�2 H2O� �� 2 H+�
+� 2 OHˉ� �� H2O� +�
2 eˉ� +� � O2.
���������������������������������� H2O� �� 2 H+� +�
2 eˉ�
+� � O2
���������������������������������������������� Pouvoir r�ducteur
���������������������������������� = photolyse
(scission dans la photosynth�se)
� L��mission d�O2 provient de la
scission de H2O�
Exp�rience
de Rubens (1941)
����������� �
Utilisation d�isotopes (= marqueur radioactif)
 ���������������������������������� H218O������������ et������� C18O2
���������������������������������� H218O������������ et������� C18O2
���������������������������������������������� � ���Chlorelles.
���������������������������������� ������ 18O2�������������������� 16O2
CO2� +�
2 H2O� �� �HCHO��
+� O2�
+� H2O
Analogies
avec la photosynth�se bact�rienne :
CO2� +�
2 SH2� �� �HCHO��
+� 2S� +� H2O
-
Chlorobact�riales (=
bact�ries vertes)
� B890
= Bact�rioviridine.
-
Thiobact�riales
(= bact�ries pourpres)
� B860 =
Bact�riochlorophylle ; Bact�riopupurine.
-
Thiorhodobact�riales :
exemple de Chromatium warmingii qui garde le souffre, ce qui leur donne leur
coloration rouge.
-
Athiorhodobact�riales :
exemple de Rhodopseudomonas sp. qui, en a�robiose, est h�t�rotrophe et, en
ana�robiose, est photo-organotrophe.
CO2 +� 2 CH3�CHOH�CH3� �� HCHO� +�
2 CH3COCH� +� H2O
���������������������������������������������� �� Pouvoir
r�ducteur
� Scission de H2O et transfert de
pouvoir r�ducteur :
Le
photosyst�me II (P680) :

���������������������������������������������������������������������� Antenne
collectrice
��������������������������������������������������������������������������������������������� =
pigments accessoires (Ca670,
������ Chlorophylle b, Carot�no�des)
2 photons
��������������������������������������������������������������������������������������������������������� Centre r�actionnel
E0 = 0,82 V�������������������������������������������������������������������������������������������������� = pigment actif.
H2O� �� � O2� ������� ���������������������������������������������������������� ����������� P680��� ������ E0 = 0,90 V
����������� ���
���+� 2 H+�
+� 2
eˉ
������ Pouvoir r�ducteur����������
���������������������������������������������� �� P+680��������������������������������� ����������������������� ������ P*680������ E1
���������������������������������������������������������� E0������������������������������������������������������������������
Donneur d�eˉ = r�ducteur
Accepteur d�eˉ = oxydant
����������� E0 Red� <� E0
Ox���������������������������������� ����������� ����������� �������� 2 eˉ
��������������������������������������������������������������������������������������������� ����� � Cha�ne
de transporteurs
|
|
PS
II |
Centre
r�actionnel P680 |
E0
= + 0,90 V |
par apport d��nergie Transfe Spontan�
|
|
Transport de H+ et eˉ |
Plastoquinone
PQ |
|
E0
= 0 V |
|
|
Transport que d�eˉ |
Cytochrome
F |
|
E0
= + 0,34 V |
|
|
Plastocyanine Pc |
|
E0
= + 0,37 V |
||
|
PS
I |
Centre
r�actionnel P700 Ratio Chl. b/Chl a > Ratio du PS II |
E0
= + 0,43 V |
||
|
Ferredoxine Fd |
|
E0
= � 0,43 V |
||
|
Transport de H+ et eˉ |
FAD
/ FADH
2 |
|
E0
= � 0,38 V |
|
|
NADP
+ / NADPH, H
+ |
Nicotinamide |
E0
= + 0,38 V |
�
Structure du chloroplaste :
Diam�tre :
3 � 10 �m����������������������������������������������������������� Thylako�de
= membrane

Lumen du thylako�de������������������������������������������������������ thylako�de
intergranaire
(pH acide)���� ��������������������������������������������������������������������������������������������� stroma
= compartiment����������������������������������������������������������������������������� thylako�de
granaire
intrathylako�dal���������������������������������������������������������������������������������������� granum
��������������������������������������������������������������������������������������������������������� enveloppe
ADN circulaire������������������������������������������������������������������������������������������
Chloroplastique����� ���������������������������������������������������������� accumulation transitoire d�amidon
���������������������������������� Globule lipidique plastidiaux
����������������������� (10
� 15 nm) � carot�no�des dissous
�
Sch�ma g�n�ral de la
cha�ne des transporteurs :

Stroma intra chloroplasmique�������������������������������������������������������������������� ����������� NADPH �+
H+
2 photons����������������������������������������������������������������� 2
photons
�� ( l = 680 nm)��������������������������������������������������������� ��� ( l = 700 nm)
��������������������������������������������������������������������������������������������������������� ����� �Fd����������� ����������������������� NADP+
���������������������������������� PQ����� ����� PQH2
����������������������� �� 2 e ˉ
����������� P680��������������������������������������� � ��������������������� ����������P700
���������������������������������������������������������� ����������������������� ���������������������������������� ����� FAD
�� 2
e ˉ������������ ����� Cyt f��������� �����������
���������������������������������������������������������� ����������������������� ���������������������������������������������� ���� FADH2
���������������������������������������������������������������������� ��� Pc
������ PS II������������������������������������������������������������������������������ ��� PS I
Stroma intra v�siculaire
����������������������� (protons
pr�lev�s � l�ext�rieur et lib�r�s � l�int�rieur)��� ������������������ ����������������������� � gradient de
protons
� Fixation et devenir du carbone min�ral (cycle de Calvin) :
� M�thode d��tude :
Melvin
Calvin (1911 � 1997) : montage � Lollipop �
Carbone
radioactif : 14CO2��� �
Radio chromatographie.
 ���� CO2���������� ��� �����Agitateur
���� CO2���������� ��� �����Agitateur
������ O2���������������������������������������������� �������Pompe��������������������������� Capillaire en
serpentin
��������������������������������������������������������������������������������������������������������� o�
l�on peut injecter du
��������������������������������������������������������������������������������������������������������� CO2
radioactif � des moments
��������������������������������������������������������������������������������������������������������� pr�cis
d��coulement.
Extraction et radiographie des sucres
solubles dans de l��thanol � 100� C
� R�sultats :
=
radio chromatogrammes des produits form�s (rayonnement b du
-
Nature des mol�cules ?
-
Ordre de parution ?
-
Quantit� de marquage ?
5 sec.�������������������������������������� 10 sec.������������������������������������ 30 sec.
![]()


 ��������������������������������������������������������������������������������������������������������������������� ������� malate
��������������������������������������������������������������������������������������������������������������������� ������� malate
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() ��������������������������������������������������������������������������������� ����� �alanine���� �� glutamate
��������������������������������������������������������������������������������� ����� �alanine���� �� glutamate
![]()
![]() ���� 80%���������������������������������������������� �������� glycine
s�rine���� ���aspartate
���� 80%���������������������������������������������� �������� glycine
s�rine���� ���aspartate
![]()
![]()
![]() ��������������������������������������������������������������������������������������������� saccharose������������������ APG
��������������������������������������������������������������������������������������������� saccharose������������������ APG
![]()
![]()
![]()
![]()
![]()
![]() ��������������������������������������������������������������������������������������������������������� trioseP oseP
��������������������������������������������������������������������������������������������������������� trioseP oseP
![]() �������������������������������������������������������������������������������������������������������������������������������� ose
diP
�������������������������������������������������������������������������������������������������������������������������������� ose
diP
��������������������������������������������������������������������������������������������������������������������� UDPG
Acide
3_phosphoglyc�rique�������������������������������������������������� Sucre
(APG)����������������������������������������������������������������������� Acides amin�s
CH2OP�CHOH�COOH
��������������������������������������������������� Acides organiques
� Fixation du CO2 :
Calvin
et Benson (1944 � 1959) :
���������������������������������������������� Rubisco
(= ribulose 1,5 biphosphate carboxylase oxyg�nase)
RUBP� +�
CO2� +�
H2O� ��
2 APG (acide_3_phosphoglyc�rique)
�� C5��� ����� C1������������������������ 2
C3��������������� On
parle de photosynth�se � C3 �
CH2O�P������������������������������������������� CH2O�P������� +��������� CH2O�P
|��������� ����������� ���������������������������������� |�������������������������������� |
C=O��������������� ���������������������������������� CHOH���������������������� CHOH
|��������������������� ���������������������������������� |�������������������������������� |
CHOH����������� ���������������������������������� COOH���������������������� COOH
|
CHOH
|
CH2O�P
La rudisco : ��� r�le de carboxylase (lors de la
photosynth�se)
et r�le d�oxyg�nase (lors de la
photo-respiration)
-
Elle est activ�e par le Magn�sium
Mg2+,
-
Et est constitu�e de 16
sous-unit�s (masse totale : 550 kDa)
-
Elle constitue 50 % des prot�ines
foliaires et 70% des prot�ines du chloroplaste.
Arguments
exp�rimentaux :
![]()
![]()
![]() Lumi�re��������� ������
Obscurit�
Lumi�re��������� ������
Obscurit�

![]() C.P.M����������������������������������������������������������������������� Glucides
C.P.M����������������������������������������������������������������������� Glucides
 (coups par
minute)��������������������������������������������������������������������������� APG
(coups par
minute)��������������������������������������������������������������������������� APG
![]()
��������������������������������������������������������������������������������������������������������� RUBP
![]()
����������� + 14CO2
(1%)� =������������������������������� 30������� ���
40��� ���� Temps (en minutes)
![]()
![]()
![]() Lumi�re�������������������� ������� Obscurit�
Lumi�re�������������������� ������� Obscurit�
![]() C.P.M������������ �������� + CO2 (1%)������������������ ����������� � CO2�� (sous
vide)
C.P.M������������ �������� + CO2 (1%)������������������ ����������� � CO2�� (sous
vide)
![]() (coups par
minute)
(coups par
minute)
![]()
![]()
![]() �������������������������������������������������������������������������������������������������������������������������������� R.U.B.P
�������������������������������������������������������������������������������������������������������������������������������� R.U.B.P
![]()
![]() �������������������������������������������������������������������������������������������������������������������������������� A.P.G
�������������������������������������������������������������������������������������������������������������������������������� A.P.G
![]()
���������������������������������������������� �
200�������������� � 100 ������������� 0��������� �
10O������������ Tps (en sec.)
-
L�absence de CO2
entra�ne une incapacit� � r�duire le R.U.B.P qui va donc s�accumuler.
Ce
qui veut dire qu�il continue � �tre synth�tis�. D�o� vient-il ?
-
La lumi�re, l�APG et toutes ses
transformations permettent de r�g�n�rer le RUBP. La photosynth�se commence avec
la synth�se du glucide RUBP (=pr�curseur) et cherche � le r�g�n�rer.
-
La photosynth�se
� C4 � :
Chez
les gramin�es tropicales (ma�s, canne � sucre, etc.)
���������������������������������������������� ������ PEP Case (= phospho-�nol pyruvate carboxylase)
����������������������� PEP� +�
CO2� +� H2O� �� OAA� +�
2 H+� +� 2 eˉ
Phospho-�nol pyruvate���������� Acide oxaloac�tique
-
La photosynth�se
� CAM � (= Crassuleam Acid Metabolism) :
Chez
les plantes dites grasses ou succulentes (agave, etc.)
� R�duction et devenir de l�APG :
�
�tape 1 :
����������� ����������������������� Triose_P
d�shydrog�nase
![]() 2 APG �+� 2 (NADPH + H+)� �� 2 Ald PG� +� 2 H2O� +� 2 NADP+
2 APG �+� 2 (NADPH + H+)� �� 2 Ald PG� +� 2 H2O� +� 2 NADP+
���� ATP���������������������� ADP� +� Pi����� (r�action non spontan�e)
CH2O�P������������������������������������������������������ CH2O�P
|�������������������������������� 2 H+��������������� ����������� |��������������������� glyc�rald�hyde_3_P
CHOH����������� +��������� +�������������������������������� CHOH����������� = ald�hyde
phosphoglyc�rique
|�������������������������������� 2 eˉ���������������������������� |
COOH��������������������������������������������������������� CHO
Tout
sera multipli� par 2 pour une mole de CO2
fix�.
Il faut donc 4 eˉ
pour r�duire une mol�cule de CO2
fix�.
�
�tape 1� :
Ald PG����������� �������� DHA�P� (d�shydroxyac�tone_P)
CH2O�P������������������������������������������� CH2O�P
|�������������������������������������������������������� |
![]() CHOH���������������������������������������������� C=O
CHOH���������������������������������������������� C=O
|�������������������������������������������������������� |
CHO������������������������������������������������� CH2OH
�
�tape 2 :
����������������������� ������
Aldolase
Ald PG� +� DHA�P� �� Fructose 1,6 bi_P
�� C3��������������� C3������������������ C6
CH2O�P������������������� CH2O�P������������������������������� CH2O�P
|�������������������������������� |�������������������������������������������� |
CHOH����������� +��������� C=O�������������������������������������� C=O
|�������������������������������� |�������������������������������������������� |
 CHO������������������������� CH2OH��������������������������������� CHOH
CHO������������������������� CH2OH��������������������������������� CHOH
��������������������������������������������������������������������������������� |
��������������������������������������������������������������������������������� CHOH
��������������������������������������������������������������������������������� |
��������������������������������������������������������������������������������� CHOH
��������������������������������������������������������������������������������� |
��������������������������������������������������������������������������������� CH2O�P
�
�tape 3 :
����������������������� ������
Fructose biphosphatase
Fructose 1,6 bi_P� +� H2O� �� Fructose 6_P�
+� Pi
� R�le central du Fructose 6_P :

![]() Fructose 6_P
Fructose 6_P
![]() ��������������������������������������������������������������������������������������������� Glucose 6_P
��������������������������������������������������������������������������������������������� Glucose 6_P
![]()
![]() ���������������������������������������������������������������������� Condensation
���������������������������������������������������������������������� Condensation
R�g�n�ration������������� Saccharose bi_P��������������������������������������������
�Isom�risation
![]() du
RUBP������ ���������������������������������������������������������������������� Glucose 1_P
du
RUBP������ ���������������������������������������������������������������������� Glucose 1_P
![]()
���������������������������������� Saccharose� +� PPi����������������� ����������������������� � Polym�risation
![]()
![]() ��������������������������������������������������������������������������������������������� n Glucose 1_P
��������������������������������������������������������������������������������������������� n Glucose 1_P
����������� R�serves
pour
les plantes saccharif�res
��������������������������������������������������������������������������������������������� Amidon� +� n Pi
(stockage temporaire durant
la phase photosynth�tique, puis stockage dans les organes sp�cifiques durant la
nuit)
� R�g�n�ration du RUBP :
�
�tape 1 :
Trans-c�tolase
Fructose 6_P� +� Ald PG� �� Xylose 5_P� +� �rythrose 4_P
![]() ������ C6����������� ������� C3���������� �� ��C5������������� ����� C4
������ C6����������� ������� C3���������� �� ��C5������������� ����� C4
��������������������������������������������������������������������������������� CHO
���������������������������������� Isom�risation� ����������� ����������� |
���������������������������������������������� Ribulose 5_P������������� CHOH
��������������������������������������������������������������������������������� |
��������������������������������������������������������������������������������� CHOH
��������������������������������������������������������������������������������� |
��������������������������������������������������������������������������������� CH2O�P
�
�tape 2 :
��� Aldolase
�rythrose
4_P� +� DHA�P� �� Sedoheptulose
1,7 bi_P
������ C3����������� ������� C3���������������������� C7
CH2O�P������������������� CH2O�P������������������������������� CH2O�P
|��������� ����������������������� |�������������������������������������������� |
CHOH���������������������� C=O�������������������������������������� C=O
|�������������������������������� |�������������������������������������������� |
CHOH���������������������� CH2OH��������������������������������� CHOH
 |������������������������������������������������������������������������������� |
|������������������������������������������������������������������������������� |
CHO������������������������������������������������������������������������ CHO
��������������������������������������������������������������������������������� |
��������������������������������������������������������������������������������� CHOH
��������������������������������������������������������������������������������� |
��������������������������������������������������������������������������������� CHOH
��������������������������������������������������������������������������������� |
CH2O�P
�
�tape 3 :
Trans-c�tolase
Sedoheptulose 1,7 bi_P�
+� Ald PG� �� Xylose 5_P� +� Ribose 5_P
![]()
![]() ������ C7����������� ����������� C3������ ����������� C5������ �����
��C5
������ C7����������� ����������� C3������ ����������� C5������ �����
��C5
���������������������������������������������� ���������������������������������� Isom�risation������������������������ ���������������������������������������������� ���������������������������������� ����������� 2 Ribulose
5_P
CH2O�P������������������� CH2O�P������� ����������������������� ����������� CH2O�P������������������� CHO
|�������������������������������� |�������������������������������������������������������� |�������������������������������� |
C=O�������������������������� CHOH���������������������������������������������� CHOH���������������������� CHOH
![]() |�������������������������������� |�������������������������������������������������������� |�������������������������������� |
|�������������������������������� |�������������������������������������������������������� |�������������������������������� |
CHOH���������������������� CHO������������������������������������������������� CHO������������������������� CHOH
|������������������������������������������������������������������������������������������� |�������������������������������� |
CHO������������������������������������������������������������������������������������ C=O�������������������������� CHOH
|������������������������������������������������������������������������������������������� |�������������������������������� |
CHOH��������������������������������������������������������������������������������� CH2OH��������������������� CH2O�P�������
|
CHOH
|
CH2O�P
�
�tape 4 :
![]() 2
Ribulose 5_P� �� RUBP
2
Ribulose 5_P� �� RUBP
ATP��������������� ADP� +� Pi����� (r�action non spontan�e)
� BILAN en Carbone du cycle de Calvin :
![]()
![]()
![]() H2O�������������������������������������� Ald PG
H2O�������������������������������������� Ald PG
![]() CO2��������������� 2 APG
CO2��������������� 2 APG
![]()
![]() RUBP������������������������������������ Ald PG����������� DHA_P��������������������� Fructose 1,6 bi_P
RUBP������������������������������������ Ald PG����������� DHA_P��������������������� Fructose 1,6 bi_P
![]()
![]()
![]()
![]()
![]()
![]() H2O�������������������������������������� Ald PG����������� ����������� �rythrose
4_P� +� Xylose 5_P
H2O�������������������������������������� Ald PG����������� ����������� �rythrose
4_P� +� Xylose 5_P
![]() CO2��������������� 2 APG ��������������������������������������������������������������������������������������������� RUBP
CO2��������������� 2 APG ��������������������������������������������������������������������������������������������� RUBP
![]()
![]() RUBP������������������������������������ Ald PG����������� ����������� Sedoheptulose
1,7 bi_P
RUBP������������������������������������ Ald PG����������� ����������� Sedoheptulose
1,7 bi_P
![]()
![]()
![]()
![]() H2O�������������������������������������� Ald PG����������� DHA_P���������� ��� Ribose 5_P� +�
Xylose 5_P
H2O�������������������������������������� Ald PG����������� DHA_P���������� ��� Ribose 5_P� +�
Xylose 5_P
![]() CO2��������������� 2 APG
CO2��������������� 2 APG
![]() RUBP������������������������������������ Ald PG ���������� DHA_P
RUBP������������������������������������ Ald PG ���������� DHA_P
D Tout est � multiplier par 2 pour une mole de CO2 fix�.
� Influence de hn sur les r�actions thermochimiques :
Exp�rience
de Calvin et Benson (1948) sur Scenedesmus sp. cultiv�e �
l�obscurit� sans CO2.
C.P.M����������������������������������������������������������� ��� C.P.M
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() ������
Sans CO2������������ +� CO2�����������������������������������
������
Sans CO2������������ +� CO2����������������������������������� ![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() ���������
Sans CO2 Sans CO2���� +� CO2
���������
Sans CO2 Sans CO2���� +� CO2
![]()
![]()
����������������������� �0�������������������� 50������������������� Min.��������������� �
10���� ����� 0��������������� �� 50���� Min.
Conclusions :
La
fixation du CO2
est possible � l�obscurit� d�s lors que les cellules chlorophylliennes
contiennent de l�ATP et du pouvoir r�ducteur produits dans les r�actions
photochimiques.
� R�actions entre les r�actions photo- et thermochimiques :
� Exigence quantique :
�
combien d��nergie q faut-il pour
fixer une mole de CO2 ?

 On
a vu qu�il fallait 4 eˉ
pour fixer 1 mol�cule de CO2.
La photosynth�se fonctionne sur le principe qu�un photon permet l�expulsion
d�un �lectron :
On
a vu qu�il fallait 4 eˉ
pour fixer 1 mol�cule de CO2.
La photosynth�se fonctionne sur le principe qu�un photon permet l�expulsion
d�un �lectron :
�������� 4 q������������������������������������������������������������������� 4
q
![]()
![]()
![]()

 ���������������������������������������������� ����������������������� 4
eˉ���������������� ���������������������������������������������� 4 eˉ
���������������������������������������������� ����������������������� 4
eˉ���������������� ���������������������������������������������� 4 eˉ
![]()
![]()
���������������������������������� PS
II������������������������������������������������������������� ��������� PS I
Il
faut 8 q pour fixer une mol�cule de CO2
et donc 8 Nq pour fixer une mole de CO2.
Calcul th�orique :
����������� 6 CO2� +� 6� H2O������ �������� C6H12O6� +� 6 O2
���������������������������������� DG0 = + 680 kCal
680/6
= 113 kCal pour une mole de CO2
fix�e.
Nq470 = 255 kJ = 61 kCal
����������������������� 113/61 � 2 Nq
Nq670 = 179 kJ = 43 kCal
����������������������� 113/43 = 2,65 � 3 Nq
Or,
on fonctionne sur l�hypoth�se de 8 Nq.
Il y a donc une perte �nerg�tique de 5 � 6 Nq.
Mesure
exp�rimentale :
����������� �
�nergie fix�e sous forme chimique
![]() Ratio
=
Ratio
=
����������� ����
�nergie photonique absorb�e
(rapport�
� une masse de v�g�tal et pour une dur�e donn�e)
-
Pour des algues vertes :
8 � 10 Nq par mole de CO2.
Rendement = 8 x 100 /10 = 80
% ���������������
� 80% de
l��nergie fix�e sert � la transformation du CO2
en sucre.
-
Pour les v�g�taux sup�rieurs :
12 � 20
Nq
par mole de CO2.
Rendement = 8 x 100 /20 = 40
% ���������������
� 40% de
l��nergie fix�e sert � la transformation du CO2
en sucre.
����������� � la perte par effet Joule
n�explique pas tout�
� Mais o� va
la fuite ?
� Les photo � phosphorylations :
![]()
![]()
![]() EN������������������������������������������������������������������������������������������������������������� Besoin d�un apport
EN������������������������������������������������������������������������������������������������������������� Besoin d�un apport
![]()
![]() � 0,43������������� Fd����������������������������������������������������������������� ����������� �������� d��nergie
� 0,43������������� Fd����������������������������������������������������������������� ����������� �������� d��nergie
![]() � 0,07������������������������ ����������� ����������� Cyt b 6
� 0,07������������������������ ����������� ����������� Cyt b 6
![]() ��� 0���������������������������������������������������� ����������� ����������� PQ
��� 0���������������������������������������������������� ����������� ����������� PQ
![]() + 0,34������������������������������������������������ Cyt
f
+ 0,34������������������������������������������������ Cyt
f
![]() + 0,37������������������������������������ PC
+ 0,37������������������������������������ PC
![]() + 0,43������������������������ PS I
+ 0,43������������������������ PS I
(en Volt)������������������������������������������������������������������� �������� Les eˉ vont des
�� r�ductions vers les oxydants.
En
pr�sence de lumi�re, la concentration en ATP augmente et ce m�me en
ana�robiose.
Ces
r�actions ce passent donc, non pas dans les mitochondries, mais dans les
chloroplastes.
Il
n�y a pas de production d�O2.
�
Phosphorylations
cycliques :
(1954)
![]()
![]() ������ ADP + Pi����������� ��� ATP
������ ADP + Pi����������� ��� ATP
![]()
![]()
![]() � 0,43������������� Fd�������
� 0,43������������� Fd�������
![]()
![]() � 0,07������������������������������������������������ Cyt
b 6
� 0,07������������������������������������������������ Cyt
b 6
![]()
![]()
![]()
![]()
![]() ��� 0��������������������������������������������������������������������������� PQ�����������������
��� 0��������������������������������������������������������������������������� PQ�����������������
![]()
![]()
![]() + 0,34������������������������������������������������ Cyt
f��������������� �� ADP + Pi���������������� Grand
saut �nerg�tique
+ 0,34������������������������������������������������ Cyt
f��������������� �� ADP + Pi���������������� Grand
saut �nerg�tique
![]()
![]() + 0,37������������������������������������ PC����������������������������� ATP
+ 0,37������������������������������������ PC����������������������������� ATP
![]()
![]() + 0,43������������� PS I
+ 0,43������������� PS I
���������������������������������� 700 nm
(en
Volt)
Quand
le saut est grand, l��nergie produite est r�cup�r�e.
Mais
quand saut est trop petit, l��nergie est perdue.
�
Phosphorylations acycliques :
=
cha�ne de transporteur de pouvoir r�ducteur
(parfois,
il y a production d�O2)
![]()
![]()
![]()
![]() � 0,43������������� ���������������������������������������������� Fd�������
� 0,43������������� ���������������������������������������������� Fd�������
![]()
![]() � 0,38������������������������������������ ����������� ����������� ����������������������� FAD
� 0,38������������������������������������ ����������� ����������� ����������������������� FAD
![]() � 0,3
� 0,3![]() 2������������� ADP + Pi������� ���������������������������������������������������������������������� NADP+
2������������� ADP + Pi������� ���������������������������������������������������������������������� NADP+

![]()
![]() ��� 0����������������� PQ������ ������� �ATP������
��� 0����������������� PQ������ ������� �ATP������
![]()
![]() + 0,34������������������������ Cyt
f���
+ 0,34������������������������ Cyt
f���
![]()
![]() + 0,37������������������������������������ ����������� PC������������������
+ 0,37������������������������������������ ����������� PC������������������
![]()
![]() + 0,43������������������������������������ ����������������������� ����������� PS I
+ 0,43������������������������������������ ����������������������� ����������� PS I
���������������������������������������������������������������������� ����������������������� ���
700 nm
![]()
![]() + 0,82������������� H2O
+ 0,82������������� H2O
![]()
![]() + 0,9�������������������������� �� PS II
+ 0,9�������������������������� �� PS II
(en
Volt) �������� ����������� ����������� ��������680 nm
D�un
point de vue �volutif,
� Th�orie chimio � osmotique de Michell :
Peter D. Michell (1920 � 1992)
![]()
![]() ���
ATPase������������������������������������������ ADP + Pi������������������� ��� ATP
���
ATPase������������������������������������������ ADP + Pi������������������� ��� ATP
 ATP��������������������������� ADP + Pi
ATP��������������������������� ADP + Pi
�������� ATPsynth�tase
��������������������������������������������������������������������������������������������������������� CF 1
Espace intra chloroplastique
Membrane
imperm�able
aux protons���������������� � �Cha�ne de transporteurs��������������������������� CF 0
���������������������������������� �� ���� pompe �
protons �
Thylaco�de
Espace intra v�siculaire
![]() CF 1 : synth�se d�ATP����������� ����������� �
Nature prot�ique
CF 1 : synth�se d�ATP����������� ����������� �
Nature prot�ique
CF 0 : canal membranaire
Les
chloroplastes produisent de l�ATP surtout pour son usage personnel. L�ATP pour
l�organisme est produit par les mitochondries.
�
Arguments
exp�rimentaux :
-
Sur une suspension de
chloroplastes :
![]() [H+]
[H+]
![]()

![]()
![]()
���������������������������������������������� �� Ionophore (d�coupe la membrane, la rendant perm�able)
![]()
����������� �0�������������������� 20������������������� 40
-
pH = 4 :
Thylako�de
isol� et � l�obscurit� :
����������� Simple
diffusion
![]()
![]()
![]()

![]()
![]()
![]()
![]()
![]()
 H+ ����������� ����������� PH = 7
H+ ����������� ����������� PH = 7
���������������������������������������������������������� Quelques
heures apr�s :
��������������������������������������������������������������������������������������������������������� ������� PH
= 4
���������������������������������������������������������� �quilibre
de [H+]
-
![]() pH
= 8 :
pH
= 8 :
![]()
![]()
![]() Ajout d�ADP +
Pi������������������������������ �ATP
Ajout d�ADP +
Pi������������������������������ �ATP

![]()
������ PH = 4![]()
![]()
v BILAN :
-
Photo � lithotrophes :����� ����������� �
Photosynth�se
-
Pr�sence de pigments actifs et
accessoires
Compl�mentarit�
entre l�aspect structural et le spectre d�action de la photosynth�se.
-
�nergie absorb�e par les pigments
restitu�e :
-
Par r�sonnance,
-
Par fluorescence,
-
Par conversion de cette �nergie
(�mission d�un �lectron)
-
Photosynth�se :
-
R�actions photo �
chimiques :
-
Scission de l�H2O,
-
Production et transfert du
pouvoir r�ducteur,
-
Production et transfert de l�ATP.
-
R�actions thermo �
chimiques :
-
Fixation CO2
�
utilisation du RUBP� (besoin de pouvoir
r�ducteur et d�ATP)
-
R�g�n�ration du RUBP
-
Bilan �nerg�tique :
-
Perte (d�perdition w0),
-
Formation d�ATP.
-
�quation g�n�rale de la
photosynth�se :
On
ne s�int�resse qu�� la lumi�re comme �nergie���� �
phototrophes
![]()
H2O� +� CO2� +� 2 AH2�������� ������ �HCHO�� +�
Photo � lithotrophe :������������ 2 H2O ���������������������������������������������� 2
O2
2 SH2 ����������������������������������� 2
S
Photo � organotrophe :�������� Mat. Org. (Red)�������������������� Mat.
Org. (Ox)
���������������������������������������������������������� (Thiobact�ries)
v L�azote
du sol :
� L�azote
organique :
Origine :
cadavres, d�jections, d�bris v�g�tations
���������������������������������������������������������� Humifications
(= d�gradations)
���������������������������������������������� Humus����������� =�������� Oligosaccharides
(provenant de polysaccharides)
���������������������������������������������������������������������� Oligopeptides
(provenant de prot�ines)
���������������������������������������������� Acides
amin�s (= monom�res) et amides,
���������������������������������������������� Ur�e
���������������������������������������������� Complexe
lignine � azote
(= composant pari�tal des
v�g�taux dur � d�composer)
� L�azote min�ral :
Origine :
������� cadavre ���������� et ������� humus
![]()
 ����������������������� ���� Putr�faction���������� ������� Ammonification
����������������������� ���� Putr�faction���������� ������� Ammonification
����������������������� ���� et d�composition
����������������������� ��� (bcp + rapide)
���������������������������������������������� NH4+
���������������������������������� (pas ce que
pr�f�rent les v�g�taux)
NH4+
: toxicit� rapide au niveau des structures cellulaires (d�placement des
charges)
����������� + antagonisme de certains
cations (K, Ca, Mg) �������� �
carences apparentes.

���������������������������������������������������������� Plante
![]() ���������������������������������� NH4+
���������������������������������� NH4+
![]() ���������������������������������� H+������������������ �quilibre
���������������������������������� H+������������������ �quilibre
Forte
acidification du sol (= de la rhizosph�re = environnement direct des racines)
Avantages :
la charge + permet
la fixation sur des �l�ments du sol (surtout � des �l�ments de charges n�gatives :
les colo�des) c�est int�ressant � petite dose.
![]() NH4+�� ����������� ����������� NO3ˉ (ion
nitrite : le nitrate) = forme finale de la min�ralisation.
NH4+�� ����������� ����������� NO3ˉ (ion
nitrite : le nitrate) = forme finale de la min�ralisation.
����������� Nitrification��������������� possibilit� de le stocker (surtout dans les vacuoles)
���������������������������������������������� +
aucun antagonisme
(au contraire : absorption
conjointe avec d�autres ions comme NO3ˉ;K+)

���������������������������������������������������������� Plante
![]() ���������������������������������� NH4+
���������������������������������� NH4+
![]() ���������������������������������� OHˉ�������������� �quilibre
���������������������������������� OHˉ�������������� �quilibre
Alcalinisation
du sol
����������� �
favorable pour la rhizosph�re car le sol est toujours un peu acide
� cause du C2O
� H2CO
D�faut :
NO3ˉ ne
tient pas longtemps dans le sol : r�pulsion des charges n�gatives et donc
la fixation est peu possible. Le NO3ˉ est
lessiv� et va dans les nappes phr�atiques et les cours d�eau.
Chez
les cultivateurs : apport des 2 formes
d�azote : nitrate d�ammonium
(= ammonitrate) NO3ˉ; NH4+
Nitrification :
-
Production d�azote nitrique par
nitrobact�riales
Exemple :
Nitrosomonas (bact�ries nitreuses) �
fixation du CO2
avec l��nergie chimique par oxydation (�tapes de nitrification)
-
Nitrosation :�������� NH4+� +� 3/2 O2� ������� �� ����� NO2ˉ� +� 2 H+� +� H2O
∆G� = 84 Kcal ����������� Pouvoir
r�ducteur
���� R�action exergonique ����� pour
la photosynth�se
������ (lib�ration d��nergie)
-
Nitratation :
������� NO2ˉ� + �� O2� �������� �� ����� NO3ˉ
Ex : Nitrobacter
(bact�ries nitriques) ����� ∆G� = � 19 Kcal���
� Cas particulier des plantes carnivores :
Surtout
insectivores, sauf les plantes exotiques (des monstres) qui peuvent choper une
grenouille)
Exemple de
Drosera sp. :
Elle
poss�de des feuilles sp�ciales qui assimilent directement (= exodigestion)
fixation des mouches par des gouttelettes � papier tue � mouches �
avec des enzymes hydrolytiques.
Exemple de
Dionaea sp. :
Elle
utilise un syst�me de pi�ge � loup.
Exemple de
Nepenthes sp. :
Elle
poss�de un syst�me de pi�ge en forme d�outre
v Utilisation
de l�azote atmosph�rique :
� Organismes fixateurs de l�azote :
Fixation
du N2 �
organismes = diazotropes
���������������������������������� 2 types
d�organismes : libres ou en association symbiotique.
� Les micro � organismes libres du sol :
-
Bact�ries h�t�rotrophes pour le
Carbone : ������ Azotobacter
chrorococcum (en a�robiose)
Clostridium pasteuriamum (en
ana�robiose)
Elles
utilisent un syst�me trop parfait qui fait donc qu�elles fixent plus de N2
qu�elles n�en ont besoin. Elles transforment la quantit� qui leur est
n�cessaire et lib�rent le surplus dans le sol.
����������������������� �
Organismes fertilig�nes.
-
Cyanobact�ries autotrophes pour
le Carbone : Nostoc
punctiforme
Anaboena cylindrica
Elles
utilisent le m�me syst�me que les bact�ries h�t�rotrophes. �
Organismes fertilig�nes.
Ce
syst�me offre la possibilit� d�une installation dans des zones
chaotiques : ce sont des organismes pionniers (ils pr�parent le terrain
pour d�autres esp�ces)
� Les symbioses :
-
Les lichens � cyanobact�ries du type
Collema sp. :
Les
cyanobact�ries sont des � esclaves � car c�est elles font tout.
-
Une plante sup�rieure et des
bact�ries :
Exemple
des l�gumineuses (pois, soja, tr�fle, luzerne, etc.) :
Les
l�gumineuses sont incapables de fixer le N2.
Les
bact�ries (Rhizobium ou Bradyrhizobium) ne fixent pas le N2
� l��tat libre, que quand elles sont en association symbiotique en formant
des nodosit�s (= petit groupement de bact�ries) :
-
Rhizobium����������������������� �
sur la racine de la plante,
-
Bradyrhizobium��� �
sur la tige de la plante.
Exemple
de l�aulne :
Il
s�agit d�une association non obligatoire, elle est surtout utile pour coloniser
un sol pauvre.
![]()

![]()
![]() ���������������������������������������������������������������������� � S�nescence��� ���
Liti�re
���������������������������������������������������������������������� � S�nescence��� ���
Liti�re
N2
 ��������������������������������������������������������������������������������������������������������� Humification
��������������������������������������������������������������������������������������������������������� Humification
 ��������������������������������������������������������������������������������������������������������� Ammonification
��������������������������������������������������������������������������������������������������������� Ammonification
��������������������������������������������������������������������������������������������������������� Nitrification
���������������������������������������������� ����������� Assimilation
du NH4+
���������������������������������������������������������� ����� � prot�ines�������������������� Enrichissement
progressif
��������������������������������������������������������������������������������������������������������� du
sol en NO3ˉ.
Fixation
� Symbiose Rhizobium � L�gumineuse :
� D�couverte :
Exp�rience
de Hellriegel et Wilfarth (1886) avec Pisum sativum (petit
pois)
|
Culture sur sable |
Culture sur terre |
R�sultat |
|
Calcin� |
Normale |
Carence
en azote �
jaunissement |
|
Calcin� |
Brute |
Croissance
et formation
de nodosit� |
|
Calcin� |
Lessiv�e
(suppression de la mati�re min�rale) |
Croissance
et formation
de nodosit� |
|
Calcin� |
Lessiv�e
et calcin�e (=
st�rilisation) |
Carence
en azote �
jaunissement |
Appellation
Beijerinck (1888) : Rhizobium leguminosarum
Mais
toutes les bact�ries ne forment pas des nodosit�s avec toutes les l�gumineuses.
�
recherche de la sp�cificit� symbiotique.
![]() Rhizobium
leguminosarum��� �� f�ve, pois, etc������� Prot�agineux
Rhizobium
leguminosarum��� �� f�ve, pois, etc������� Prot�agineux
Rhizobium
japonicum����������������������� �� soja
![]() Rhizobium
meliloti��������������� �� luzerne����������������� Fourrages
Rhizobium
meliloti��������������� �� luzerne����������������� Fourrages
Rhizobium
trifolii������������������ �� tr�fle
� Formation de nodosit�s :
�
![]() Modalit� signal�tique d�infection :
Modalit� signal�tique d�infection :
 Cellules de racine
Cellules de racine
���������������������������������������������� ����������� � Communication
 Rhizobium sensible��������������������������� ����� chimique
Rhizobium sensible��������������������������� ����� chimique
![]()
![]()
![]()
 aux flavono�des ������������������������������������������������������������������������������������������� ƒ Activation des
aux flavono�des ������������������������������������������������������������������������������������������� ƒ Activation des
de cette plante���������������������������������������������� - Flavono�des������������������������������������� g�nes noduline
![]()
![]() ���������������������������������������������������������� - Biotine (facteur de���� ����������� ������� ��� ������� Nodulation
���������������������������������������������������������� - Biotine (facteur de���� ����������� ������� ��� ������� Nodulation
 ����������������������� ‚ Activation������������� d�veloppement bact�rien) ������� �������R�cepteur sp�cifique
����������������������� ‚ Activation������������� d�veloppement bact�rien) ������� �������R�cepteur sp�cifique
����������� ������ des g�nes Nod���������������� - B�ta�ne
 �
�![]() �Production de lipo �
oligosaccharides
�Production de lipo �
oligosaccharides
sp�cifiques du rhizobium = Facteur Nod
Les
flavono�des sont des m�tabolites accessoires qui existent sous beaucoup de
types diff�rents. Chaque l�gumineuse envoie les siens : la bact�rie va
donc voir si la plante lui correspond ou non���������� �
spectre symbiotique.
�
![]() Nodulation :
Nodulation :
Elle
se fait au niveau de la zone pilif�re, avec les poils absorbants. Le rhizobium
y prolif�re et la plante y r�pond par 2 modifications :
-
Enroulement du poil sur lui-m�me
(= poil en crosse)
-
S�cr�tion d�une enzyme
hydrolytique, la pectinohydrolyse, qui d�truit partiellement les cellules du
poil permettant l�entr�e du rhizobium et la prolif�ration par un cordon
infectieux ferm� par la membrane de s�questration.
Celle-ci
conf�re au rhizobium une chromoprot�ine, la legH�moglobine. Cette prot�ine est
dite � mixte � parce que l�h�me est produit par la plante et la
bact�rie apporte la partie prot�ique. La legH�moglobine est un pi�ge � oxyg�ne,
toxique pour la bact�rie.
����������������������� LegH�moglobine������� �������� OxylegH�moglobine
���������������������������������������������� Fixation
de l�O2
La
legH�moglobine est une chromoprot�ine : les nodosit�s efficientes,
fixatrices de N2,
ont une couleur ros�e alors que les nodosit�s non efficientes, trop jeunes ou
trop vielles, ont une couleur blanche.
�
![]() Modalit� de la fixation du N2 :
Modalit� de la fixation du N2 :
����� ∆G� = 84 Kcal (r�action endergonique)
N2� +�
6 H+� +� 6 eˉ���� � ��
��� 2NH3
����������������������������������������������� ammonium
![]() ����������������������� ��� Pouvoir r�ducteur������������� azote min�ral r�duit�� NH3�
+� H2O� �� NH4+� +�
HOˉ
����������������������� ��� Pouvoir r�ducteur������������� azote min�ral r�duit�� NH3�
+� H2O� �� NH4+� +�
HOˉ
Enzyme : Nitrog�nase (NT)�������������������������������������� ����������� �����
�ammoniac���������������������� ammoniaque
� L�origine
du pouvoir r�ducteur :
Exp�rience
sur Clostridium pasteuranium (fixateur de N2
� l��tat libre et en ana�robiose) :
Vitesse d�incorporation du 15N2
(isotope stable)
![]() ( 106
atome.h�1)
( 106
atome.h�1)

![]()
![]() 20����������������������������������������������������������������������������������������� 60
min
20����������������������������������������������������������������������������������������� 60
min
��������������������������������������������������������������������������������������������������������� �+ Pi
35 min
25 min
15 min
���������������������������������������������� 10
min
2,5����������������������������� 5 min������������������������������������������������������������ ��� Pas de Pi (phosphate)
![]()
![]()
![]() � 2
� 2
![]()
����������������������� ��������������������������������������������������������������������������������������������� Pyruvate
����������������������� ����������� �
500�������������������������� ����������������������� ������� 1000������� consomm�
(�mol)
Interpr�tation :
3 (PO4H2ˉ, H+)� +�
3 (CH3�CO�COOˉ, H+)� �� 3 CO2� +� 6 H+�
+� 6 eˉ� +� 3 (CH3�CO~P)
���������������������������������������������� Pyruvate�������������������������������������������������������� �� ac�tyl_phosphate
L�origine
du pyruvate (ou acide pyruvique) est la glycolyse � partir du glucose
synth�tis�.
La
fixation du N2
est en fonction du m�tabolisme du carbone.
� Condition
de la fixation du N2 :
(en
ana�robiose)
����������� ��
Extrait de Clostridium pasteuranium
����������� + Fe, Mo, Mg
����������� + Prot�ine de 220 kDa (nitrog�nase)
����������� + ATP (2 ATP par eˉ
transport�)
����������� + Ferr�doxine
![]()
 20����������������������������������������������������������������������������������������� � ��Avec ATP
20����������������������������������������������������������������������������������������� � ��Avec ATP
 ��������������������������������������������������������������������������������������������� ��� Sans ATP
��������������������������������������������������������������������������������������������� ��� Sans ATP
����������������������� Avec
Fd :
10
���������������������������������������������������������� ����������� Sans
Fd :
![]()
![]() ��������������������������������������������������������������������������������������������� ������� Avec ATP Sans ATP
��������������������������������������������������������������������������������������������� ������� Avec ATP Sans ATP
![]() ��������������������������������������������������������������������������������������������� ���������
��������������������������������������������������������������������������������������������� ���������
����������������������� 5��������������������� 10������������������� 15������������������� 20������� Temps (en minutes)
� La
nitrog�nase :
= 2 sous � unit�s m�talloprot�iques
Prot�ine
II
![]()
![]() =
ferro � prot�ine ����������������� ATP � Mg
=
ferro � prot�ine ����������������� ATP � Mg
(= dim�re 2x27 kDa)
�� 54 kDa


![]()
![]()
![]()
![]()
![]()
![]() �����������
�����������
![]() ����������������������� ���������������������������������� ��
S������������������ S��������� �
Mo
����������������������� ���������������������������������� ��
S������������������ S��������� �
Mo
�S�������� S
����������� ����������������������� (Fe4
� S4)�������� ������
(Fe4 � S4)
![]() ����������� ����������� ����������� �S�������� S
����������� ����������� ����������� �S�������� S
![]() �� S����������������� S��������� �
Mo
�� S����������������� S��������� �
Mo
![]()
���������������������������������� ���� Prot�ine I = ferro � molybdo - prot�ine
220 kDa
���������������������������������������������� (=
t�tram�re 4x55 kDa)
� Sch�ma
g�n�ral de la fixation par r�duction du N2 :

![]()
![]()
![]()
![]()

![]()


�N������������������������������������������ N � H
|||����� +
2 H+� +� 2 eˉ����������������� ||������������������ +
2 H+� +� 2 eˉ
![]()
![]()
![]()
![]()
![]()
![]() ������������������ �N������������������������������������������
N �
H
������������������ �N������������������������������������������
N �
H
� M�tal
de transition������������������������� ����������� Di � imine

![]()

 ���������������������������������������������� H���� H�������������������������������������������������������� ����� H
���������������������������������������������� H���� H�������������������������������������������������������� ����� H
![]() ����������������������� |�������������������������������������������������������������������� ������ �|
����������������������� |�������������������������������������������������������������������� ������ �|
N �
H��������������������������������������������������������� ������ N �
H
���������������������������������������������������������������������� �� + 2 H+� +� 2 eˉ�������������� ������� |
![]()

![]() N �
H��������������������������������������������� ������ N �
H
N �
H��������������������������������������������� ������ N �
H
![]() ���������������������������������������������� |�������������������������������������������������������������������� ������ �|
���������������������������������������������� |�������������������������������������������������������������������� ������ �|
������������������������������������� H��� �H��������� ���������������������������������������������� ����� ![]() �H
�H
��������
Ammoniac������������������������������������������������������ ������ Hydrazyne

![]()
![]()
![]()
![]()

� Bilan :
-
La ferr�doxine c�de 6 �lectrons
en 3 �tapes (3 x 2 eˉ)
-
Il faut 2 ATP pour le transfert
des �lectrons de la prot�ine I � la prot�ine II.
-
Donc le co�t �nerg�tique pour une
mol�cule de N2 fix�e
est de 12 ATP.
�quation
th�orique : ������������ N2� +�
6 H+� +� 6 eˉ� +� 12 ATP ��� 2NH3
+ �12 (ADP + Pi)
���������������������������������������������� 6 x 2 (ATP � Mg)
![]() ���������������������������������� ����������� ����
12 ATP (pour assembler les 2 sous
unit�s)
���������������������������������� ����������� ����
12 ATP (pour assembler les 2 sous
unit�s)
![]()
![]()
![]()
![]()
![]()
![]() Pyruvate��������� FdOx��� ����� Fe2+���������� ����� Mo6+
Pyruvate��������� FdOx��� ����� Fe2+���������� ����� Mo6+
![]()
![]() + Pi���������������������������������������������������������������������������������������
2 NH
+ Pi���������������������������������������������������������������������������������������
2 NH
![]()
![]()
![]() ����������������������� �� 6 eˉ� ����������� ��
����NT���������� �����������
6 eˉ
����������������������� �� 6 eˉ� ����������� ��
����NT���������� �����������
6 eˉ
Ac�tyl~P������������������������������������������������������� �������� + 6 H+��� N2
 + 3 CO2��������� FdRed�� ����� Fe3+���������� ������ Mo5+
+ 3 CO2��������� FdRed�� ����� Fe3+���������� ������ Mo5+
+ 6 H+ ���������������������������������������������� 12 (ADP + Pi)
On
peut trouver d�autres �l�ments � la place du pyruvate et des �l�ments dans la
cha�ne de transporteurs.
-
Il y a production de H2
par les nodosit�s et par la m�me prot�ine,
�quation
secondaire :������������ 2 H+� +� 2 eˉ� +� 4 ATP ���
H2� + �4 (ADP + Pi)
D�o�
une �quation globale :
N2� +� 8 H+�
+� 8 eˉ� +� 16
ATP ��� 2NH3� +� H2� + �16 (ADP + Pi)
�
Gaspillage ?���������������������� NON,
Recyclage !
� Gestion de l�O2 par organismes fixateurs :
-
Strat�gie de l��vitement pour les
organismes ana�robies.
-
Adaptation physiologie pour les
organismes a�robies :
-
Hydrog�nase (cycle dit futile),
-
Augmentation de l�activit�
respiratoire (Azotobacter)
O2
dissous (�mol)

���������������������������������������������������������� Sans
Pi
![]()
![]()
����������� =�������� 10������� 20������� 30������� 40������� 50
Choc O2 40%
-
Adaptation cytologique :
-
Par sp�cialisation cellulaire :
Exemple :
Anabaena cylindrica (algues filamenteuse)
![]()
H�t�rocystes�������������������������� Cellules chlorophylliennes
(fixation du N2)��������� ����������� (photosynth�se)
-
Par compartimentation intra
cellulaire :
LegHb�
+� O2� �� OxylegHb (= filtre � O2)
� Application de la fixation N2 :
-
Fertilisation biologique des
sols :
-
Bact�ries libres : 5 � 40
kgN2.ha�1.an�1
Turned
over (= mort de l�organisme sinon fixation pour son usage personnel)
-
Symbioses : 10 � 20% d�azote
fix� qui est restitu�.
![]() En
pratique : � Soit une
association : Ray � Grass / Tr�fle�� � 60 �
150 kgN2.ha�1.an�1
En
pratique : � Soit une
association : Ray � Grass / Tr�fle�� � 60 �
150 kgN2.ha�1.an�1
���������������������������������������������������������� F�tuque
/ Tr�fle
����������������������� Soit une rotation :����� C�r�ales
� F�v�roles
���������������������������������������������������������� Betteraves � Luzerne
-
Enrobage (semences
techniques) :
(Hollande) Inoculum = culture
� dense � de Rhizobium
Objectif : 2L pour
-
G�n�tique de la fixation de
l�azote :
(sciences
fiction)��������� Enzyme NT � g�nes
NIF (d�couvert par Dixonet Postgate en 1974)
���������������������������������� Hydrog�nase � g�nes
HUP
Possibilit�
d�int�grer ces g�nes dans E. coli. Maintenant, il faut int�grer ces g�nes
procaryotiques dans un g�nome eucaryotique en faisant en sorte que ces g�nes
soient constitutifs.
� Effet de l�azote du sol sur la fixation du N2 :
Quand
il y a une symbiose, il y a une r�gulation de la fixation en fonction de la
pr�sence dans le sol.
![]() Activit� de
Activit� de


 2��������������������� ����������� (�mol.gMF�1.h
�1)
2��������������������� ����������� (�mol.gMF�1.h
�1)
���������������������������������������������������������������������� 2 jours
1
���������������������������������������������������������������������� 4 jours
���������������������������������������������� ��� 7 jours
![]()
� 0������������������� 2��������������������� 4��������������������� 6��������� NH4
/ NO3 (en
mM) dans le sol

![]()
![]() D�veloppement des nodosit�s ��������������������� (chez
le pois)
D�veloppement des nodosit�s ��������������������� (chez
le pois)
 Masse d�un
Masse d�un
nodosit�������������������������������������������������������������������������������������������� Nombre de nodules
��������������������������������������������������������������������������������������������������������� par
plante
![]()
�
��������� 0,3������������������ 3��������������������� 30������������������� NO3
(en mM) dans le sol
� Conclusion :
 Cellule
h�te
Cellule
h�te
 Photosynth�se����������� ����������������������� ����������� Symbiosome
Photosynth�se����������� ����������������������� ����������� Symbiosome
���������������������������������� Squelettes������������������������������ LegHbO2
![]()
![]()
 ���������������������������������� carbon�s�������������������������������� �
���������������������������������� carbon�s�������������������������������� �
�Glycolyse������ LegHb
���������������������������������������������������������� ����� +
![]() ���������������������������������������������������������� �� Krebs
���������������������������������������������������������� �� Krebs
��������������������������������������������������������������������������������������������� ATP
���������������������������������������������������������������������������������
H+ ; eˉ

![]() ���������������������������������������������������������� NH4
���������������������������������������������������������� NH4
���������������������������������������������������������� �����
���������������������������������� Acides amin�s����������� NT
![]()
![]()
![]() ��������������������������������������������������������������������������������� ��� N2�������������������������� N2
��������������������������������������������������������������������������������� ��� N2�������������������������� N2
���������������������������������������������� ����������� Prot�osynth�se
���������������������������������� Prot�osynth�se
v Utilisation
de l�azote nitrique :
� Mise en �vidence de la r�duction du NO3ˉ :
![]() Ion nitrique
(NO3ˉ)
Ion nitrique
(NO3ˉ)

![]() ���������������������������������������������� NO3ˉ������������������������������������ Min�ral
���������������������������������������������� NO3ˉ������������������������������������ Min�ral
![]() 15NO3ˉ��������������������������������� NH4
15NO3ˉ��������������������������������� NH4
���������������������������������������������� R�NH�R������ amines
I
���������������������������������������������� R�CO�NH��� amides������������ Organique
���������������������������������������������� N�prot�ines
���������������������������������������������� N�bases azot�es
�������������������������������������������������������������������������������������������������������������������������������� Temps
Exp�rience
d�Eckers en 1924 :
���������������������������������������������� ?��������������������� ?��������������������� ����� ?
![]()
![]()
![]()
![]() ����������������������� eˉ������������������� eˉ������������������� eˉ������������������� ����� eˉ
����������������������� eˉ������������������� eˉ������������������� eˉ������������������� ����� eˉ
![]()
![]()
![]()
![]() ����������� NO3ˉ������������� NO2ˉ������������� N2O2������������� � NH2OH������������������� NH4OH
����������� NO3ˉ������������� NO2ˉ������������� N2O2������������� � NH2OH������������������� NH4OH
![]()
![]()
����������� Nitrate r�ductase������������������������������� Nitrite
r�ductase
� M�canisme de la r�duction du nitrate :
� 1�re �tape avec
1953 :
Evans et Nason sur le soja,
1985 : enzyme cytotonique.
����������������������� NO3ˉ� +� 2H� +� 2 eˉ� �� NO2ˉ� +� H2O
Origine
du pouvoir r�ducteur est en fonction de la localisation de la nitrate
r�ductase :
-
Dans les cellules non
chlorophylliennes : NADH + H+
(respiration)
-
Dans les cellules
chlorophylliennes : NADPH + H+
(photosynth�se)
� le
m�tabolisme de l�azote est li� au m�tabolisme du carbone.
Nitrate
r�ductase : ���������������� (double
cha�ne polypeptidique)



![]()
![]() ���������������������������������� FAD��������������� b 557�������������� Co � Mo�������������������� NO3ˉ
���������������������������������� FAD��������������� b 557�������������� Co � Mo�������������������� NO3ˉ
NADPH, H+



![]()
���������������������������������� FAD��������������� b 557�������������� Co � Mo�������������������� NO2ˉ
![]()
![]()
![]()
![]()
![]()
![]()
![]() ����
NADPH, H+�������� �� FAD �������� 2 Fe2+���� Mo5+�
����
NADPH, H+�������� �� FAD �������� 2 Fe2+���� Mo5+�
![]()

![]()
![]() ���������������������������������������������������������� 2 eˉ���������������� ��� 2 eˉ
���������������������������������������������������������� 2 eˉ���������������� ��� 2 eˉ
![]() ����
NADPH, H+�������� FADH2������� 2 Fe3+���� Mo3+�
����
NADPH, H+�������� FADH2������� 2 Fe3+���� Mo3+�
����������� � 0,32 V��������� � 0,06V
���������������������������������������������� ������� NO3ˉ� ���
NO2ˉ� +�
H2O
���������������������������������������������������������� +
0,42V
� R�action spontan�e (= r�action exergonique)
∆G� = � 34,5 Kcal

Paradoxe :
���������������������������������������������� ������ R�action exergonique
![]()
![]() ���������������������������������������������� A������������������������������������������� B
���������������������������������������������� A������������������������������������������� B
���������������������������������������������� ������ R�action exergonique
� 2�me �tape : R�duction de l�azote
nitrique avec
Exp�rience
de Hageman (1962) sur les chloroplastes
���������������������������������������������� 6 FdOx
![]()
![]()
![]()
![]()
![]() ����������������������� PS
I��������������������������������������������������� Fe 4S 4����������������� 2
eˉ
����������������������� PS
I��������������������������������������������������� Fe 4S 4����������������� 2
eˉ

���������������������������������������������� 6
FdRed
���������������������������������������������� ����� � 0,43 V�������������������������������������� ��� Encore une relation entre
![]() Photosynth�se :���������� SH+ �������������������������������������������������� ����les m�tabolismes de l�azote
Photosynth�se :���������� SH+ �������������������������������������������������� ����les m�tabolismes de l�azote
et du carbone.
���������������������������������������������������������� ���� NO 2ˉ� ��
NH 4+�
+� 2 H2O
��������������������������������������������������������������������������������� + 1,14 V
� transfert spontan� (∆G� = � 95 Kcal)
Exp�rience
de Hageman (1962) sur les proplastes de
champignons et de racines.
����������� 3 NAD(P)H + H+������ 3 FlaP
![]()
![]()
![]()
![]()
![]() ��������������������������������������������������������������������������������� Fe 4S 4����������������� 6
eˉ
��������������������������������������������������������������������������������� Fe 4S 4����������������� 6
eˉ

����������� ������ 3 NAD(P)+���������� 3 FlaPH2
���������������������������������� ������� Flavoprot�ine
![]() ���������������������������������������������������������������������� 6 H+
���������������������������������������������������������������������� 6 H+
![]() Respiration :�������������������������� 2 H+
Respiration :�������������������������� 2 H+
���������������������������������������������������������� NO
2ˉ� ��
NH 4+�
+� 2 H2O
� Origine du pouvoir r�ducteur :
� Relation avec la respiration :
Chlorella
sp.�������������� ����������������������� Volume de d�gagement de
CO2
![]() ����������� Quotient respiratoire : QR =
����������� Quotient respiratoire : QR =
���������������������������������������������������������� Volume
de d�gagement de O2
dissous
-
Obscurit� et absence de NO3ˉ : QR � 1 (constant)
-
Obscurit� et apport de NO3ˉ : QR > 1
Interpr�tation :
![]()
![]()
![]() ����������� ����������������������� NADH + H+�
+� O2����������� ������������������ NADH + H+� +�
O2
����������� ����������������������� NADH + H+�
+� O2����������� ������������������ NADH + H+� +�
O2
![]()
![]() Sans NO3ˉ���������������������������������������������������� Avec NO3ˉ
Sans NO3ˉ���������������������������������������������������� Avec NO3ˉ
���������������������������������� NAD+ ��+ �H2O��������������������� ����������������������� NH 4+� +� NAD+
Lors
de la respiration (obscurit�), il y a comp�tition du NO3ˉ et de
l�O2 pour
le pouvoir r�ducteur.
� Relation avec la photosynth�se :
Chlorella
sp.�� ����������� ���������������������������������� Volume
de d�gagement de O2
![]() ����������� Quotient photosynth�tique : QR
=
����������� Quotient photosynth�tique : QR
=
���������������������������������������������������������������������� Volume
de d�gagement de CO2
dissous
-
Lumi�re et absence d�azote : QR � 1 (constant)
-
Lumi�re et apport de NH4+ : QR � 1
-
Lumi�re et apport de NH4+ : QR > 1
Interpr�tation :
![]()
![]()
![]() ����������� ����������������������� NADH
+ H+� +� CO2���������������������������� NADH + H+� +� CO2
����������� ����������������������� NADH
+ H+� +� CO2���������������������������� NADH + H+� +� CO2
![]()
![]() Sans NO3ˉ���������������������������������������������������� Avec NO3ˉ
Sans NO3ˉ���������������������������������������������������� Avec NO3ˉ
���������������������������������� NAD+ ��+ �sucres�������������������� ����������������������� NH 4+� +� NAD+
Lors
de la photosynth�se (lumi�re), il y a comp�tition du NO3ˉ et de
le CO2 pour
le pouvoir r�ducteur.
v Assimilation
de l�ammonium :
∆ probl�me d�accumulation
� cause du d�s�quilibre qu�il entra�ne chez les autres cations.
|
Environnement |
|
Plante |
|||
|
N
2
NO2ˉ |
Symbiose
(Nitrog�nase) Absorption
dans le sol Absorption
+ NR + NiR |
|
-
Acides amin�s
���������������������������������� ���������������������������������������������������������������������� (Glutamines,
Asparagine)
��������������������������������������������������������������������������������������������� =
mol�cules mobiles et solubles
��������������������������������������������������������������������������������������������� � forme
majoritaire pour le
transport de l�azote (via le
phlo�me)
-
Amides (Glutamates, Aspartames)
� : 3 strat�gies :��������
-
La voie de la
glutamine,
-
L�amination
r�ductrice,
-
La transamination.
� Assimilation de NH par transamination :
� M�canisme g�n�ral :
R�������������������������������� R�������������������������������� R�������������������������������� R�
|�������������������������������� |�������������������������������� |�������������������������������� |
C = O������������� +��������� CH�NH2������� �������� CH�NH2������� +��������� C = O
|�������������������������������� |�������������������������������� |�������������������������������� |
COOH���������������������� COOH���������������������� COOH���������������������� COOH
A. organique 1����������� ����������� A. amin�
2����������������� A. anim� 1����������������� A. organique 2
� Synth�se de l�aspartate :
Aspartate transaminase
Oxaloac�tate� +�
glutamate� ��
Aspartate� +�
a � c�toglutarate
COOH���������������� COOH
|�������������������������� |���������
C = O������������������ CH�NH2�������
|�������������������������� |
CH2��������������������� (CH2)2
|�������������������������� |
COOH���������������� COOH
Aspartate
synthase
Aspartate� +��������� NH3��� ����������� �������� Aspartagine� +�
H2O
COOH���� ����������� (ou NH4OH)�������������� COOH���������� (ou 2 H2O)
|������������������������������������������������������������� |
CH�NH2� ������������������������������������� CH�NH2
|������������������������������������������������������������� |
CH2 ������������������������������������������������������� CH2
|������������������������������������������������������������� |
COOH��������������������������������������������������� CO�NH2
v Conclusions :
� R�gulation de l�assimilation de l�azote :
Exp�rience
sur la lentille d�eau ayant subit une carence en azote pendant 24 �
48H :
Activit�
de
![]()
 ���������������������������������������������������������������������� T�moin
���������������������������������������������������������������������� T�moin
����������������������� NO3ˉ
![]()
![]()
![]() ��������������������������������������������������������������������������������� � + Cytoheximide (inhibiteur de
��������������������������������������������������������������������������������� � + Cytoheximide (inhibiteur de
La
nitrate r�ductase est induite par son substrat. Il s�agit d�un enzyme co�teuse
en �nergie : elle n�est secr�t�e qu�en pr�sence de nitrate (Turn over tr�s
court : quelques heures)
� Assimilation du NO3+ dans les cellules foliaires :
Paroi (pas de s�lectivit� de transport)

![]()
![]() Membrane plasmique����������������������������������� Chloroplaste
Membrane plasmique����������������������������������� Chloroplaste
��������������������������������������������������������������������������������������������� GOGAT
![]()
![]() ��������������������������������������������������������������������������������� Gln
��������������������������������������������������������������������������������� Gln
��������������������������������������������������������������������������������������������������������� 2 Glu
![]()
![]() ���������������������������������������������������������� �� GS�������������������������� Glu���������������� Transamination
���������������������������������������������������������� �� GS�������������������������� Glu���������������� Transamination
![]()
![]() ���������������������������������������������������������������������� ����� NH4+������������������� A.A
���������������������������������������������������������������������� ����� NH4+������������������� A.A
![]() ���������������������������������������������������������������������� � �����NiR
���������������������������������������������������������������������� � �����NiR
![]() ���������������������������������������������� ATP��������������������������� ���������������������������������� � ����Prot�ines
���������������������������������������������� ATP��������������������������� ���������������������������������� � ����Prot�ines
![]() ����������� Transporteur� ����������� ������ (pas
toxique)������������������� NO2ˉ (toxique)
����������� Transporteur� ����������� ������ (pas
toxique)������������������� NO2ˉ (toxique)


![]()
![]()
![]() NO3ˉ� ����������������������� ��� T���������������� NO3ˉ ������������ NR
NO3ˉ� ����������������������� ��� T���������������� NO3ˉ ������������ NR
![]()
![]() Anion������������������������������������������������ Anion� ���������������������������������������������� Vacuole
Anion������������������������������������������������ Anion� ���������������������������������������������� Vacuole
���������������������������������������������� ADP + Pi
�������������������������������������������������������������������������������������������������������������������������������� Stockage
��������������������������������������������������������������������������������������������������������������������� Sans
compartimentation
� Cycle de l�azote dans la biosph�re :
� D�nitrification :
=
Retour de l�azote sous forme nitrite gazeux N2
dans l�atmosph�re.
Chez
les bact�ries h�t�rotrophes pour le carbone (et aussi autotrophes pour le
carbone)
Nitrococcus
denitrificans
Pseudomonas
denitrificans
�� �Prot�ines�������������������������������������������������� N2

![]()
![]()
![]()
![]() ���������������������������������������������� Acides amin�s
���������������������������������������������� Acides amin�s

![]()
![]() Acides
Acides
![]()
![]() C�toniques����� ���������������������������������������������������������� NH4+
C�toniques����� ���������������������������������������������������������� NH4+
 ����������� ��������� �nergie
����������� ��������� �nergie
![]()
![]()
![]() ���������������������������������� NADH + H+�������������������������������������������������
�N2O
���������������������������������� NADH + H+�������������������������������������������������
�N2O
�����������
����������� Catabolisme���
![]() ����������� �nerg�tique���� ����������������������������������������������������������������������
�NO2ˉ
����������� �nerg�tique���� ����������������������������������������������������������������������
�NO2ˉ
![]()
![]() ����������� Substrats�������������������������������������������������������������������������������
�NO3ˉ
����������� Substrats�������������������������������������������������������������������������������
�NO3ˉ
����������� Organiques�������������������������������������������������������������������������������������������������� D�nitrification
![]()
��������������������������������������������������������������������������������������������������������� Nitrate
Surtout
dans les r�gions plus tropicales quand le sol est asphixique (� cause des inondations)
et dans les intersaisons.
� ![]()
 Cycle de
l�azote :
Cycle de
l�azote :
N2



![]() D�jections
D�jections
![]()

![]()
���������������������������������� Prot�ines animales

![]() Putr�faction����� ���������������������������������������������������������������������� �� Fixation
Putr�faction����� ���������������������������������������������������������������������� �� Fixation
![]() ���������������������������������������������������������� Prot�ines v�g�tales���� ���� biologique
���������������������������������������������������������� Prot�ines v�g�tales���� ���� biologique
![]()
![]() ����������� Humification������������������������������������������������������������������������� ����� D�nitrification
����������� Humification������������������������������������������������������������������������� ����� D�nitrification

![]()
![]() ����������� ����������� �� Humus������������������������������� Acide amin�
����������� ����������� �� Humus������������������������������� Acide amin�
�������� Ammonification�������������� ����������� ����������� ����
Amination


![]() ����������������������� ����� NH4+������������������������������� NH4+
����������������������� ����� NH4+������������������������������� NH4+
���������������������������������������������� Absorption

![]()
![]() NO3ˉ
NO3ˉ
![]() ����������������������� Lessivage��������������������� Absorption
et r�duction
����������������������� Lessivage��������������������� Absorption
et r�duction
Dans la plante.������������������������������������ ����������� ����������������������������������������������
Dans le sol.
![]()
![]() Nitrate� "� Nitrite���������������������������������������� NO3ˉ������������������������������������ Nitrite� "� Nitrate
Nitrate� "� Nitrite���������������������������������������� NO3ˉ������������������������������������ Nitrite� "� Nitrate
����������� �NR�������������������������������������������������������������������������������������������������� ����� Nitrification
���������������������������������������������� D�G < 0��������������������� ������� D�G < 0
Pourquoi ? puisque
c�est une r�duction������������� ����������� ����������� Normal,
car c�est une oxydation
���������������������������������������������������������������������� NO2ˉ
Nitrite� "� Ammonium������������������������������������������������������������������� Ammonium� "� Nitrite
����������� NiR�������������������������������������������������������������������������������������������������� �� Nitrosation
(chez les v�g�taux
sup�rieurs)��������������������������������������������������������������� (chez
les bact�ries nitreuses)
![]()
![]()
![]()
![]() Photosynth�se " 8 H+ + 6eˉ������������������������ NO3ˉ������������� ���� 2H+ + H2O
Photosynth�se " 8 H+ + 6eˉ������������������������ NO3ˉ������������� ���� 2H+ + H2O
����������� ���������������������������������������������������������������������������������������������
����������������������� D�G = �95kCal���������� ����������� ����������������������� � ���D�G = � 84 kCal
Pourquoi ? puisque c�est une r�duction�� ����������� ����������� ����������� ����������� Normal, car c�est une oxydation
���������������������������������� 2
H2O������������������������ NH4
�������������� �����”
O2
Autotrophie pour
le Carbone� "� Stockage de l��nergie sous forme de
mol�cules.
Autotrophie
pour l�Azote� "� Utilisation d�un peu d��nergie
v Modalit�s :
� D�finition
:
![]() Le
d�veloppement est constitu� de :
Le
d�veloppement est constitu� de :
![]()
![]() Croissance :� Augmentation
irr�versible de la taille (masse s�che)
Croissance :� Augmentation
irr�versible de la taille (masse s�che)
����������� "
Ph�nom�ne quantitatif
![]()
![]()
![]() Diff�renciation :� Augmentation
irr�versible de la taille (masse s�che)
Diff�renciation :� Augmentation
irr�versible de la taille (masse s�che)
����������� "
Ph�nom�ne qualitatif
�  Croissance
des diff�rents organes :
Croissance
des diff�rents organes :
� Croissance racinaire :
Pas de croissance
��������������������������������������������������������������������������������� ����� observ�e
24 heures
��������������������������������������������������������������������������������� �Zone sp�cialis�e
Traits
�quidistants���������������������������������������������������� pour
la croissance
���������������������������������� Apex��������������
��������������������������������������������������������������������������������� Pas
de croissance

![]() ���������������������������������������������� Cylindre
central
���������������������������������������������� Cylindre
central
���������������������������������� ����������� �
Zone de diff�renciation cellulaire�
= Zone d�histogen�se

� �longation cellulaire
= Zone d�aux�sis
���������������������������������� ����������������������� Quand la paroi est
d�finitivement install�e,
il n�y a plus
de croissance.
��������������� �������������������������������������������������������������������������������������������������������������������������������������������� Faible
ratio noyau /cytoplasme
![]() Zone d�entretien de la coiffe
Zone d�entretien de la coiffe
![]()
![]()
![]() Coiffe������������������������ ����������� �
Multiplication cellulaire
Coiffe������������������������ ����������� �
Multiplication cellulaire
���������������������������������������������� =
Zone de m�r�sis
Centre quiescent
��������������� ���������������������������������������������������������������������������������������������������������������������������� Important
ratio noyau /cytoplasme
�
Croissance
en diam�tre :
Elle est effectu�e par le m�rist�me
secondaire (= cambium) qui n�existe que chez les dicotyl�dones.
�
Ramification
(racines lat�rales) :
![]()
![]()
 �piderme ����������������������������� Xyl�me (s�ve brute, ascendante)
�piderme ����������������������������� Xyl�me (s�ve brute, ascendante)
![]()
![]() ����������� Parenchyme
cortical�������������������������� ����������� ����������� Phlo�me (s�ve �labor�e, descendante)
����������� Parenchyme
cortical�������������������������� ����������� ����������� Phlo�me (s�ve �labor�e, descendante)
![]()
![]() ����������������������� Endoderme���������������� ����������������������� � �����Cylindre central
����������������������� Endoderme���������������� ����������������������� � �����Cylindre central
![]()
![]()
���������������������������������� P�ricycle��������� ����������� ����������� ������ Parenchyme m�dullaire
Les
cellules du p�ricycle sont des cellules diff�renci�es qui subissent une
diff�renciation et deviennent des cellules totipotentes (qui refont une
nouvelle racine)
� Croissance de la tige
(feuill�e) :
M�rist�me d�attente

![]() �bauche
de feuille
�bauche
de feuille
![]() R�g�n�ration des cellules utilis�es
pour les �bauches foliaires
R�g�n�ration des cellules utilis�es
pour les �bauches foliaires
![]() ���������������������������������������������������������������������� M�rist�me
m�dullaire
���������������������������������������������������������������������� M�rist�me
m�dullaire

![]() M�rist�me d�attente
M�rist�me d�attente
��������������������������������������������������������������������������������������������� L�anneau
initial est � l�origine
![]() ��������������������������������������������������������������������������������������������� de
la prochaine �bauche foliaire
��������������������������������������������������������������������������������������������� de
la prochaine �bauche foliaire
Anneau initiale
� R�gulation
hormonale de la croissance :
On
ne s�int�resse qu�aux facteurs endog�nes :
-
Compos�s oligotrophiques (en trop
petite quantit� pour dire qu�ils ont un r�le nourricier "
inint�ressant)
-
Phytohormones�������������������������������������� (�
Hormones animales)
"� Hormonologie
Structures tr�s vari�es dans une m�me
famille.
Dans une m�me famille "
plusieurs fonctions.
Selon l��quilibre hormonal, il y a des cons�quences totalement diff�rentes
"� Endocrinologie
1 hormone�
�"� 1 structure�
���
"� 1 fonction
On
a �tabli 4 crit�res pour qu�une mol�cule soit une hormone v�g�tale :
-
Sp�cification dans le cycle de
synth�se,
-
Mol�cule active � tr�s faible
concentration,
-
Site d�action diff�rent du site
de synth�se (valeur de signal),
-
Nature universelle de l�hormone
(m�me structure dans diff�rentes esp�ces)
v Les auxines :
Il
a fallu 50 ans pour les d�couvrir et faire accepter leur existence.
Travaux
sur le col�optile d�avoine :
 ���������������������������������� Col�optile
(= gaine de protection de la premi�re faille)
���������������������������������� Col�optile
(= gaine de protection de la premi�re faille)
![]() ���������������������������������������������� Racines
s�minales (3 pour les monocotyl�dones)
���������������������������������������������� Racines
s�minales (3 pour les monocotyl�dones)
![]()
![]()
![]()
![]() Faisceau
intense sur l�apex
Faisceau
intense sur l�apex
![]()
����������������������� Obscurit�
��������������������������������������������������������������������������������������������� Il
excite forc�ment 2 sites (au moins) :
-
Un de perception,
-
Un de r�action.���������������
"
Transmission d�un signal
� Auxines
et grandissement cellulaire :
� D�couverte de l�AIA
(principales �tapes) :
Exp�rience
sur le col�optile d�couvert :
 j
j
![]() �����������
�����������
��������������������������������������������������������������������������������� Apex
juste repos�
���������������������������������������������� "
����������� Plus de croissance������������������ Reprise de la croissance
�� L�apex contr�le la croissance du col�optile.
Mais le contr�le est de quelle nature ?
|
Plaque de platine |
Permet un signal �lectrique |
� |
|
Couche lipidique |
Permet un signal chimique
lipidique |
� |
|
Couche de mica |
Emp�che tout type de signal |
� |
|
Bloc de g�lose |
Permet un signal chimique
hydrophile |
� |
![]() k
k
����������������������������������
l
![]() ���������������������������������������������� "
Reprise de la croissance
���������������������������������������������� "
Reprise de la croissance
���������������������������������������������� � La
g�lose mime l�apex car elle contient des mol�cules hydrophiles.
![]()
![]()
![]()
 m
m
 ���� Col�optile de
monocotyl�done���� Tige de dicotyl�done d�capit�e
���� Col�optile de
monocotyl�done���� Tige de dicotyl�done d�capit�e
L�AIA
(acide indole_3_ac�tique) est l�auxine naturelle la plue r�pandue.
Elle
peut �tre libre ou fix�e � d�autres radicaux.
Il
existe d�autres auxines moins naturelles et d�riv�es de l�AIA, mais elles
pr�sentent un rendement plus faible. On y trouve :
-
Les auxino�mim�tiques (de
synth�se),
-
Les r�gulateurs de croissance,
-
Les d�sherbants.
L�AIA
est une mol�cule thermolabile et photosensible : elle est d�grad�e sous
les effets de la chaleur et de la lumi�re.
Les
auxino�mim�tiques sont non sensibles � la chaleur et � la lumi�re.
Dans
le cas d�une lumi�re anisotrope (in�gale) :
-
L�auxine est d�truite l� o� il y
a de la lumi�re,
-
Et elle est produite l� o� il n�y
a pas de lumi�re
"� Les cellules � l�ombre s�allongent et il y a
une courbure vers la lumi�re.
� Dosages :
�
Dosage
biologique de l�AIA = test de Went (ou test avoine) :
 Les
lieux de synth�se de l�AIA sont tr�s sp�cifiques : l�apex foliaire et les
organes reproducteurs.
Les
lieux de synth�se de l�AIA sont tr�s sp�cifiques : l�apex foliaire et les
organes reproducteurs.
a
![]() ����������������������������������������������������������������������
����������������������������������������������������������������������
 � �����20
� �����20
���������������������������������������������������������������������� "
Croissance asym�trique
������ 10
![]() ���������������������������������������������������������� AIA
(10�7 g.mol�1)
���������������������������������������������������������� AIA
(10�7 g.mol�1)
����������������������� 1��������� 2��������� 3
�
Dosage
par analyse physico�chimique :
j� Chromatographie d�extraits naturels :� Test de Salkowski (1885) qui donne la
concentration � 10�5
g.mol�1 pr�s� (m�thode moins pr�cise mais plus pratique)
k� Couplage chromatographie et spectrom�trie de
masse :�
sensibilit� importante (d�tection d�une quantit� de 5 � 10 ng)
l� M�thodes immunologiques :� Test �lisa : sensibilit� �norme
(d�tection d�une quantit� de 0,1 ng)
� Transport :
Le
transport de l�AIA est polaris� (ou vectoriel) : de l�apex vers la base.

���������������������������������� ������ Segment sous�apical
��������������������������������������������������������������������������������������������������������� "� Reprise de la croissance
�� Il y a bien un transport de l�AIA.

��������������������������������������������������������������������������������������������� "� Pas de reprise de la croissance
Le
m�canisme du transport polaris� de l�AIA se fait dans les cellules du liber.

![]() Paroi������������������������������������������������������������������������������������� neutre
�lectriquement
Paroi������������������������������������������������������������������������������������� neutre
�lectriquement
��������������������������������������������������������������������������������������������������������� "
Elle peut franchir le
��������������������������������������������������������������������������������������������������������������������� plasmalemme�
Plasmalemme
Cytosol
![]() ��������������������������������������������������������������������������������������������������������� Transporteur
+ ATPase
��������������������������������������������������������������������������������������������������������� Transporteur
+ ATPase
��������������������������������������������������������������������������������������������������������������������� (au
p�le basal)
� M�tabolisme de l�AIA :
�
Synth�se
de l�AIA :
Il
existe 2 voies de synth�se.

Le
pr�curseur de l�AIA est le Tryptophane :
����������� Ou�
� I � pour le noyau imidazole :

���������������������������������������������������������������������������������������������


�
Acide c�tonique������������������������������������������������������
![]()
 Transamination������������������������������������������������������������������� D�carboxylation
Transamination������������������������������������������������������������������� D�carboxylation
����������� Acide amin���������������������������������������������������
���������������������������������������������������������������������� ����������� CO2
I � CH2 � CO � COOH������������������������������������������������������ I
� CH2 � CH2 � NH2
Acide
indol_pyruvique������������������������������������������������������������ Tryptophane


![]() ��������������������������������������������������������������������������������������������� ���� H2O
��������������������������������������������������������������������������������������������� ���� H2O
D�carboxylation������������������������������������������������������������������� ����������� D�samination oxydative
����������������������� CO2�������������������������������������������������������������� NH3 + H+
���������������������������������������������� I
� CH2 � CHO
![]()
![]()
![]() ���������������������������������������������� Indol_ac�tald�hyde
���������������������������������������������� Indol_ac�tald�hyde
����� Voie principale������������������������������������������������� Voie privil�gi�e
dans l�apex de col�optile
![]() ����������������������� ������� H2O + NAD+
����������������������� ������� H2O + NAD+
����������� ����������� Oxydation
����������������������� �������� NADH + H+
�����������
���������������������������������������������� I
� CH2 � COOH
���������������������������������������������������������� AIA
�
Catabolisme
de l�AIA :
De
trop grandes quantit� d�auxines causent une prolif�ration cellulaire
d�sorganis�e. Il existe donc des enzymes de d�carboxylation oxydative :
les auxines oxydatives.
Il existe d�autres possibilit�s de
r�actions cataboliques, comme la r�gulation par la fixation de l�AIA . Tant que celle� ci est conjugu�e,
elle n�est plus fonctionnelle.
���������������������������������������������� I
� CH2 � COOH
���������������������������������������������������������� AIA
 ���������������������������������������������� O2
���������������������������������������������� O2
����������������������� �������� CO2 + H2O����������������������������������������������������������������������������������������
Oxy_indole_3_m�thyl�ne
��������������������������������������������������������������������������������������������������������� Indole_3_ald�hyde
� Mode d�action de l�AIA :
L��longation
concerne les cellules jeunes, o� il n�y a encore que la paroi IAIRE
de d�velopp�e.
Sch�ma
de la paroi IAIRE :
![]()
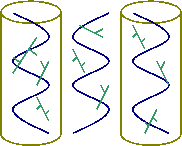 Myofibrille
Myofibrille
![]() = Trame
= Trame
![]()
![]() ���������������������������������������������������������������������� Pectine
(pouvoir g�lifiant)
���������������������������������������������������������������������� Pectine
(pouvoir g�lifiant)
���������������������������������������������������������������������� H�micellulose
(plus petite et ramifi�e)���������� Matrice
���������������������������������������������������������������������� +
Extensine (15%)
���������������������������������������������������������������������� (
surtout des liaisons hydrog�ne et ionique
���������������������������������������������������������������������� "� liaisons labiles)
�
Les
polym�res pari�taux :
j� La cellulose :������� b
(1�4)glucane
Les
liaisons b
(1�4) entra�nent une forme en h�lice et apporte une grande solidit� � la
cellulose (indigeste)
Les
liaisons a
(1�4) entra�nent une forme plane et concerne l�amidon.
k� Les h�micelluloses :�������� (tr�s grande famille)
Il
s�agit d�h�t�ropolym�res (= combinaison de diff�rents polym�res)
l� Les pectines :������ a
(1�4)galacturonanes
On
observe une fonction carboxylique libre. Les pectines sont pr�sentes dans la
paroi IAIRE.
����������������������� COOˉ L H+������������� COOˉ L H+ ����������� ����������� �COOˉ L H+

Les
cations bivalents jouent le r�le d�une pince � linge pour relier 2 pectines.
m� L�extensine :�������� glycoprot�ines � hydroxyproline��������
MM = 86 kDa� "� 300 acides amin�s���������������������������������� ⅔ d�oses et ⅓
d�acides amin�s
�
Les
effets de l�AIA :
j� Augmentation de la plasticit� de la
paroi :
Exp�rience
de Heyn (1991) puis Tagawa et Bonne (1957) :

���������������������������������������������� 20
minutes
���������������������������������������������������������������������� On
retire de poids
��������������������������������������������������������������������������������� 5
minutes
a

���� at�
����������������������� +
AIA������������������������������������ ����������������������� ae�
���� at� ��������������������������������������������������������������������������������������������������������� ap�� >>>� ap
��������������������������������������������������������������������������������� ��ae��� ap�
����������������������� �T�moin�������������������������������������������� � ap
����������� 0�������������������������������������������� 20������� ���������
25��������� (minutes)
k� Stimulation de l�extension pari�tale :
![]() Milieu physiologique�� ���������������������������������������������� ����������� Segment
d�hypocotyle de soja
Milieu physiologique�� ���������������������������������������������� ����������� Segment
d�hypocotyle de soja
�� (pH = 7��
�
AIA)
D
longueur (�m)

1500
����������� pH������ pH������ ����������� + AIA
����������� � 7������� � 5
���������������������������������������������� �T�moin (toujours
un peu d�AIA dans la plante)
�� 0
����������� ��
����0�������������� 20������������������������������������������ 90������� (minutes)
Cytosol

�������������������������������������������������������������������������������������������������������������������������������� �� AIA
��������������������������������������������������������������������������������������������������������� ���� Pompe � proton inactive
��������������������������������������������������������������������������������������������������������� �����
��������������������������������������������������������������������������������������������������������������������� � ATP
������������������������������������������������������������������������������������������������������ H+
��������������������������������������������������������������������������������������������������������� �� ����Pompe � proton active
��������������������������������������������������������������������������������������������������������������������� � ADP + Pi
L�acidification
de la paroi entra�ne une perte de coh�sion et donc une plus grande plasticit�.
� On
fait de la place en �cartant les livres pour pouvoir en ranger d�autres �
l� Stimulation du m�tabolisme :
Exp�rience sur l��picotyle de pois +
AIA :
 Unit�s
relatives
Unit�s
relatives
15
��������������������������������������������������������������������������������������������� Cellulose
10����������������������������������������������������������������������������������������� (petit
effet retard)
��������������������������������������������������������������������������������������������� ARNM celluloase
�5
�1
����������� ���
0����������������� 12������������������� 24������������������������������ 48������� (heures)
L�AIA
induit la transcription et la traduction.
"
Effet � court et moyen terme.
|
R�sum� |
|
|
Au
niveau pari�tal (quelques
minutes) |
Au
niveau mol�culaire (quelques
heures) |
|
Extrusion
de H+ $ Perte
de coh�sion Trame
/ Matrice
|
Activation
de la transcription $ Activation
de la traduction
Synth�se
d�enzymes (remaniement
des polym�res pari�taux) |
![]()
Extension de la paroi
= croissance par �longation cellulaire
� Liaisons auxines �
r�cepteurs :
Il
existe 2 types de r�cepteurs.
Tr�s
mal connus�
"
Comparaison des points communs des structures des phytohormones de type
auxines.

�
Auxines
de synth�se :
:
AIA
-
 Acide
a_naphtal�ne
ac�tique
Acide
a_naphtal�ne
ac�tique
= ANA
-
 Acide
a_naphtal�ne
oxyac�tique
Acide
a_naphtal�ne
oxyac�tique
-
 Acide
2,4_dichloroph�noxyac�tique
Acide
2,4_dichloroph�noxyac�tique
= 2,4�D
C�est la plus puissante. ���������������������
Elle est utilis�e, en grande quantit�,
comme d�sherbant puissant par multiplication.
En
plus, elle est biod�gradable.
-
 Acide
2,4,5_trichloroph�noac�tique
Acide
2,4,5_trichloroph�noac�tique
= 2, 4, 5�T
-
Acide� 2_m�thyl_4_chloroph�noac�tique
 =
MCPA
=
MCPA
�
Points
communs :
j� La cha�ne lat�rale doit �tre courte :
����������� AIA :� I�CH2�COOH
����������� AIP :� I�CH2� CH2�COOH������������� moins
efficace
����������� AIB :� I� CH2� CH2� CH2�COOH������������� beaucoup
moins efficace
����������������������� I�CH2� CH2� CH2� CH2�COOH�������������� plus
d�activit�
k� Pr�sence d�un protons H libre en position
� ortho � :

 ����������� 2, 4�D����������������������������������������������������������� 2, 6 D
����������� 2, 4�D����������������������������������������������������������� 2, 6 D
����������� ��������������������������������������������������������������������������������������������������������������������� Pas
d�activit�
l� le noyau doit pr�senter des doubles liaisons
(= liaisons �thyl�niques) :
d+
����������� Acide
benzo�que�������������������������������� Acide
cyclohexano�que


����������� ��������������������������������������������������������������������������������� Pas
de mouvements des charges
Th�orie
de Kenneth Thimann (1904 � 1997) :
 AIA��������������������������������������������������� 2,
4 D
AIA��������������������������������������������������� 2,
4 D


 �
�
R�cepteur � 2 points d�ancrages �
une distance pr�cise
� Auxines
et multiplication cellulaire :
Les
effet des auxines sont doses�d�pendants.
-
Grandissement cellulaire� = Aux�sis
Pour de faibles concentration :��������� [ AIA ] = 10�7
� 10�11 g.mL�1
-
Multiplication cellulaire :
���������������������������������� [
AIA ] = 10�2 � 10�6
g.mL�1
-
Organogen�se :
[ AIA ] = 10�7
� 10�6 g.mL�1
� Mise en �vidence :
�
Prolif�ration
cellulaire non contr�l�e, anarchique :
Soit
des fragments v�g�taux dans un milieu g�los� ou aqueux��������� +� [ AIA ] = 10�2 g.mL�1
![]()
����������� 4 semaines
Obtention
de � cal � (= amas de cellules ressemblant � une tumeur)
S�il
l�on ajoute de l�AIA, la prolif�ration continue ; sinon,� il y a un arr�t de la croissance.
�
Prolif�ration
cellulaire organis�e :

Phlo�me
��������������������������������������������������������������������������������� Cambium
( 3 couches de cellules )
![]()
Xyl�me��������������������������������������������������������������������������������� +� [ AIA ] = 10�6 g.mL�1
��������������������������������������������������������������������������������� 8
assises (= couches) cellulaires
� �Action cambio�stimulante de l�AIA.
� Cas de crown gall :
Gall
=� multiplication cellulaire en d�sordre,
due � une piq�re d�insecte.
����������������������� �
Crown
gall =� multiplication cellulaire en
d�sordre, due � une bact�rie
(Agrobacterium
temufaciens)
Le
crown gall est une tumeur naturelle (qui se manifeste sur un tissu jeune) On
parle aussi de tumeur IAIRE
qui correspond au point de d�part de l�infection.
Les bact�ries sont en multiplication et
causent un exc�s d�auxines.


![]() ���������������������������������� renferme les
bact�ries
���������������������������������� renferme les
bact�ries
![]()
![]() ����������������������
����������������������
Lorsque la tige grandit :������������������������������������������������������� Tumeurs
secondaires
Elles ne contiennent pas l�agent
infectieux.
Les
cellules se multiplient m�me sans apport d�AIA.����������������������� �� Habituation hormonale
Les
cellules des tumeurs IAIRES
ont acquis la capacit� de synth�tiser l�AIA alors qu�elle � tait r�serv�e
� l�apex.
����������������������� "� Il y a eu un transfert d�informations
g�n�tiques de la bact�rie � la plante.


 ADN bact�rien��������������������������������������������� ����������� ����������� Plasmide Ti� (Tumeror inducing)
ADN bact�rien��������������������������������������������� ����������� ����������� Plasmide Ti� (Tumeror inducing)
��������������������������������������������������������������������������������������������������������� ���� responsable de la tumeur

���������������������������������������������������������������������� G�ne
de r�plication
G�ne de virulence�����������������������������������������
����������������������� ����������������������� ������ TL������������ �
TR�����
����������� ADN de transfert������ ����������������������� ����������� S�quences de bordure (TL et TR)
����������� ������ (ADNT)
���������������������������������� Production d�opine (= facteur de
croissance de la bact�rie) et d�enzymes v�g�tales
���������������������������������� et
g�nes ONC responsables de l�ontogen�se
�
Production
de plante transg�ne (OGM) :
j� Fabrication d�un vecteur de transfert :
����������� "
Utilisation d�enzymes de restriction pour retirer les g�nes responsables de la
tumeur et ins�rer le g�ne d�int�r�t.
���������������������������������� ������ 1�������������� ��� P ���� ��P������� �������� �1
![]()
���������������������������������� �� S�lection
v�g�tale��� � G�ne d�int�r�t
k� Transformation bact�rienne :

���������������������������������� GSB
G�ne de s�lection bact�rienne
���������������������������������� �������� TL �������������������������������� ���������TR
���������������������������������������������� �1������������������������������� ������� 1
���������������������������������������������� GSV��� ����������������������� �G�ne d�int�r�t
���������������������������������������������������������� �� P������ ����� P
l� S�lection :
On
effectue une culture avec un antibiotique sp�cifique.
"� Seules les bact�ries modifi�es survivent, les
autres meurent.


m� Transformation de plantes par Agrobacterium
GM :
Plante
m�re��� ���� Disques foliaires scarifi�s�� �����
Incubation en pr�sence de Agrobacterium GM
����������������������� "������������������������������������������� "
Milieu
de s�lection des cellules ��������� Antibiotique
pour d�truire
����� transform�es (GSV)�������������������� �� les
bact�ries restantes

���������������������������������������������� "
n� Quelques applications (g�nes d�int�r�t) :
-
R�sistance aux
insectes (ma�s, coton, pomme de terre, colza),
-
R�sistance aux
herbicides,
-
R�sistance aux
virus (tabac, laitue, colza, pomme de terre),
-
R�duction des
introns azotes (optimisation de l�azote donn�),
-
Am�lioration des qualit�s
nutritives :
Huile plus riches en acides gras
essentiels avec modification que de la graine,
Composition
de l�amidon de pomme de terre,
-
R�sistance aux
stress abiotiques (froid, s�cheresse, sols sal�s, etc.),
-
Production de m�dicaments
(prot�ines humaines, h�moglobine, etc.)
"
Il y a un avantage sur les bact�ries GM (en plus de la biomasse) : la
pr�sence de g�ne effecteur de g�nes (activateur)
o� Quelques probl�mes :
-
R�sistance aux
antibiotiques (dont la canabicine) qu�il vaut mieux ne pas diffuser,
-
Les partielles exp�rimentales
n�cessitent un p�rim�tre de s�curit� avec interdiction de faire pousser des
hybrides pouvant s�auto�croiser avec l�OGM.
Ma�s :� OK, il n�y a pas d�hybrides,
Colza : plus probl�matique car il y a une hybridation
possible avec la ravelle.
����������� "
Probl�me de dispersion.
-
Probl�me d��thique avec les
manipulation du vivant.
� Auxines
et organogen�se :
� Rhizogen�se :
j� Bouturage de la vigne Vitis
vinifera :
![]() ���������������������������������������������������������������������� Bourgeon
auxiliaire (v�g�tatif)
���������������������������������������������������������������������� Bourgeon
auxiliaire (v�g�tatif)

![]() ���������������������������������������������������������������������� AIA ?
���������������������������������������������������������������������� AIA ?
![]()
![]() Sable humide������������� ���������������������������������� ����������� Racines
adventives
Sable humide������������� ���������������������������������� ����������� Racines
adventives
Le
bourgeon auxiliaire est n�cessairement obligatoire pour avoir des racines.
Comme il est v�g�tatif, il n�y a pas de photosynth�se.

 k� D�cortication annulaire :
k� D�cortication annulaire :
���������������������������������������������� ��� "
Ce qui fait qu�il y a des racines passe par le Phlo�me.
L�AIA y passe�






l� Exp�rience de Cooper (1935) sur Citrus
sp. :
Bouture :������������������������������������������������������������������������������������������ Rebouture :
![]()
AIA :
10�5 g.mL�1���������������������������������������������������������������������������� Plus
de racines adventives
"
Les compos�s endog�nes
oligotrophiques jouent un r�le de r�gulation
(des compos�s macrotrophiques n�ont pas
�t� trouv�s)
"
La rhizogen�se est due � l�AIA et � des compos�s oligotrophiques (vitamines)
� Caulogen�se :
j� Exemple avec une plante tropicale Allopectus :
 "
N�oformation de bourgeon sur une feuille
"
N�oformation de bourgeon sur une feuille
![]()
![]()
![]() Sable
humide����������������������������������������������������������������������������������� Blessure � l�apex de la feuille
Sable
humide����������������������������������������������������������������������������������� Blessure � l�apex de la feuille
(trou)
![]() ����������������������� �������� Nervure principale �paisse
����������������������� �������� Nervure principale �paisse
|
[AIA]� =� 10�8
g.mL�1 |
" |
Bourgeons
adventives |
|
[AIA]� >�
10�8 g.mL�1 |
" |
Bourgeons et
racines adventives |
|
[AIA]� =� 10�5
g.mL�1 |
" |
Racines
adventives |
|
[AIA]� >�
10�5 g.mL�1 |
" |
Gall |
![]()
![]()
![]() ���������������������������������� ����������� AIA
���������������������������������� ����������� AIA

����������� ���
�?
k� Exemple avec Crambe
maritima (chou
avec une grande racine) par Stroughton et Plant (1940) :
Soit
un segment de longueur variable :
����������������������� �8 cm ������������� ����������������������������������������������������������������������
2 cm

����������� Gradient d�AIA
��������������������������������������������������������������������������������������������� ����������� Gradient d�AIA
����������������������� �������� "��������������������������������������������������������������������������������� ��� "
�������������������������������������������������������������������������������������������������������������������������������� �Caulogen�se
����������������������� ����������� ��
Surtout de la rhizogen�se
� Quelques applications :
|
|
|
|
|
|
�j� Bouturage :
k� Marcottage :
 On
retrouve cette application dans la nature chez les fraisiers. On peut la
r�aliser artificiellement :
On
retrouve cette application dans la nature chez les fraisiers. On peut la
r�aliser artificiellement :
-
Marcottage par couchage :
-
 Marcottage
a�rien :
Marcottage
a�rien :
 l� Exp�rience de Nitsch (1950) :
l� Exp�rience de Nitsch (1950) :
����������� ����������� La
fraise est un polyak�ne (plusieurs fruits)
Apr�s
f�condation :
-
On retire les carpelles :
"� La fraise ne grossit pas.
-
Si on n�en laisse qu�un :
"� Atrophie l� o� il n�y a pas de carpelles.
-
On retire les carpelles et on
pulv�rise de l�AIA :
"� Obtention de fruits parth�nocarpiques.
(=
production de fruits sans qu�il n�y ait eu
d�veloppement
d�une graine, naturelle ou mim�e)
Exemple :
|
|
Parth�nocarpe
naturelle ? |
Induction
par les auxines |
|
Tomate |
Oui S�il
y a un stress (m�canique, ou abiotique) ou une pollinisation inter esp�ce |
AIA ;
AIP ; AIB ; ANoA |
|
Aubergine |
Non |
AIA ;
2,4�D ; ANA ; DefH9�iaaM
(= trang�ne chim�rique) |
|
Banane |
Oui Par
s�lection vari�tale et avec un meilleur rendement |
AIA ;
2,4�D ; ANA |
|
Concombre |
Oui (contr�le
g�n�tique) |
AIA ;
2,4�D ; ANA |
Cela permet d�obtenir des fruits plus
nombreux, d�augmenter le rendement et de faire de la culture hors saison.
m� Culture in vitro :
La
1�re culture a �t� effectu�e par Roger Jean Gautheret (1910 � 1997),
pr�sident de l�acad�mie des Sciences.
n� D�sherbage hormonal :
Il
s�agit de l�accumulation des auxines de synth�se, entra�nant une prolif�ration
cellulaire l�tale.
"
Il consiste en un herbicide
s�lectif : les monocotyl�dones (= gramin�es) deviennent plus r�sistantes.
Il
diff�re du d�sherbage chimique comme avec le chlorate. Ce dernier est un
analogue du nitrate. Il n�y a aucune diff�rence pour la plante mais la NR ne le
reconna�t.
"
Il y a une accumulation l�tale et une r�manence longue dans le sol.
Alors que le d�sherbant hormonal est
biod�gradable.
v Les gibb�rellines :
� D�couvertes
et structures :
� D�couverte :
Dans
les rizi�res, les cultivateurs asiatiques observaient des �longations anormales
des entre�n�uds. Ce gigantisme entra�nait la verse puis la st�rilisation par
�puisement.
"� � foolish
seedlings �� =� � bakanae �� =�
� plantes�folles �
En 1926, Eiichi Kurosawa a d�couvert un
champignon parasite � la base des plantes�folles (riz) Il s�agit d�un
ascomyc�tes : Gibberella funjikoro�
En
pulv�risant un broyat de ces champignons sur du riz sain, il observa de nouveau
le gigantisme.
� Structure :
-
1939 :� La mol�cule active est isol�e et purifi�e par
cristallisation,
-
1956 :� La structure est �lucid�e.

Noyau
gibb�rellane :
���������������������������������������������������������������������������������
��������������������������������������������������������������������������������������������� (num�ro
d�ordre de d�couverte)

��������������������������������������������������������������������������������� ����������� Pont formant un autre cycle
�
�� GA 3� =
acide gibb�relique
(le plus puissant des
gibb�rellines)
� R�le
:
-
Lev�e de la dormance
embryonnaire,
-

 Lev�e de la
� dormance � des bourgeons axillaires,
Lev�e de la
� dormance � des bourgeons axillaires,
-
�longation des entre�n�uds.
![]()
����������������������� Pois nain
���������������������������������������������������������� Pois
WT�������������������� Pois nain� +� 10
ng de GA 3
� Modes
d�action :
� Synergisme gibb�rellines �
AIA :
Exp�riences
sur les jeunes tiges :
![]() j
j
����������������������� Apex coup����� "� Pas de
croissance.
![]()
k
���������������������������������� "� Pas de
croissance.

 l
l
���������������������������������� � "���������������������������������������������������������������������������� "
�� Synergie
Gibb�relline � AIA pour l��longation cellulaire.
Les
gibb�rellines favorisent la synth�se de l�AIA :
-
Augmentation de la
transcription :
-
Prot�ase pour la prot�olyse,
-
Cellulase : enzyme cl� de
l��longation cellulaire.
-
Augmentation de la stimulation de
l�anabolisme protidique :
 GA3��������������������� Acide
pyruvique��������������������� Ac�tyl_CoA
GA3��������������������� Acide
pyruvique��������������������� Ac�tyl_CoA
Acide ac�tique (
���������������������������������������������� Acide oxaloac�tique
����������� Acide malique����������������������������������������������������������� Acide
citrique
���������������������������������������������� ������ KREBS
����������� Acide succinique������������������������������������������� Acide ac�toglutarique
��������������������������������������������������������������������������������� Acide
glutamique������������������ Prot�ines
� Applications
:
� Floraison des bisannuelles
ornementales :
Ces
plantes ont un cycle de 2 ans avec une floraison la 2�me ann�e. Avec
les gibb�rellines, la floraison est donc contr�l�e et rapide.
� Obtention de fruits
parth�nocarpiques :
Les
gibb�rellines sont identiques que les auxines mais pour des esp�ces
diff�rentes.
� � Raccourcissement �
des c�r�ales par des anti-gibb�rellines :
Ils
interf�rent avec les gibb�rellines.
Exemples :
-
Le chlorure de
2_chloro�thyl_trim�thylamonium (CCC),
-
Le Cycocel (chlorure de
chlorm�quat)
v Les cytokinines :
Kines = division��������� Cyto
= cellulaire
� D�couverte
:
-
Johannes Van Overbeck (1941) a
effectu� une culture d�embryon isol� in
vitro de Datura avec l�apport de lait de coco et d�AIA.
-
Stewart et Shantz (1954) ont
d�couvert la diph�nylur�e :
![]()
NH -
CO - NH
Le probl�me est que cette mol�cule
d�couverte n�est pas universelle.
"
Elle n�est donc pas une hormone mais juste un facteur de croissance.
-
Folke K. Stkoog (1908 � 2001) a
travaill�, en 1956, sur des cultures de tissus de tabac et a remarqu� le besoin
d�une mol�cule avec une base structurale d�ad�nine (que l�on trouve en grande
quantit� dans le sperme de hareng)
"
Il s�agit de la 1�re cytokinine isol�e :
 ����������������� 6_furfuryl_aminopurine (ou
6_furfuryl_ad�nine)
����������������� 6_furfuryl_aminopurine (ou
6_furfuryl_ad�nine)
En fait, il s�agit d�une
cytokinine de synth�se (pas pr�sente dans la plante mais de bon march�)
-
D. S. Letham (1963) a d�couvert
la 1�re cytokinine naturelle dans le ma�s : la z�atine.
Prix hors taxe : ��������� 29,30�
les 5 mg
���������������������������������� 59
� le gramme
-
Les cytokinines de
synth�se :
-
La benzyl_aminopurine� (BAP)�
ou benzyl_ad�nine :

Il s�agit de la cytokinine la plus
active.
Les
cytokinines sont synth�tis�es dans les racines, graines et fruits. On les
retrouve dans les parties a�riennes de la plante via la s�ve montante.
� Action
sur la croissance :
� Stimulation des divisions
cellulaires :
Exemple
de cultures de moelle de tabac in vitro :
-
Sans hormone :��� "� Pas de division, pas d��longation,
-
Avec de l�AIA :���� "� Elongation cellulaire mais pas de division,
-
Avec des cytokinines :������ "� Divisions cellulaires mais pas d��longation,
-
Avec les 2 (lait de coco) :�� "� Divisions et �longation cellulaires.
�� Il y une
synergie pour les divisions cellulaires.
Test
de Skoog :
Pour savoir si un tissu contient des
cytokinines, on ajoute au tissu de l�AIA.
S�il y a des divisions cellulaires, il y
a des cytokinines.
� Caulogen�se :
Travaux
sur des fragments de Funaria in vitro :
���������������
Nombre
de bourgeons adventifs
 ����������������������� (en unit� relative)
����������������������� (en unit� relative)
�� 1000
���������������������������������������������������������� � Avec cytokinines
��� 100����������������������������������������������������������������������� ����������� � Sans cytokinines
���������������������������������� 10������������������� 14������������������� 16������������������� Temps
Exemple
de balances hormonales :
|
|
AIA |
Cytokinine |
|
|
Balance
auxinique : |
2.10�6
g.mL�1 |
10�8
g.mL�1 |
"� Racine |
|
Balance
cytokinique : |
2.10�6
g.mL�1 |
Plus
de 10�8 g.mL�1 |
"� Bougeon |
Si
la balance est mal ajust�e, il y a soit aucun effet, soit l�effet inverse.
Si
on remplace l�AIA par l�ABA, il faut revoir la balance.
v Acide abscissique et
�thyl�ne :
� La
chute des feuilles :
Les
effecteurs (climatiques et etc.) sont : la s�cheresse, les jours
courts, la comp�tition inter�organes, etc.
Au
niveau d�un n�ud :
 ����������������������� Tige��������������������������� P�tiole
����������������������� Tige��������������������������� P�tiole
![]()
![]() ���������������������������������������������������������������������� Couche
r�g�n�ratrice (cellules pallissadiques)
���������������������������������������������������������������������� Couche
r�g�n�ratrice (cellules pallissadiques)
��������������������������������������������������������������������������������� Elle
appara�t en 1�re.
���������������������������������������������������������������������� Couche
d�abscission
��������������������������������������������������������������������������������� Elle
est mise en place par la couche r�g�n�ratrice
����������������������������������������������������������
���������������������������������������������������������� Les
2 couches forment la zone d�abscission.

La couche d�abscission est le si�ge de
s�cr�tions d�enzymes de d�gradation : les � ases � (cellulase,
etc.)
Elle entra�ne ainsi :
-
la digestion cellulaire de la
couche r�g�n�ratrice,
-
la s�cr�tion de li�ge
cicatrisant,
-
et la chute par mouvement
m�canique.
� R�gulation
hormonale :
� Intervention des
auxines :
j
�Concentration en AIA dans les feuilles lors de
la chute en automne :
����������� En jours longs, la concentration en
AIA est constante.
����������� Durant les jours courts, celle�ci
diminue.
k
�Un
apport d�AIA retarde la chute des feuilles, exp�rience sur le Coleus :
����������� Si on supprime le limbe (source de
l�AIA), il y a la chute du p�tiole.
����������� Si on remplace le limbe par un bloc
imbib� d�AIA, il n�y a pas de chute.
� Intervention des
cytokinines :
j������ Lors d�un stress hydrique, les feuilles
tombent.
����������� Si on applique des cytokinines (10�5
g.mL�1) sur
une feuille basale, celle�ci �chappe � la s�nescence comme s�il s�agissait
d�une jeune feuille
feuille basale = feuille � la base de la tige, donc
plus ancienne
k������ Si on apporte des cytokinines sur un seul
cot� de la feuille (10�5
g.mL�1), on
observe une concentration en AIA diff�rente de part et d�autre de la
feuille :
-
-
��
Les cytokinines ont un r�le indirect sur la s�nescence en faisant
augmenter la concentration en AIA.
� R�le de l��tyl�ne :
H2C 9 CH2
Il
s�agit d�un gaz, il peut donc diffuser facilement d�un tissu � un autre.
Il
est synth�tis� � des moments pr�cis :
-
Maturation des fruits dits
climact�riques (fruit matur� gr�ce � un pic d��thyl�ne)
-
Tissus �g�s, comme la
feuille, qui entrent en s�nescence
Il
joue un r�le dans :
-
Le d�clenchement de l�abscission
des feuilles, fleurs et fruits
-
La lev�e de dormance des
bourgeons axillaires (effet inverse de l�auxine qui maintient les bourgeons en
dormance)
-
Migration � partir d�une synth�se
de 0,5 mL.h�1.kgMF�1
Son
�mission est maximale �
L��thyl�ne
est dit � anti�auxine �.
Synth�se de
l��thyl�ne :

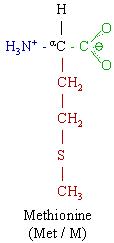
�������������������������������������������������������������������������������������������������������������������������������� ����������� Ad�nosine
���������������������������������� �Activation����������������������������������������������������� ACC
Synthase������������� ������ �
 �������������������������������������������������������������������������������������������������������������������������������������������� ������ S � CH3
�������������������������������������������������������������������������������������������������������������������������������������������� ������ S � CH3
����������������������� �� + �ATP�������� ���������������������������������������������� +� P�P� +� Pi�������������������������� +
�������������������������������������������������������������������������������������������������������������������������������� CH2���������������� COO�
���������������������������������������������������������� �Ad�nosine ��
*��������������������� ����������������������� ��������� �� C
�������������������������������������������������������������������������������������������������������������������������������� CH2���������������� NH3+
�������������������������������������������������������������������������������������������������������������������������������� =
ACC
��������������������������������������������������������������������������������������������������������� = AminoCyclopropane Carboxylique
![]() ����������� CH2����������������
�COO�������������� ACC Oxydase
����������� CH2����������������
�COO�������������� ACC Oxydase
![]() ����������� ��������� ��� C���������������������������� ���������������������������������� H2C 9 CH2
����������� ��������� ��� C���������������������������� ���������������������������������� H2C 9 CH2
����������� CH2���������������� � NH3+
+������������������������������������������������������������������������������� +� CO2� +� H2O� +� HCN
����������� �� O2
Application au
contr�le du m�rissage des fruits :
j
Atmosph�re contr�l�e � post�r�colte � (non satur�) :
-
Pomme,
poire, banane :������������� CO2��������������� "������� Stabilisation
- Banane, p�che, abricot :��������������� CH4��������������� "������� Facilitation
de la maturation
post�r�colte
- Melon, avocat, tomate ���������������������������������������� "������� Ventilation
pour le stockage
-
Fruits
tropicaux���������������������������� ����������������������� "������� R�frig�ration
(hydro�cooling)
Blocage des m�canismes
(maturation
complexe)���������������������������������� "������� R�colte
pile � maturit�
��������������������������������������������������������������������������������� Froid
humide (chambre froide)
k
G�nie g�n�tique :
-
Inhibition de la synth�se
d��thyl�ne (au niveau de l�ACC oxydase) par les techniques antisens. ��������� Exemple : ����� la tomate long life (anti ACC oxydase), la tomate mid life
����
"
Int�ressantes pour les coulis, concentr�, etc.
 ����������� ADN������������������������������������� ����������� ARN�� ���������������������������������������������� � Prot�ine
����������� ADN������������������������������������� ����������� ARN�� ���������������������������������������������� � Prot�ine
�����������
![]() ���������������������������������� Transcription������������������������������������ Traduction
���������������������������������� Transcription������������������������������������ Traduction
![]()
![]() ��������������������������������������������������������������������������������������������� impossible
��������������������������������������������������������������������������������������������� impossible
��������������������������������������������������������������������������������������������������������������������������������
��������������������������������������������������������������������������������� Hybridation
��������������������������������������������������������������������������������� avec
un antisens
Remarques :
M�rissage
des bananes :�������� 95 % de N2� et� 5 %
d��thyl�ne �������� pendant 24 H �
� Intervention de l�acide
abscissique :
L�acide
abscissique est d�couvert en 1963 dans le cotonnier.
-
Il favorise la formation de la
couche abscissique (anti�auxine)
-
Il y a une accumulation en jours
courts dans les graines et les bourgeons
"
Il joue un r�le dans l�entr�e en
dormance des bourgeons auxiliaires (dormine)
-
Il stimule la tub�risation.
-
Il s�agit d�une hormone de
� d�tresse �
v D�autres hormones ?
-
L�acide salicylique :���������� Inhibiteur de la synth�se d��thyl�ne
-
L�acide jasmonique :�������� Stimulateur de la �thyl�ne,
Acc�l�rateur de la d�gradation des
pigments,
Inhibiteur de la croissance des racines
-
Les polyamines
v Aspects morphologiques et
biologiques :
� D�finition :
Il
s�agit du processus de diff�renciation (changement qualification d��tat :
potentiel de la plante � fleurir)
� Transformation
de l�apex :
Il
s�agit du passage de l��tat v�g�tatif � l��tat reproducteur :
 ����������� Apex v�g�tatif :
����������� Apex v�g�tatif :
![]() ��������������������������������������������������������������������������������������������� Pro�m�rist�me
sporog�ne
��������������������������������������������������������������������������������������������� Pro�m�rist�me
sporog�ne
![]() ����������� ����� Anneau initial
����������� ����� Anneau initial
![]() ��������������������������������������������������������������������������������������������� Pro�m�rist�me
respectaculaire
��������������������������������������������������������������������������������������������� Pro�m�rist�me
respectaculaire
![]()
![]() ����������� M�rist�me
m�dullaire
����������� M�rist�me
m�dullaire
��������������������������������������������������������������������������������������������� ��� =��
M�rist�me d�attente
�����������
Apex floral :

![]() ��������������������������������������������������������������������������������������������������������� A
l�origine des organes floraux :
��������������������������������������������������������������������������������������������������������� A
l�origine des organes floraux :
![]()
R�ceptacle floral
-
S�pales,���� (de
l�ext�rieur)
-
![]() P�tales,
P�tales,
-
Etamines,
-
Carpelles� (vers l�int�rieur)
� Cycle
biologique :
La
transformation d�pend de la plante : floraison unique, annuelle, � une
certaine saison, apr�s 30 ann�es de vie v�g�tative.
"�
On parle d�aptitude � fleurir.
Germination :
D�but de la croissance d'une graine m�re, g�n�ralement dormante Emergence :
Apparition des organes a�riens � la surface du sol. Montaison :
D�veloppement et croissance de la plante Epiaison :
Chez les gramin�es, apparition de l'�pi (bl�) ou de la panicule (avoine) au
sommet de la derni�re gaine. Fruitaison :
Apparition du fruit.
� Plantes monocarpiques :
Ces
plantes ne fleurissent qu�une seule fois.
Exemple des
c�r�ales :
![]() j
Dites � de printemps � :��������������������������������������� cycle
d�environ 8 mois
j
Dites � de printemps � :��������������������������������������� cycle
d�environ 8 mois
|
Automne |
Hivers |
Printemps |
Et� |
|
|
� |
� |
Germination Emergence |
Montaison Epiaison |
… Mort |
![]() k
Dites � d�hivers � :
k
Dites � d�hivers � :
|
Automne |
Hivers |
Printemps |
Et� |
|
|
� |
Germination Emergence |
� |
Montaison Epiaison |
… Mort |
Ce
sont des fausses bisannuelles : elles sont � cheval sur 2 ann�es civiles
mais leur cycle est inf�rieur � 12 mois.
Ces
c�r�ales n�cessitent de passer l�hivers sous forme de rosette. Si elles sont
plant�es au printemps, il n�y a pas de graines.
Cas des
bisannuelles :
��������������������������������������������������������������������������������������������������������� Carottes,
betteraves, digitales, �
![]() j
Exemple de
j
Exemple de
|
Printemps |
Et� |
Automne |
Hivers |
Printemps |
Et� |
|
|
Germination Emergence |
D�veloppement
uniquement v�g�tatif |
Montaison |
Fruitaison |
… Mort |
||
De
m�me que les c�r�ales d�hivers, les bisannuelles ont besoin de basses
temp�ratures pour qu�il y ait une floraison.
Cette
application aux basses temp�ratures est appel�e vernalisation. Mais on verra qu�il ne faut pas que cette condition.
k
Cas des plantes pluriannuelles mais monocarpiques :
Agare, �
L�ann�e
de floraison est la derni�re ann�e du cycle.
� Plantes polycarpiques :
Il
y a plusieurs floraisons sur plusieurs ann�es successives.
� Acquisition des comp�tences
n�cessaires � la mise � fleur :


� ��������������������� ���������������������������������������������� M�rist�me������ ��
M�rist�me��� ������ M�rist�me
Pas pour les annuelles�� ����������������������� � v�g�tatif������� inflorescentiel������������ floral
|
M�rist�me v�g�tatif |
|
M�rist�me apte � fleurir |
Conditions tropiques
photop�riodiques : |
Initiation florale |
Croissance des organes floraux |
|
|
-
Plante
indiff�rente, -
Plante
pr�f�rente, -
besoin
absolu de la vernalisation |
|
-
Plante
indiff�rent, -
Plante
de jours courts, -
Plante
de jours longs |
=
Mise en place des organes floraux |
|
v Aspects physiologiques =
conditions trophiques et thermiques :
� Conditions
trophiques :
Une
plante a besoin de r�serve (ce n�est pas qu�un aspect quantitatif mais
aussi qualitatif) :
-
Pour la floraison� "� R�serve de compos�s carbon�s
-
Pour la poursuite de l��tat
v�g�tatif (�bauche de feuille)� "� R�serve de compos�s azot�s
� Thermo�induction
froide = Vernalisation :
� Les diff�rents besoins en
froid :
Plantes �
besoins nuls :
Il s�agit des plantes
indiff�rentes : les plantes annuelles (c�r�ales de printemps)
Plantes �
besoins relatifs :
Il s�agit des plantes pr�f�rentes :
j �Exemple des
c�r�ales d�hivers (fausse bisannuelle)
�Exemple des
c�r�ales d�hivers (fausse bisannuelle)
���������������������������������������������������������������������������������������������������������������������������� Floraison
tardive
���������������������������������������������������������������������� � 25
feuilles �
���������������������������������������������� � 7
feuilles �
����������������������� � 1 � 2
feuilles �
����������� �
����������������������������������������������
k Exemple de
 Jusquiame
(bisannuelle vraie) :
Jusquiame
(bisannuelle vraie) :
����������������������� Printemps������ Et������� � Automne���
Hivers��� � Printemps����
Et�
6 semaines � ![]()
���������������������������������������������������������������������� ����� Mort
![]() ��������������������������������������������������������������������������������������������������������� "�
Cycle annuel
��������������������������������������������������������������������������������������������������������� "�
Cycle annuel
![]()
![]()
![]()
On
parle de besoins relatifs car, des fois, ils peuvent �tre absolus.
� Caract�ristiques de la
vernalisation :
�
Maturation
de vernalisation :
Une
plante mature est une plante r�ceptrice de la vernalisation.
-
Pour les c�r�ales d�hivers,
c�est au stade de semence,
-
Pour la Jusquiame noire
bisannuelle, c�est au stade de rosette.
�
Sur
des tissus m�taboliquement actifs :
Exemple :
Les c�r�ales d�hivers :
Si
on les hydrate et on les met au froid, les graines r�agissent comme celles de
c�r�ales de printemps.
|
Vernalisation pas
efficace : |
El�ments n�cessaires � la
vernalisation : |
|
Grains
secs |
H2O |
|
Grains
hydrat�s + 2,4 DNP (dinitroph�nol) |
O2� (activit� respiratoire) |
|
Embryon
isol� |
R�serves
de Carbone |
�
Temp�rature
optimale de vernalisation :
Exemples :
-
C�r�ales d�hivers :����������������������������������� 1 mois � 2 �
5 �C
-
Jusquiame noire
bisannuelle :����� 6 semaines � 5 �C
-
Olivier :��������������������������������������� quelques
semaines � 13 �C
�
Application
du froid continue ou discontinue :
Exemple :
Les c�r�ales d�hivers :
On
peut effectuer une alternance de 2 � 3 jours � 2 � 5 �C sur 2 � 3 jours � 12 � 13
�C.
"
Il faut que la somme des p�riodes
froides soit sup�rieure � 1 mois.
�
D�vernalisation
:
Exemple :
Les c�r�ales d�hivers :
On
applique un froid (2 � 5 �C) pendant un mois puis, imm�diatement apr�s, 7 jours
� 35 �C. "
On aura alors une floraison tardive.
Si
on attend avant d�appliquer les 35 �C, il n�y aura pas de retard dans la
floraison.
� M�canisme de la
vernalisation :
La
vernalisation est diff�rente de la floraison. Il s�agit en fait de
l�acquisition d�une aptitude � fleurir.
j Exemple de
greffage :
|
Greffon |
Porte greffe |
R�sultat |
|
Rameau
de Jusquiame noire bisannuelle non vernalis�e |
Jusquiame
noire bisannuelle vernalis�e |
Floraison
du greffon " Signal |
|
Jusquiame
noire annuelle |
Floraison " Signal pr�sent naturellement |
|
|
Tabac
(plante annuelle) |
Floraison " Signal universel |
� Il y a
la pr�sence d�un signal transmis par hormone.
A ce jour, on
ne la toujours pas isol�e mais elle a d�j� un nom : la vernaline�
k R�le
des gibb�rellines :
-
GA3 induit la floraison.
Exemple de la carotte qui peut fleurir
sans �tre vernalis�e avec, � la place, un apport de GA3. Mais cela ne marche
pas avec toutes les esp�ces.
-
CCC supprime l�effet de la
vernalisation.
-
Les gibb�rellines n�agissent pas
seules
� Applications :
Elles
sont d�ordre agronomiques et horticoles.
Petite
histoire qui a pos� un probl�me d��thique : l�affaire Lyssenko Trofime (1898 � 1976)
Les
sovi�tiques avaient leur autonomie mais il y avait des probl�mes
climatiques : la belle saison �tait trop courte pour le bl� de printemps
et l�hivers �tait soit trop rigoureux (Ukraine), soit trop doux (Sud du
Caucase) pour le bl� d�hivers. Il a fallu la vernalisation artificielle des
grains de bl� d�hivers.
Lyssenko : � On s�en fout de l�origine g�n�tique de
l�individu, l�environnement change tout. La g�n�tique n�a plus besoin d��tre
enseign�e car il ne s�agit que de croisements hasardeux �
"
Th�orie de la dominance des facteurs environnementaux sur l�origine g�n�tique.
Un
ajout qualitatif permet de modifier un individu et de le transmettre � se
descendance.
Lyssenkisme = divergence jusqu�en 1962 avec la g�n�tique
mend�lienne et de Watson et Cricks.
� Thermo�induction
chaude :
Elle
entra�ne la formation d��bauches florales. Il s�agit plus qu�une acquisition de
potentiel.
Elle
concerne essentiellement les plantes � bulbe.
Exemples :
-
Les tulipes :���������������������� temp�ratures douces (20 �
25 �C)
-
L�ail et les oignons :��������� temp�ratures fra�ches (10 � 15 �C)
� Exemple de la tulipe :
�
Cycle
de culture :
|
Octobre
� Novembre |
Janvier
� F�vrier |
Mars
� Avril |
Juin |
|
Plantations
des bulbes |
D�but
de v�g�tation |
Floraison |
Retrait
des bulbes |
�
Conditions
thermiques optimales :

�������
Et������������������������������������������ � ��Printemps � Hivers
20
�C
����������� �� Ebauches ���������������� Lev�e
de dormance
�����������
����������� ���� Florales����� ����� �par les basses temp�ratures�������������������� R�chauffement
��������������������������������������������������������������������������������������������������������� progressif
����������� �� dormantes ������������� ( ≠� Vernalisation )���������������� ���� " Epanouissement de la fleur
�8 �C
Automne � Hivers
���������������������������������� �3������������������������������������������� ��� 16�������������������������� � 21����������������� Semaines
v Aspects physiologiques =
photop�riodes et mise � fleur :
� D�finitions :
Photop�riodisme :
Ensemble
des r�actions d�un organisme influenc�es par l�alternance quotidienne des jours
et des nuits avec ses variations annuelles.
Nycth�m�re :
R�partition
jour � nuit sur une journ�e (24H)
![]()
����������� 0
H��������������������������������������������������������������������������������������������������� 24H
����������������������� �H�m�rop�riode�������������������������������� � Nyctip�riode
����������������������� ou Photop�riode������������������������������� ou Scotop�riode

� Esp�ce indiff�rente � la
longueur du jour :
�
Plante
ap�riodique :
Exemple :
Pomme de terre

������������������ F������ ��� =������������ F������ � =���� ���� F� ������ =��������� F
�
Plante
photop�riodique :
Exemple :
Tomate, Pois, Lilas, Cerisier

������������������ F���������������� �� F������������� =������ �� F��� �����
= ����� F
����������������������� ������� MT
MT : Minimum
trophique� =�
minimum de lumi�re pour la photosynth�se
����������� Environ 5 Heures, jusqu�� 8 H
� Esp�ce sensible � la longueur
du jour :
�
Plante
h�m�rop�riodique absolue :
Exemple :
C�r�ales d�hivers, Bruy�re, Carotte,
Jusquiame
noire bisannuelle

���������������������������������������������������������� ��� f
���������������������������������������������������������� �������� f
������������������������������������������������������� �������� F
������������������ F������ � ������ F������ ������������������ � ������ �������F
���������������������������������� MT����� ������
HC
HC :
H�m�rop�riode critique� =�
dur�e d��clairement � d�passer pour avoir une floraison
MT <
HC������������������ Plus
elle sera d�pass�e, plus la floraison sera importante (= plante de jours longs)
�
Plante
h�m�rop�riodique pr�f�rente :
� MT=HC .����������

���������������������������������� �
��������� f
���������������������������������������������� �������� f
���������������������������������������������� �������� �������� F
������������������������������������� ������������������ � ������ ������������������ �������F
����������������������� ������� MT=HC
�
Plante
nyctyp�riodique absolue :
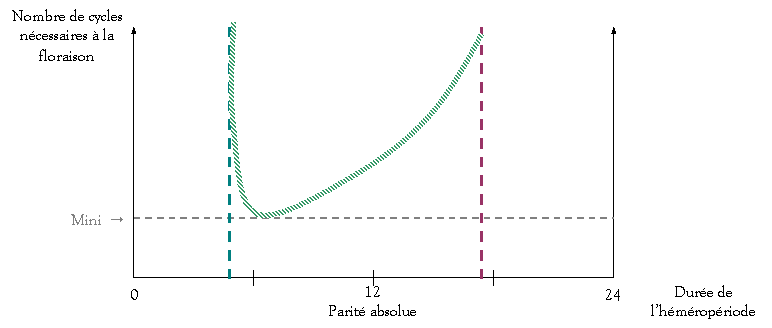
���������������������������������� ���������������������������������������������� ������ ����f
����������� ����������������������� ����������������������� ����������������������� �f
���������������������������������������������� �������� F
�������� �������� � ���������������� F
���������������������������������� MT���������������������������������������������������� �� HC
HC : H�m�rop�riode
critique� =�
dur�e d��clairement � ne d�passer pour avoir une floraison
����������� ����������������������� Plus
on s�en approche, plus la floraison est importante (= plante de jours courts)
�
Plante
nyctip�riodique pr�f�rente :
������������������

���������������������������������� ���������������������������������������������������������������������� ������ ����f
��������������������������������������������������������������������������������������������������������� f
����������� ����������������������� ����������������������� ���������������������������������� �
��������������������������������������������������������������������������������� ������� F
���������������������������������������������� �������� �F
�������� �������� � ���������������� F
����������������������� ����������� MT���������������������������������������������������� ��� HC
�
Plante
amphip�riodique :
Exemple :
quelques vari�t�s de tomates

���������������������������������������������������������� �f�������������������������������� �� f
���������������������������������������������������������� � ���f���������������������� f
���������������������������������������������� ������ F��������� ���� F
������������������ F���������������� F������ �������� �����
F��������������� � ������ F
���������������������������������� MT����� ������
HC1 ������������������������������ ��HC2
HC1 :
H�m�rop�riode critique� =�
dur�e d��clairement � d�passer pour avoir une floraison
HC2 :
H�m�rop�riode critique� =�
dur�e d��clairement � ne d�passer pour avoir une floraison
� Caract�ristique
du photop�riodisme :
� Eup�riode et
dysp�riode :
Eup�riode :
Conditions photop�riodiques favorables � la floraison (= initiation florale)
Exemples :
-
Plante nyctip�riode :������� Lampourde���� "������� 1 jour court
-
Plante h�m�rop�riode :�� C�leri������������� "������� 4 jours longs
Betterave������� "������� 18 jours longs
Dysp�riode :
Conditions photop�riodiques d�favorables � la floraison.
� Efficacit� des �clairements
faibles :
j Esp�ces
de jours courts en eup�riode :
 ����������������������� 950
W.m�2
����������������������� 950
W.m�2
��������������������������������������������������������������������������������������������������������������������� ��
Floraison
���������������������������������������������� ������ 50 W.m�2
��������������������������������������������������������������������������������������������������������������������� ��
Pas de floraison
��������������������������������������������������������������������������������������������������������� ������� (r�version de l�initiation
���������������������������������������������� �� = �clairement faible����������������������������������� ����������� florale)
���������������������������������������������� (� �clairement de la lune)
k Esp�ces
de jours longs en dysp�riode :
 ����������������������� 950
W.m�2
����������������������� 950
W.m�2
��������������������������������������������������������������������������������������������������������������������� ��
Pas de floraison
����������������������� ���������������������������������� ����������� ����������� ����������� 50 W.m�2
��������������������������������������������������������������������������������������������������������������������� ��
Floraison
��������������������������������������������������������������������������������������������������������� �������
�
Spectre
d�action des �clairements :
�L�efficacit� de l
d�pend de sa longueur d�onde et de son intensit�.
��������������������������������������������������������������������������������������������������������������������� J.m�2
������������� Efficacit�
 �������������������������������������������������������������������������������������������������������������������������������������������� � de l :
�������������������������������������������������������������������������������������������������������������������������������������������� � de l :
 250��������������������������������������������������������������������������������������������������� 25
000
250��������������������������������������������������������������������������������������������������� 25
000
200��������������������������������������������������������������������������������������������������� 20
000
150��������������������������������������������������������������������������������������������������� 15
000
100��������������������������������������������������������������������������������������������������� 10
000
�
50���������������������������������������������������������������������������������������������������
5 000
����������� (UV)��� ��
560������� 600������� 640������� 680������� 720������� 760 �������800 ��� (IR)
����������� ���������������������������������� ����� Rouge clair��������� Rouge sombre
���������������������������������������������������������� R ; red� ����������� FR ; far red
���������������������������������������������� ������ �
665 nm ���������������������� ���
735 nm
� Antagonisme rouge clair /
rouge sombre :
Exemple :
la Lampourde (plante de jours courts) :

��������������������������������������������������������������������������������������������������������������������� "�
Floraison
���������������������������������������������������������� Flash
FR
��������������������������������������������������������������������������������������������������������������������� "�
Floraison
���������������������������������������������� ����������� �
Flash R
��������������������������������������������������������������������������������������������������������������������� "�
Pas de floraison
��������������������������������������������������������������������������������������������������������������������� "�
Floraison
Si
on termine par un flash de rouge clair, il n�y a pas de floraison.
Si
on termine par un flash de rouge sombre, il y a une floraison.
�
Le
phytochrome :
= Chromoprot�ine
Prot�ine�
�� S � S� �� Chromophore
����������� ���������������������������������������������� =
t�trapyrrole ouvert
Pour
le dernier pyrrole, il existe 2 conformations possibles (Cis et Trans)
Conversion Pr
� Pfr :

Synth�se�������������������������������� ���� R�version enzymatique��������������������������� ���� D�gradation
La
nuit, le Pfr n�est pas �clair�. Il subit donc sa
d�gradation et sa r�version en Pr.
� Spectre d�absorption :

665����� ������� 735
����������������������� 300����� 400����� 500����� 600����� 700����� 800����������������� l� (nm)
�
La Pfr est toujours la forme active :
j Plantes
de jours longs :
La Pfr
stimule la floraison.

����������� Pr
���������������������������������������������� ���� En position JOUR, le Pr est converti en Pfr qui s�accumule
![]()
![]() ���������������������������������������������������������� Dur�e
d��clairement (665 nm) minimale pour constituer le Pfr.
���������������������������������������������������������� Dur�e
d��clairement (665 nm) minimale pour constituer le Pfr.
����������� Pfr��������������������������������������� =
HC � d�passer
 ��������������������������������������������������������������������������������������������������������������������� "�
Pas de Floraison
��������������������������������������������������������������������������������������������������������������������� "�
Pas de Floraison
��������������������������������������������������������������������������������������������������������������������� "�
Floraison
���������������������������������������������������������� ����� Pr
���������������������������������������������������������� �������� 9
�Conversion en Pfr
k Plantes
de jours courts :
La Pfr
inhibe la floraison.
En position NUIT, le PFR est d�grad� en Pr.

����������� Pfr �������������������������������������� Dur�e
minimale pour d�grader le Pfr.
���������������������������������������������� ����������� = HC � ne pas d�passer
����������������������������������������������������������
����������� Pr�����������������������������
�
Phytochrome
et photomorphogen�se :
Exemple �cophysiologique : L�ombre verte en sous
bois :
Il
y a une comp�tition plante � plante pour la lumi�re, ainsi qu�un auto�ombrage
des feuilles � l�apex sur les feuilles plus basses.

Exemple :
Le tr�fle :
-
Chute d�intensit� de la lumi�re�� "������� Diminution du taux de ramification
-
Chute du ratio� Pr �/ Pfr��������� ����������� "������� Sans effet sur la ramification
Augmentation de la longueur du p�tiole
|
|
Conditions
standard |
Ombre
forte |
|
Intensit�� I |
500� �mol.m�2.s�1 |
150
�mol.m�2.s�1 |
|
Ratio� Pr �/ Pfr |
1,15 |
0,1 |
|
|
Stolons
tr�s ramifi�s P�tioles
courts |
Stolons
peu ramifi�s P�tioles
longs |
|
|
Occupation
maximale de l�espace optimum |
|
Photosensibilit�
des g�nes : S�quences promotrices
photosensibles :
Exemple :
Promoteur du g�ne rbcS de la sous�unit� de la rubisco (chez le pois)
|
|
|
|
+ + + |
� |
|
+ + |
� |
|
+ |
� |
|
� |
� |
|
+ + + |
+ + + |
|
+ + + |
� � � |

� Nature
hormonale du photop�riodisme :
� Site de perception diff�rent
du site de r�action :
Exemple :
La lampourde (plante de jours cours) :
|
Greffon |
Porte
greffe |
|
|
Bourgeon
auxiliaire en
jours longs |
Feuilles
isol�es en
jours longs "
Dysp�riode |
"� Pas de floraison |
|
Feuilles
isol�es en
jours longs "
Eup�riode |
"� Floraison |
� Le stimulus agit � faible
concentration :
Exemple :
La lampourde :

Une
feuille en eup�riode permet de d�clencher une floraison chez toute la plante.
� Le stimulus peut �tre
inhib� :
Exemple :
La lampourde :

���������������������������������������������������������� "�
Pas de floraison
����������� ���������������������������������������������������������� "�
Floraison plus abondante
Les
feuilles en dysp�riode cr�ent une inhibition.
� L�inhibition peut �tre
totale :
Exemple :
L��pinard (plante de jours longs) :

Le
signal dysp�riodique peut �tre suffisamment important pour annuler le signal eup�riodique.
� Le stimulus est non
sp�cifique :
|
Greffon |
Porte greffe |
|
Rameau
d�foli� de tabac (jours courts) cultiv� en jours longs |
Jusquiame
bisannuelle (jours longs) cultiv�e
en jours longs |
"�
Floraison.
Quelle est
l�hormone ?
Une hormone
florig�ne, appel�e anthocaline, mais elle n�est pas encore d�couverte�
� Conclusion
:
La
mise � fleur est une diff�renciation, un changement d��tat, du m�rist�me
v�g�tatif en m�rist�me reproducteur puis floral.
j Cas
complexe :
Il y a
un nombre �lev� de conditions diff�rentes.
Exemple
de la jusquiame noire bisannuelle :

k Cas
particulier :
Exemple
des bulbes :

l Cas
simples :
Exemple
des lilas, pois, cerisier :
